
【题目】中国传统文化对人类文明贡献巨大,《本草纲目》中有如下记载:“(火药)乃焰消(KNO3)、硫黄、杉木炭所合,以为烽燧铳机诸药者”,其中利用KNO3的性质是( )
A. 自燃性 B. 稳定性 C. 还原性 D. 氧化性
科目:高中化学 来源: 题型:
【题目】环境污染影响人类生存,治理污染是化学工作者研究的重要课题。
(1)可用CO与H2合成甲醇(CH3OH),己知CO、CH3OH(l)、H2的燃烧热分别为:a kJ·mol-1、b kJ·mol-1、c kJ·mol-1,请写出合成CH3OH(l)的热化学方程式:___________________________________。
(2)反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g)在容积固定的密闭容器中进行,其平衡常数K与温度T的关系如图所示。
Fe(s)+CO2(g)在容积固定的密闭容器中进行,其平衡常数K与温度T的关系如图所示。
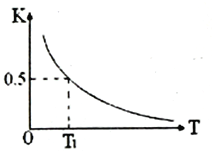
①该反应是________(填“吸热”或“放热”)反应。
②一定条件下,下列能说明该反应达到平衡状态的是__________
a.混合气体的密度不再变化 b.容器内压强不再变化
c. v(CO2)=v(CO) d. CO在混合气中的质量分数保持不变
③写出该反应的平衡常数表达式______________________________________;T1温度下,加入FeO和CO反应达平衡时CO的转化率为 ________________________________。
(3)①把含二氧化硫的工业烟气通入含Cr2O72-和Cr3+的酸性电镀废液中(Cr2O72-被还原为Cr3+,Cr3+能水解),写出该反应的离子方程式:_________________________。
②反应一段时间后开始出现Cr(OH)3沉淀,用必要的离子方程式和文字,表述产生沉淀的原因:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X分别与Y、Z形成10电子的化合物P和Q。P能使湿润的红色石蕊试纸变蓝,Q常温下是一种液体。下列说法正确的是
A. 简单离子半径大小关系为W>Z
B. P形成的水溶液能导电,说明P属于电解质
C. 电解W的氯化物水溶液可以得到W单质
D. 由X、Y、Z组成的盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下, 下列各组物质中,Y既能与X反应又能与Z反应的是( )
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 稀盐酸 |
③ | O2 | N2 | H2 |
④ | FeCl3溶液 | Cu | 浓硝酸 |
A. ①③ B. ①④ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24 L H2中所含质子数、中子数均为2NA
B. 71g 氯气与足量铁粉充分反应,转移的电子数为3NA
C. IL 1 mol·L-1的盐酸中所含粒子总数为2NA
D. 同质量、不同密度的N2和CO 中的原子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题为《化学反应原理(选修4)》选做题。
(l)T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C的浓度随时间t的变化如图所示。

该反应的化学方程式为____________。在2分钟内用A的浓度变化表示的平均反应速率为___________mol·L一l·min一l。
(2)一定条件下,上述反应达到化学平衡状态的标志是_____(填字母代号)。
A.v(正)=v(逆)=0
B.各物质的浓度不再变化
C.单位时间内消耗1molA,同时生成3molB
(3)若该反应放出热量,升高温度时,化学反应速率______(填“增大”或“减小”),平衡向______(填“正”或“逆”)反应方向移动。
(4)下图是电解NaCl溶液的示意图。请回答下列问题:
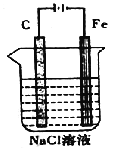
① 石墨电极上的反应式为_____________;
② 电解一段时间后,溶液的pH______(填“增大”“减小”或“不变”)。
(5)水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
① 常温下,0.1mol/LNH4Cl溶液呈______(填“酸”“碱”或“中”)性,溶液中c(NH4+)____c(Cl-)(填“>”“< ”或“=”);
② 已知:20℃时,Ksp(AgCl)=1.1×10-10, Ksp(AgBr)=2.0×10-13。在浓度均为0.01mol/L的NaCl和NaBr混合溶液中,逐滴加入AgNO3溶液,先产生的沉淀是_____(填“AgCl”或“AgBr ”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下n为气体。m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是

A. 原子半径:Z>Y
B. 图示转化关系涉及的反应均为氧化还原反应
C. 最简单气态氢化物的稳定性:W>X
D. 化合物p中只存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,用0.100 0 mol·L-1的盐酸滴定25 mL 0.100 0 mol·L-1 Na2CO3溶液,所得滴定曲线如下图所示。下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是( )
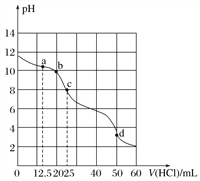
A. a点:c(HCO![]() )>c(Cl-)>c(CO
)>c(Cl-)>c(CO![]() )
)
B. b点:c(Na+)+c(H+)=c(Cl-)+c(HCO![]() )+c(CO
)+c(CO![]() )+c(OH-)
)+c(OH-)
C. c点:c(OH-)+c(CO![]() )=c(H+)+c(H2CO3)
)=c(H+)+c(H2CO3)
D. d点:c(Cl-)=c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com