
| 编号 | I | Ⅱ | Ⅲ |
| 实验 | 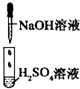 |
 |
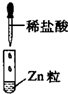 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A、I中混合前后溶液中各离子种类、个数均不变 |
| B、Ⅱ中反应前后溶液中Cu2+、Cl-浓度均未变 |
| C、Ⅱ中BaCl2替换为Ba(NO3)2溶液,发生的离子反应相同 |
| D、Ⅲ中发生的反应属于置换反应,不属于离子反应 |


科目:高中化学 来源: 题型:
 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为0mol?L-1,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为0mol?L-1,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫化钠水解:S2-+2H2O?H2S+2OH- |
| B、碳酸钠与醋酸溶液反应:CO32-+2H+=H2O+CO2↑ |
| C、HCO3-的电离:H2O+HCO3-?CO32-+H3O+ |
| D、NaHS在水中的电离:NaHS?Na++HS- HS-?H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性 HClO4<HBrO4<HIO4 |
| B、碱性 NaOH>Mg(OH)2>Al(OH)3 |
| C、稳定性 HCl>PH3>H2S |
| D、还原性 Cl->Br->I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、(1) |
| C、(2) | D、(3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com