
【题目】I.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是___。
(2)In的最高价氧化物的水化物的碱性___Ba(OH)2的碱性(填“>”或“<”)。
(3)![]() In的中子数与电子数的差值为___。
In的中子数与电子数的差值为___。
II.A+、B2-、C-、D、E、F3+分别表示含10个电子的六种粒子(离子或分子)。其中:
a.A+、B2-、F3+核外电子层结构相同
b.C-是由两种元素组成的
C.D是两种元素组成的四原子分子
d.E在常温下是无色液体
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失
(4)C-的电子式:___。
(5)A+、B2-、F3+离子半径由大到小的顺序为___(用离子符号表示)。
(6)电子式表示A2B的形成过程___。
(7)含F3+的溶液中通入过量D,反应的离子方程式是___。
(8)A单质与E反应的离子方程式为___,生成的化合物中化学键的类型是___。
III.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(9)Se原子结构示意图可表示为___。
(10)下列说法合理的是___。
a.SeO2既有氧化性又有还原性
b.浓硒酸可能具有强氧化性、脱水性
c.热稳定性:H2Se<HCl<H2S
d.酸性:H2SeO4<HBrO4<HClO4
【答案】第5周期IIIA族 < 17 ![]() O2->Na+>Al3+
O2->Na+>Al3+ ![]() Al3++3NH3+3H2O=Al(OH)3↓+3NH4+ 2Na+2H2O=2Na++2OH-+H2↑ 离子键和极性键
Al3++3NH3+3H2O=Al(OH)3↓+3NH4+ 2Na+2H2O=2Na++2OH-+H2↑ 离子键和极性键 ![]() abd
abd
【解析】
I.(1)In的原子结构中含5个电子层、最外层电子数为3;
(2)金属性Ba大于In;
(3)中子数为115-49=66,电子数为49;
II.A+、B2-、C-、D、E、F3+分别表示含10个电子的六种粒子(离子或分子),其中:
a.A+、B2-、F3+核外电子层结构相同,可知A为Na、B为O、F为Al;
b.C-是由两种元素组成的,C-为OH-;
c.D是两种元素组成的四原子分子,D为NH3;
d.E在常温下是无色液体,E为H2O;
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失,白色沉淀为氢氧化铝;
III.(9)Se原子的质子数为34;
(10)a.Se为+4价,为中间价;
b.浓硒酸与浓硫酸性质类似;
c.非金属性越强,对应氢化物越稳定;
d.非金属性越强,对应最高价含氧酸的酸性越强。
I.(1)In的原子结构中含5个电子层、最外层电子数为3,位于元素周期表中第五周期ⅢA族;
(2)金属性Ba大于In,则In的最高价氧化物的水化物的碱性<Ba(OH)2的碱性;
(3)中子数为115-49=66,电子数为49,中子数与电子数的差值为66-49=17;
II.(4)C-的电子式为![]() ;
;
(5)具有相同电子排布的离子,原子序数大的离子半径小,则A+、B2-、F3+离子半径由大到小的顺序为O2->Na+>Al3+;
(6)电子式表示A2B的形成过程为![]() ;
;
(7)含F3+的溶液中通入过量D,反应的离子方程式是Al3++3NH3+3H2O=Al(OH)3↓+3NH4+;
(8)A单质与E反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,生成的化合物为NaOH,含化学键的类型是离子键和极性键;
(9)Se原子结构示意图可表示为 ;
;
(10)a.Se为+4价,为中间价,则SeO2既有氧化性又有还原性,故a正确;
b.浓硒酸与浓硫酸性质类似,可能具有强氧化性、脱水性,故b正确;
c.非金属性越强,对应氢化物越稳定,则热稳定性:H2Se<H2S<HCl,故c错误;
d.非金属性越强,对应最高价含氧酸的酸性越强,则H2SeO4<HBrO4<HClO4,故d正确;
故答案为:abd。


科目:高中化学 来源: 题型:
【题目】已知:从石油中获得A是目前工业上生产A的主要途径,A的产量通常用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
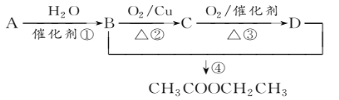
回答下列问题:
(1)写出A的结构简式______________。
(2)B、D分子中的官能团名称分别是_______________、________________。
(3)写出下列反应的反应类型:①_________,②________,④__________。
(4)写出下列反应的化学方程式:
①________________________________________________________________;
②________________________________________________________________。
③________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
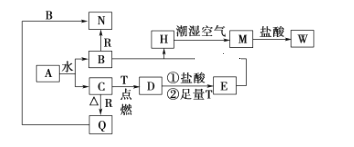
(1)写出下列物质的化学式A:_______________,Q:_____________,W:__________________。
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:_______________________
②R与B溶液反应时的离子方程式:___________________________________
③D与盐酸反应的离子方程式:_______________________________________
(3)简述检验气体C的方法:___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙3个烧杯中分别装有稀H2SO4、CuCl2溶液、饱和食盐水,甲中电极为锌片和铜片,乙中电极为石墨棒C1、C2,丙中电极为石墨棒C3、铁片,电极之间用导线相连。则下列叙述正确的是
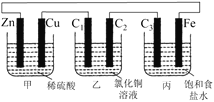
A.C1和C3放出的气体相同,铜片和铁片放出的气体也相同
B.C3是阴极,锌片、C2上都发生氧化反应
C.甲中H+向铜电极移动,丙中Cl-向铁电极移动
D.甲中硫酸溶液的浓度逐渐变小,丙中溶液的pH逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1 mol共价键所需要吸收的能量分别为H—H:436 kJ,I—I:151 kJ,H—I:299 kJ,下列对H2(g)+I2(g)![]() 2HI(g)的反应类型判断错误的是( )
2HI(g)的反应类型判断错误的是( )
A.放出能量的反应B.吸收能量的反应
C.氧化还原反应D.可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有___。
(2)磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4![]() 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4
①该反应体现出酸性关系:H3PO4___H2SO4(填“>”或“<”)。
②结合元素周期律解释①中结论:P和S电子层数相同,___。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:__。
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:___。
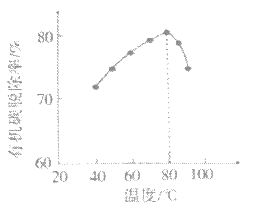
(5)脱硫时,CaCO3稍过量,充分反应后仍有SO42-残留,加入BaCO3可进一步提高硫的脱除率,其离子方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.天然气、水煤气、液化石油气均是生活中常用的燃料,它们的主要成分都是化合物
B.无水![]() 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
C.制玻璃和水泥都要用到石灰石原料
D.1996年人工合成了第112号元素鎶(Cn),盛放鎶的容器上应该贴的标签是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图所示:
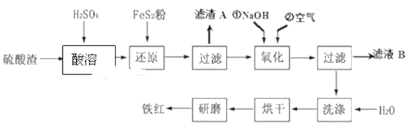
回答下列问题:
(1)酸溶时,粉碎硫酸渣的目的是__________
(2)还原过程中加入FeS2粉增大溶液中Fe2+的含量,同时有H2SO4生成,完成该反应的离子方程式:FeS2+14Fe3++______H2O═15Fe2++______SO42-+______.______________
(3)滤渣A的主要成分为__________
(4)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_____;(部分阳离子以氢氧化物形式沉淀时溶液的pH见表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
为得到纯净的Fe(OH)3固体,需要对沉淀进行洗涤,判断沉淀Fe(OH)3是否洗净的方法是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1905年哈珀开发实现了以氮气和氢气为原料合成氨气,生产的氨制造氮肥服务于农业,养活了地球三分之一的人口,哈珀也因此获得了1918年的诺贝尔化学奖。
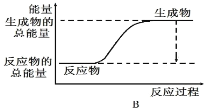
(1)工业合成氨的反应如下:N2+3H2 2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为__________kJ。 下图能正确表示该反应中能量变化的是__________(填“A”或“B”)。
2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为__________kJ。 下图能正确表示该反应中能量变化的是__________(填“A”或“B”)。

(2)反应2NH3(g)![]() N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
实验序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
① | 400℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
② | 400℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
③ | 500℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据回答:实验①②中,有一个实验使用了催化剂,它是实验_____(填序号);实验①③对比说明了_________________________________。在恒温恒容条件下,判断该反应达到化学平衡状态的标志是_________(填序号)。
a. NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
(3)近日美国犹他大学 Minteer教授成功构筑了H2—N2生物燃料电池。该电池类似燃料电池原理,以氮气和氢气为原料、氢化酶和固氮酶为两极催化剂、质子交换膜(能够传递H+)为隔膜,在室温条件下即实现了氨的合成同时还能提供电能。则A电极为_____极(填“正”、“负”),该电池放电时溶液中的H+向______极移动(填“A”、“B”)。
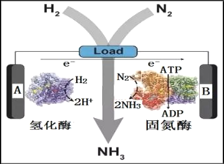
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com