
【题目】元素周期表中主族元素左上角与右下角元素性质相似,如Be和Al、B和Si、……,则下列说法错误的是
A.BeO是两性化合物B.Li2CO3和LiOH均易溶于水
C.1molBe与NaOH溶液反应可生成1molH2D.已知Si熔沸点高则B熔沸点也高
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】某同学用某种粗盐进行提纯实验,步骤见下图。请回答:
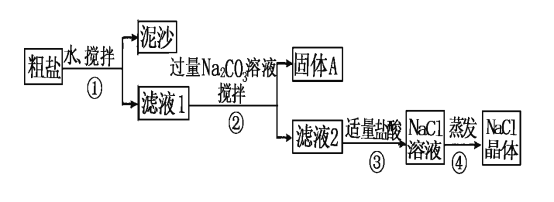
(1)步骤①和②的操作名称是________________。
(2)步骤②中判断加入碳酸钠是否过量的方法是_____________________
步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止__________________,当蒸发皿中有较多量固体出现时,应___________________________________。
(3)猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | ___________ | 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入________,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想Ⅱ不成立 |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,__________ | __________________ | 猜想Ⅲ成立 |
(4)写出“猜想Ⅲ”中对应的化学反应方程式:______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的摩尔质量为__________。
(2) 标准状况下,0.5molH2和 O2的混合气体所占的体积为________。
(3)8.5 g氢氧根离子含有的电子数目为________。
(4)14 g C2H4与C4H8的混合物所含质子的物质的量为________。
(5)将4gNaOH溶于__________g水中,可使溶液中H2O与Na+的物质的量之比等于20:1,若测得该溶液的密度为1.1g/cm3,则该溶液中c(Na+)为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①R—NO2![]() R—NH2;
R—NH2;

③苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯为原料制备某些化合物的转化关系图:
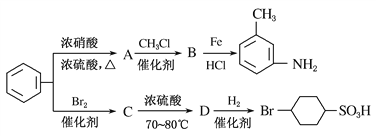
(1)A是一种密度比水________(填“小”或“大”)的无色液体;A转化为B的化学方程式是________________________。
(2)在“![]()
![]() ”的所有反应中属于取代反应的是________(填字母),属于加成反应的是________(填字母)。
”的所有反应中属于取代反应的是________(填字母),属于加成反应的是________(填字母)。
(3)B中苯环上的二氯代物有________种同分异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探宄固体X(仅含两种常见短周期元素)的组成和性质,设计并完成如下实验:

己知:气体A是一种纯净物,在标准状况下的密度为1.429g/L;固体B是光导纤维的主要成分。请回答:
(1)气体A分子的电子式_______,白色沉淀D的化学式_______。
(2)固体X与稀硫酸反应的离子方程式是_______。
(3)己知NH3与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为140g/ mol)和H2,写 出该反应 的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.有以下物质:①石墨; ②氯化氢气体; ③酒精; ④铝; ⑤二氧化碳;
⑥碳酸氢钠固体;⑦氢氧化钡溶液; ⑧液态醋酸; ⑨氯化银固体; ⑩氨气。
(1)其中能导电的是:______________________________;
(2)属于非电解质的是:___________________________。
Ⅱ.氧化铜是一种黑色固体,可溶于稀硫酸,某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解,请你和他一起通过如图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。

(3)通过实验Ⅰ可以证明_____________________________________________________.
(4)要证明另外两种粒子能否与氧化铜反应,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步确认的实验操作是:在Ⅲ中先加入_________,再加入___________。
(5)探究结果为_____________________________________________________________。
(6)反应的离子方程式为_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法错误的是
A. 实验①中,若5min时测得n(M) =0.05mol,则0至5min时间内,用N表示的平均反应速率v(N) =0.01 mol/( L·min)
B. 实验②中,该反应的平衡常数K= 1.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.06
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探索苯结构的过程中,人们写出了符合分子式“C6H6”的多种可能结构(如图),下列说法正确的是
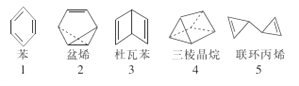
A. 1~5对应的结构中的一氯取代物只有1种的有3个
B. 1~5对应的结构均能使溴的四氯化碳溶液褪色
C. 1~5对应的结构中所有原子均可能处于同一平面的有1个
D. 1~5对应的结构均不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是

A. 通入保护电流使钢管桩表面腐蚀电流接近于零
B. 通电后外电路电子被强制从高硅铸铁流向钢管桩
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com