
【题目】实验室在模拟工业制备和提纯硅时,利用氯气、石英砂和碳粉等原料按以下装置制备了SiCl4。已知SiCl4熔点-70°C,沸点57.6°C,遇水极易水解。

下列说法不正确的是( )
A.实验所用氯气等原料必须预先干燥处理
B.两通管中发生的化学反应为SiO2+C+2Cl2![]() SiCl4+CO2
SiCl4+CO2
C.液体X的作用是液化SiCl4气体,可以选择冰水等作冷却剂
D.若缺少固体Y的装置,实验时Z中可能会出现大量的白色烟雾
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】铁、钴、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)Fe(CO)x常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于______(填晶体类型),若配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___。
(2)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO__FeO(填“>,<或=”),原因是_________。
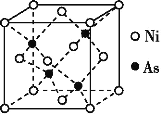
(3)NiAs的晶胞结构如图所示:
①Ni的配位数为____。
②若阿伏伽德罗常数的值为NA,晶体密度为ρ g·cm-3,则该晶胞中最近的Ni之间的距离为______cm。(写出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() ,向同温、同体积的三个真空密闭容器中分别充入气体:
,向同温、同体积的三个真空密闭容器中分别充入气体:![]() 甲
甲![]() 和
和![]() ;
;![]() 乙
乙![]() 和
和![]() ;
;![]() 丙
丙![]() ;恒温、恒容下反应达平衡时,下列关系一定正确的是
;恒温、恒容下反应达平衡时,下列关系一定正确的是![]()
A.容器内压强p:![]()
B.![]() 的质量m:
的质量m:![]()
C.![]() 与
与![]() 之比k:
之比k:![]()
D.反应放出或吸收热量的数值Q:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,2L密闭容器中充入
时,2L密闭容器中充入![]()
![]() ,发生反应:
,发生反应:![]() ,获得如下数据:下列判断正确的是
,获得如下数据:下列判断正确的是![]()
时间 | 0 | 20 | 40 | 60 | 80 | 100 |
|
|
|
|
|
|
|
A.![]() 内,
内,![]()
B.在相同条件下,开始时若向容器中充入的是![]()
![]() ,达到平衡后
,达到平衡后![]() 的转化率为
的转化率为![]()
C.反应达平衡时,吸收的热量为![]() kJ
kJ
D.100s时再通入![]() mol
mol![]() ,达新平衡时
,达新平衡时![]() 的转化率增大
的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气的无害化处理已成为当今汽车工业的一项重要课题,其基本原理是实现2NO(g)+2CO(g)![]() N2(g)+2CO2(g)的反应.关于该反应,下列说法正确的是
N2(g)+2CO2(g)的反应.关于该反应,下列说法正确的是
A.只要使用合理的催化剂及载体,就可完全清除NO和CO
B.使用性能好的催化剂可使反应的反应热增大
C.假设该反应在密闭容器中进行,一段时间后达到平衡时c(NO)=c(CO)
D.该反应达到平衡时v(NO)正=v(CO)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)某化学反应A![]() B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
实验 序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)该反应属于__________反应(填“可逆”或“不可逆”)。
(2)在实验1、2中,有一个实验使用了催化剂。请你利用表中数据判断实验___(填1或2)使用了催化剂,理由是_______________。
(3)该实验表明,影响化学反应速率的因素还有__________。
(II)下图是1molNO2和1molCO反应生成1molCO2和1molNO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:__________________。

该反应的活化能等于____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某学习小组做Na2O2与H2O反应的实验,发现一些有趣的现象:
①取适量Na2O2固体用脱脂棉包好放在石棉网上,然后向脱脂棉上滴加3-4滴水,结果脱脂棉剧烈燃烧。
②取适量Na2O2固体置于试管中,加水使其充分反应至不再产生气体为止,滴入几滴酚酞试液,溶液先变红后褪色。回答有关问题。
(1)写出Na2O2的电子式_______________________。
(2)已知Na2O2可看作二元弱酸H2O2对应的盐,其第一步水解完全进行。写出其第一步水解的离子方程式为___________________________________。
(3)由①实验现象所得出的有关结论是:a.有氧气生成;b.___________________。
(4)Na2O2与H2O反应的离子方程式____________________________________。
II.为探究Na2O2与H2O反应的机理,他们在老师的指导下设计了下图所示装置。连接好装置,打开K1、K2,通过注射器注入适量蒸馏水,充分反应后用气球鼓气,Na2S溶液变浑浊,酸性KMnO4溶液褪色。分别取A、C中溶液滴入几滴酚酞,开始都变红,以后A中溶液很快褪色,C中溶液缓慢褪色。另取A、C中溶液分别加入少量二氧化锰,充分振荡,发现均反应剧烈、产生大量气泡,把带火星的木条伸入试管,木条复燃,向反应后的溶液中滴入几滴酚酞试液,溶液变红不褪色。
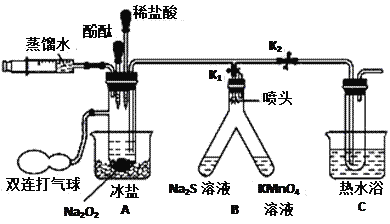
(5)A中冰盐和C中热水的作用分别是__________________,___________________。
(6)用化学方程式表示Na2S变浑浊的原因___________________________________。
(7)用离子方程式表示KMnO4溶液褪色的原因(MnO4-在酸性条件下被还原成Mn2+)__________________________________________。
(8)Na2O2与H2O反应的机理是(用化学方程式表示)第一步_____________________,第二步_______________________________。
(9)若向Na2O2中滴加适量的稀盐酸,也能产生同样的气体,请写出该反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是

A.ZY、ZW、W2X的水溶液都显酸性
B.原子半径大小:W>R>X,简单离子半径大小:R>W>X
C.W的氢化物与R的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W
D.Z与X、Z与R两种元素形成的化合物中均可能存在共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com