
【题目】A、B、C、D、E、F六种元素,它们的核电荷数均小于18,且原子序数逐渐增大。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。11.5g A单质恰好与100mL 5mol/L的盐酸完全反应,反应后溶液呈中性。D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。请回答下列问题:
(1)写出D的元素符号______,E的最高价氧化物的水化物的化学式__________。
(2)画出B元素的离子结构示意图__________________。
(3)若构成F元素的一种原子的质量数为35,写出其原子符号________。
(4)A与F反应的离子方程式为___________________________。
【答案】Si H3PO4 ![]()
![]() H++OH-=H2O
H++OH-=H2O
【解析】
A、B、C、D、E、F六种短周期元素,核电荷数均小于18,且原子序数逐渐增大.A、C、F三种元素的最高价氧化物的水化物之间两两皆能反应,应是氢氧化铝、强碱、强酸之间的反应,且A、C、F三种原子的最外层共有11个电子,可推知A为Na元素、C为Al元素、F为Cl,且符合11.5gA单质恰好与100mL 5mol/L的盐酸完全反应,反应后溶液呈中性;B的原子序数介于Na、Al之间,故B为Mg元素;D元素原子的最外层电子数比次外层电子数少4个,最外层电子数为4,则D为Si元素;E元素原子的次外层电子数比最外层电子数多3个,最外层电子数为8-3=5,故E为P元素,以此来解答。
根据上述推断可知A是Na元素,B是Mg元素,C是Al元素,D是Si元素,E为P元素,F是Cl元素。
(1)由上述分析可知,D为硅元素,元素符号为Si;E为P元素,P元素的最高价氧化物的水化物的化学式为H3PO4;
(2)B元素是Mg,Mg原子核外有12个电子,失去2个电子形成Mg2+,Mg2+离子结构示意图为![]() ;
;
(3)F是Cl元素,Cl元素质子数是17,它的一种原子的质量数为35,则根据原子的表示方法可知其原子符号为![]() ;
;
(4)A、C、F元素最高价氧化物的水化物分别为NaOH、Al(OH)3、HClO4,A与F元素最高价氧化物的水化物反应的化学方程式为NaOH+HClO4=NaClO4+H2O,由于NaOH、HClO4都是可溶性的强电解质,所以反应的离子方程式为H++OH-=H2O。


科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是

A. 加水稀释可以使溶液由c点变到d点
B. 此温度时,Ksp(BaSO4)=1.1×10-10
C. b点有BaSO4沉淀析出
D. a点对应的Ksp等于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,气体被还原的是
A.CO2使Na2O2固体变白B.Cl2使KBr溶液变黄
C.一定条件下H2能使CuO固体变红D.NH3使AlCl3溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )
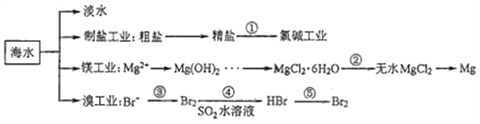
A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。

(1)仪器A的名称为________;A中反应的离子方程式为________。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为________。
②不能证明产生的气体中含有HCl的实验是________(填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:______________________________________。
(4)已知:2S2O32-+I2=== S4O62-+2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL-1 AgNO3溶液滴定所得溶液中的Cl-。
①X中的HClO不会影响I的测定结果,原因是________。
②由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 molL-1 AgNO3溶液的体积应大于________mL(用含V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,X既能与Y反应又能与Z反应的是
Y | X | Z | |
① | H2O(g) | Fe | ZnSO4溶液 |
② | KOH溶液 | Al | 稀硫酸 |
③ | Si | Cl2 | H2 |
④ | 酸性高锰酸钾溶液 | Fe2+(aq) | 漂白液 |
A.①③B.①④C.②③④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于下列反应:2SO2(g) + O2(g) ![]() 2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_____
2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_____
(2)下图表示在密闭容器中反应:2SO2+O2 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是______;b~c过程中改变的条件可能是______________; 若增大压强时,反应速度变化情况画在c~d处。___________

(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应正向为___反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时_____(“增大”、“减小”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法中正确的是

A. 简单离子半径:R>M
B. M和Z两种元素可以共存于同一种离子化合物中
C. 工业冶炼R的单质通常用热还原法
D. 氧化物的水化物酸性:Z<M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com