
【题目】 着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲。红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如下图所示。
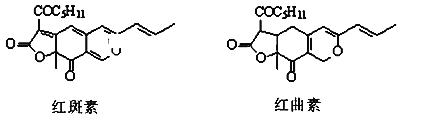
下列说法正确的是
A.红斑素和红曲素都存在2个手性碳原子
B.红斑素和红曲素 属于同分异构体
C.红斑素中含有醚键、羰基、酯键这三种含氧官能团
D.1 mol红曲素最多能与6 mol H2发生加成反应
【答案】C
【解析】
A、根据手性碳原子要求判断;
B、根据红斑素和红曲素的结构及分子组成进行判断;
C、据红斑素和红曲素含有的官能团进行分析;
D、红曲素中含有的羰基和碳碳双键与氢气发生加成反应
A、手性碳原子为连接四个不同的原子或原子团的碳原子,由红斑素和红曲素结构可知,红斑素含有1个手性碳原子,而红曲素含有2个手性碳原子,故A错误;
B、红斑素含有5个碳碳双键,而红曲素含有3个碳碳双键,其他结构相同,因此含有的氢原子数不同,所以它们的分子式不同,一定不是同分异构体,故B错误;
C、红斑素中含有的官能团有:醚键、羰基、酯基三种含氧官能团,故C错正确;
D、1mol红曲素中含有3mol碳碳键和2mol羰基,最多能与5molH2发生加成反应,故D错误;
故选C;


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】有下列几个反应:①向NaAlO2溶液中滴加盐酸;②向盐酸和AlCl3的混合溶液中滴加NaOH溶液;③向NaOH溶液中滴加AlCl3溶液;
⑴符合反应①的图象是______,符合反应②的图象是_____,符合反应③的图象是____;

(2)写出③步骤中的二个离子方程式__________________、________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程,请回答下列问题:
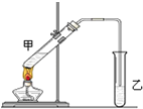
(1)浓硫酸的作用是:①__________②______________;
(2)饱和碳酸钠溶液的主要作用是________________;
(3)装置中通蒸气的导管只能插到饱和碳酸钠溶液的液面处,不能插入溶液中,目的____,长导管的作用是____;
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是____;
(5)进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是____;
(6)实验室可用乙醇来制取乙烯,将生成的乙烯通入溴的四氯化碳溶液,反应后生成物的结构简式是____;
(7)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态,下列描述能说明该反应已达到化学平衡状态的是(填序号)____。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置从含NH4H2PO4和(NH4)2HPO4的废水中回收NH3·H2O和H3PO4,下列说法错误的是( )
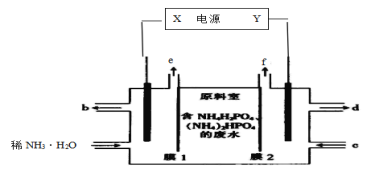
A.电源中X和Y两电极的电势X比Y低
B.膜1为阳离子交换膜,f口放出的是O2
C.阳极区反应之一为:2H2O-4e-+2HPO![]() =O2↑+2H3PO4
=O2↑+2H3PO4
D.每放出11.2L(标准状况下)H2时,能回收98gH3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表短周期中六种元素的原子序数与主要化合价的关系如图:
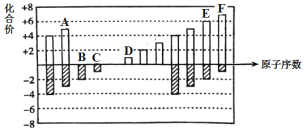
(1)元素F在周期表中的位置是 ______。
(2)元素C、D、E原子半径由大到小的顺序是 ______(填元素符号)。
(3)A、B、C的单质与氢气反应的剧烈程度由强到弱的顺序_____(用单质的化学式表示)。
(4)应用元素周期律和元素周期表的知识,写出D和E所形成的化合物的化学式______、__(写2种)。
(5)根据氯、溴、碘单质间的置换反应,判断F的单质和E的最简单氢化物之间能否发生反应 _____(填“能”或“不能”), 若能则写出反应的化学方程式 ______。
(6)一定温度下,在体积恒定的密闭容器中发生反应:2AB(g)+B2(g) ![]() 2AB2(g)。可以作为达到平衡状态的标志是 ______。
2AB2(g)。可以作为达到平衡状态的标志是 ______。
A. 单位时间内生成nmolB2的同时生成2nmolAB B. 2 ν正(B2)=ν逆(AB2)
C. 混合气体的颜色不再改变(AB2为有色气体) D. 混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
A.2NaBr+Cl2=2NaCl+Br2
B.AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl
C.2H2S+SO2=2H2O+3S↓
D.C+H2O![]() CO+H2
CO+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌原子的价电子排布图:____________________________________________
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是________________
(3)Cd2+与NH3等配体形成配离子。1 mol [Cd(NH3)4]2+含___________mol σ键。该配离子中三种元素的电负性大小关系是:_______________________
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为________
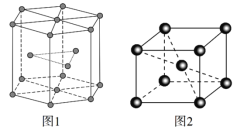
(5)锆晶胞如图1所示,这种堆积方式称为______________________,镉晶胞如图2所示。已知:NA是阿伏加德罗常数的值,晶体密度为d g·cm3。在该晶胞中两个镉原子最近核间距为______nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________(用含π的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研工作者研制出基于PANa(聚丙烯酸钠)电解质的![]() 可充电电池,该电池具有高容量和超长循环稳定性。电池反应为
可充电电池,该电池具有高容量和超长循环稳定性。电池反应为![]()
![]()
![]()
![]()
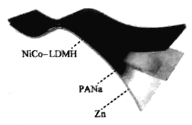
![]() 。PANa是一种超强吸水聚合物,吸收大量
。PANa是一种超强吸水聚合物,吸收大量![]() 和KOH溶液作为水和离子含量调节剂形成水凝胶电解质,示意图如下。下列说法错误的是( )
和KOH溶液作为水和离子含量调节剂形成水凝胶电解质,示意图如下。下列说法错误的是( )
A.PANa是一种有机高分子聚合物,在水溶液中不会发生电离
B.PANa具有超强吸水性可避免电池充放电过程中因失水使离子导电率下降
C.放电时,负极附近pH减小
D.充电时,阳极反应为![]()
![]()
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com