
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。实验室用氯化钠、废铁屑、稀硫酸、氢氧化钾溶液等为原料,通过以下过程制备高铁酸钾(K2FeO4):

(l) Na2O2的电子式为__________。
(2)操作I的步骤为蒸发浓缩、冷却结晶、过滤、洗涤、隔绝空气减压干燥.其中隔绝空气减压干燥的目的是_______。
(3)气体X为____,写出FeSO4与Na2O2反应的化学方程式:________。
(4)最终在溶液中可得到K2FeO4 晶体的原理是_________。
(5)已知K2FeO4在水溶液中可以发生:4FeO42-+10H2O![]() 4Fe(OH)3(胶体)+8OH-+3O2↑,,则K2FeO4 可以在水处理中的作用是__________。
4Fe(OH)3(胶体)+8OH-+3O2↑,,则K2FeO4 可以在水处理中的作用是__________。
(6)称取提纯后的K2FeO4样品0.2100g于烧杯中,加入强碱性亚铬酸盐溶液,反应后再加稀硫酸调节溶液呈强酸性,配成250mL 溶液,取出25.00 mL放入锥形瓶,用0.0l000mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00mL。涉及的主要反应为:Cr(OH)4-+FeO42-=Fe(OH)3+CrO42-+OH-
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
则该K2FeO4样品的纯度为______________.
【答案】 ![]() 将FeSO4·7H2O转变成不含结晶水的FeSO4,同时防止亚铁离子被氧化 O2 FeSO4+4Na2O2=Na2FeO4+2Na2O+Na2SO4+O2↑[答案不唯一, FeSO4+(2+2n)Na2O2=Na2FeO4+2nNa2O+Na2SO4+nO2↑ (n为正整数)] 0℃时K2FeO4的溶解度比Na2FeO4、NaOH、KOH和Na2SO4的溶解度小 杀菌消毒、净水 94.3%
将FeSO4·7H2O转变成不含结晶水的FeSO4,同时防止亚铁离子被氧化 O2 FeSO4+4Na2O2=Na2FeO4+2Na2O+Na2SO4+O2↑[答案不唯一, FeSO4+(2+2n)Na2O2=Na2FeO4+2nNa2O+Na2SO4+nO2↑ (n为正整数)] 0℃时K2FeO4的溶解度比Na2FeO4、NaOH、KOH和Na2SO4的溶解度小 杀菌消毒、净水 94.3%
【解析】 (l) Na2O2属于离子化合物,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)操作I的目的是从硫酸亚铁溶液中获得硫酸亚铁固体,步骤为蒸发浓缩、冷却结晶、过滤、洗涤、隔绝空气减压干燥。其中隔绝空气减压干燥可以将FeSO4·7H2O转变成不含结晶水的FeSO4,同时防止亚铁离子被氧化,故答案为:将FeSO4·7H2O转变成不含结晶水的FeSO4,同时防止亚铁离子被氧化;
(3)过氧化钠与硫酸亚铁反应时,过氧化钠能够与水反应生成氧气,根据流程图, FeSO4与Na2O2反应的化学方程式为FeSO4+4Na2O2=Na2FeO4+2Na2O+Na2SO4+O2↑,故答案为:O2;FeSO4+4Na2O2=Na2FeO4+2Na2O+Na2SO4+O2↑;
(4)根据流程图,0℃时K2FeO4的溶解度比Na2FeO4、NaOH、KOH和Na2SO4的溶解度小,可以从溶液中通过冷却结晶获得K2FeO4 晶体,故答案为:0℃时K2FeO4的溶解度比Na2FeO4、NaOH、KOH和Na2SO4的溶解度小;
(5)根据反应4FeO42-+10H2O![]() 4Fe(OH)3(胶体)+8OH-+3O2↑,,K2FeO4 具有氧化性,能够杀菌消毒,生成的Fe(OH)3(胶体)具有吸附性,可以除去水中的悬浮物,故答案为:杀菌消毒、净水;
4Fe(OH)3(胶体)+8OH-+3O2↑,,K2FeO4 具有氧化性,能够杀菌消毒,生成的Fe(OH)3(胶体)具有吸附性,可以除去水中的悬浮物,故答案为:杀菌消毒、净水;
(6)根据反应Cr(OH)4-+FeO42-═Fe(OH)3↓+CrO42-+OH-和Cr2O72-+6Fe2++14H+═ 6Fe3++2Cr3++ 7H2O,可得关系式2FeO42-~Cr2O72-~6Fe2+,根据题意可知,(NH4)2Fe(SO4)2的物质的量为0.03L×0.01000mol/L=0.0003mol,所以高铁酸钾的质量为0.0003mol×![]() ×198g/mol×
×198g/mol×![]() =0.198g,所以K2FeO4样品的纯度为
=0.198g,所以K2FeO4样品的纯度为![]() ×100%=94.3%,故答案为:94.3%。
×100%=94.3%,故答案为:94.3%。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】某种利胆解痉药的有效成分是亮菌甲素,其结构简式如图所示。下列关于亮菌甲素的说法中,正确的是

A. 亮菌甲素的分子式为C12H12O5
B. 1mol亮菌甲素最多能和2molNaOH反应
C. 1mol亮菌甲素最多能和4molH2发生加成反应
D. 亮菌甲素在一定条件下可以与乙酸发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4g NaOH溶解在10 mL水中,稀释至1 L后,再取出10 mL,这时的物质的量浓度为 ( )
A. 0.01 mol/LB. 0.1 mol/LC. 1 mol/LD. 无法精确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.摩尔质量就等于物质的相对分子质量
B.摩尔质量就是物质相对分子质量的6.02×1023倍
C.HNO3的摩尔质量是63 g
D.硫酸和磷酸的摩尔质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类的说法正确的是( )
A. 所有糖类物质都有甜味,但不一定都溶于水
B. 葡萄糖和果糖性质不同,但分子式相同
C. 摄入人体的纤维素在酶的作用下能水解为葡萄糖
D. 用浓硫酸与蛋白质的颜色反应鉴别部分蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物AM有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与 NaHCO3溶液反应;F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色;D能发生银镜反应;M与NaOH溶液反应后的产物,其一氯代物只有一种。

请回答:
(1)B、F的结构简式分别为____________、____________。
(2)反应①⑦中,属于消去反应的是________ (填反应序号)
(3)D发生银镜反应的化学方程为_________________________________________;
反应⑦的化学方程为__________________________________________________。
(4)A的相对分子质量在180260之间,从以上转化中不能确认A中的某一官能团,确定该官能团的实验步骤和现象为________________________________________。
(5)符合下列条件的F的同分异构体共有________种。
a.能发生银镜反应
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
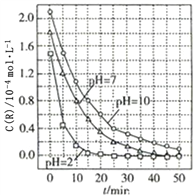
A. 在20~25min之间,pH=10时R的平均降解速率为0.04molL-1min-1
B. 溶液酸性越强,R的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 50min时,pH=2和pH=7时R的降解百分率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com