
【题目】为了证明一氧化碳具有还原性,有人设计了下列实验:
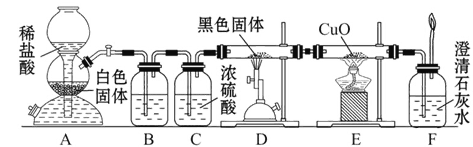
(1)装置A中生成的主要产物是___________________________________________。
(2)装置D中发生反应的化学方程式是___________________________________。
(3)必须用装置C吸收除去气体中水蒸气的理由是_________________________。
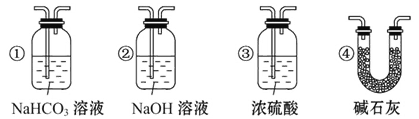
(4)若根据F中石灰水变浑浊的现象也能确定CO具有还原性,应在上图中装置______与______之间连接下列装置中的______(填序号)。
【答案】CO2 CO 2 +C![]() 2CO 水蒸气进入D中在高温下能跟碳反应产生H 2 ,H 2 也能使CuO还原,不能证明CO具有还原性 D E ④
2CO 水蒸气进入D中在高温下能跟碳反应产生H 2 ,H 2 也能使CuO还原,不能证明CO具有还原性 D E ④
【解析】
利用一氧化碳还原氧化铜证明一氧化碳具有还原性。一氧化碳可以由二氧化碳和碳反应制得,所以需要首先制取二氧化碳。用稀盐酸和大理石制取二氧化碳,通过饱和碳酸氢钠溶液除去二氧化碳里的氯化氢,再通过浓硫酸除去水蒸气,通入装有碳的硬质玻璃管,得到的一氧化碳还原氧化铜,生成的二氧化碳能使石灰水变浑浊,多余的一氧化碳可以点燃除去。
根据上述
(1)装置A中生成的主要产物是CO2。
(2)装置D中发生反应的化学方程式是CO 2 +C![]() 2CO。
2CO。
(3)水蒸气进入D中在高温下能跟碳反应产生H 2 ,H 2 也能使CuO还原,不能证明CO具有还原性,所以必须用装置C吸收除去气体中水蒸气。
(4)二氧化碳通过碳,不能全部和碳反应,剩余的二氧化碳进入F中,也能使石灰水变浑浊。若要证明CO的还原性,就必须除去剩余的CO2,所以应在上图中装置D与E之间连接一个可以除去二氧化碳同时又不能带入水蒸气的装置,故选④。


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+4NO3(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
若用标准状况下4.48 LCH4还原NO2至N2,整个过程中转移的电子总数________(阿伏伽德罗常数用NA表示),放出的热量为_________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述,正确的是
A. 新制氯水中只含Cl2和H2O分子
B. 新制氯水可使蓝色石蕊试纸先变红后褪色
C. 光照氯水有气泡逸出,该气体是Cl2
D. 氯水放置数天后酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.往碘化亚铁中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl-
B.氯气与水反应:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
C.硝酸银溶液中加入过量氨水:Ag+ +NH3·H2O=AgOH↓+NH4+
D.Ca(HCO3)2溶液与少量NaOH溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 若反应X + Y = M是放热反应,该反应一定不用加热。
B. 需要加热方能发生的反应一定是吸热反应。
C. 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热。
D. CO2与CaO化合是放热反应,则CaCO3分解是吸热反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定体积的密闭容器中,加入4molA和2molB发生反应:2A(g)+B(g)![]() 3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
A. 4molA+2molB
B. 2molA+1molB+3molC+1molD
C. 3molC+1molD+1molB
D. 3molC+1molD
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)、 一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:
2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:

(1)降低温度,SO2的转化率_________,化学反应速度_________。(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是_________。
(3)反应进行至20 min时,曲线发生变化的原因是______________________(用文字表达)。10 min到15 min的曲线变化的原因可能是_________(填写编号)。
a. 加了催化剂 b. 缩小容器体积
c. 降低温度 d. 增加SO3的物质的量
(二) 在一个固定体积的密闭容器中,充入 2 mol A 和1 mol B,发生如下反应:2 A(g) + B(g)![]() 3C(g) + D(s), 反应达到平衡时 C的浓度为1.2 mol/L。
3C(g) + D(s), 反应达到平衡时 C的浓度为1.2 mol/L。
(1)若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为_____反应(填“吸热”或“放热”)反应。
(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是____________(用序号填空)
① 4 mol A + 2 mol B ② 3 mol C + 1 mol D + 1 mol B
③ 3 mol C + 2 mol D ④ 1.6 mol A + 0.8 mol B + 0.6 mol C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于配制980mL,0.1mol·![]() 的
的![]() 溶液的实验,下列说法正确的是
溶液的实验,下列说法正确的是
A. 需要称取![]() 固体的质量为16.0g
固体的质量为16.0g
B. 一定用到的玻璃仪器有 1000 mL 的容量瓶、烧杯、玻璃棒、漏斗、胶头滴管
C. 为加快![]() 固体的溶解,可适当加热,然后趁热将溶液转移到容量瓶中
固体的溶解,可适当加热,然后趁热将溶液转移到容量瓶中
D. 倒转摇匀后发现液面低于刻度线,若补加蒸馏水至刻度线会使所得溶液的浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型纽扣电池在现代生活中有广泛应用。有一种银锌电池如图所示,电池总反应为:
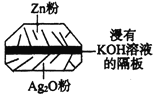
Zn + Ag2O + H2O = 2Ag + Zn(OH)2。下列叙述中正确的是( )
A.在使用过程中,电解质KOH不断被消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.正极反应式为:Ag2O+H2O+2e- = 2Ag+2OH-
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com