
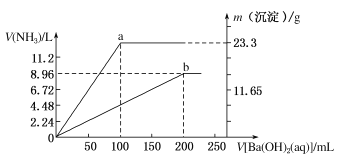
【题目】现有(NH4)2SO4和NH4NO3的混合溶液,向该混合溶液中逐滴加入Ba(OH)2溶液,并加热使之充分反应,直至Ba(OH)2溶液过量。加入Ba(OH)2溶液的体积与产生沉淀的质量和放出NH3的体积(标准状况下)的关系如下图,曲线a代表沉淀的质量变化,曲线b代表NH3的体积变化(假设NH3全部放出)。
(1)混合溶液中NH![]() 的物质的量为________mol。
的物质的量为________mol。
(2)混合溶液中NO![]() 的物质的量为________mol。
的物质的量为________mol。
(3)当加入Ba(OH)2溶液的体积在100~200mL范围内,发生反应的离子方程式为_________________。
【答案】 0.4 0.2 NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
【解析】本题考查化学计算,(1)整个过程中NH![]() +OH-
+OH-![]() NH3↑+H2O,当加入200mL氢氧化钡时,气体达到最大,即n(NH4+)=n(NH3)=8.96/22.4mol=0.4mol;(2)根据关系图,当加入100mL氢氧化钡溶液时,沉淀达到最大,即SO42-全部转化成BaSO4沉淀,即溶液中n(SO42-)=23.3/233mol=0.1mol,根据溶液显电中性,即n(NH4+)=2n(SO42-)+n(NO3-),则n(NO3-)=(0.4-2×0.1)mol=0.2mol;(3)根据(1)和(2)的分析,100mL到200mL之间发生的离子反应是NH
NH3↑+H2O,当加入200mL氢氧化钡时,气体达到最大,即n(NH4+)=n(NH3)=8.96/22.4mol=0.4mol;(2)根据关系图,当加入100mL氢氧化钡溶液时,沉淀达到最大,即SO42-全部转化成BaSO4沉淀,即溶液中n(SO42-)=23.3/233mol=0.1mol,根据溶液显电中性,即n(NH4+)=2n(SO42-)+n(NO3-),则n(NO3-)=(0.4-2×0.1)mol=0.2mol;(3)根据(1)和(2)的分析,100mL到200mL之间发生的离子反应是NH![]() +OH-
+OH-![]() NH3↑+H2O。
NH3↑+H2O。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I均为有机物,根据下列框图和已知条件回答问题: 
已知:A中有一个甲基,D都能使溴水褪色,F能发生银镜反应,I的结构简式为: 
请回答下列问题:
(1)A中含有的官能团:(文字叙述)
(2)属于取代反应的有:
(3)写出反应④的化学方程式
(4)写出A的结构简式
(5)E有多种同分异构体,其中一种既能发生银镜反应又能和NaOH溶液反应,请写出它的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项操作中,发生“先产生沉淀,然后沉淀又溶解”现象的是
①向石灰水中逐渐通入CO2直至过量
②向CaCl2溶波中逐渐通入CO2直至过量
③向Ba(OH)2溶液中逐滴加入稀硫酸直至过量
④向Fe(OH)3胶体中逐滴加入稀盐酸直至过量
A. ①② B. ①②③ C. ②④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化不能通过一步反应完成的是
A.Al2O3→Al(OH)3B.MgCl2→Mg(OH)2C.Na2CO3→NaClD.Fe(OH)2→Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)把一块纯净的锌片插入盛有稀硫酸的烧杯中,可观察到锌片逐渐溶解,并有气泡产生;平行地插入一块铜片(如图甲装置所示),可观察到铜片上________(填“有”或“没有”)气泡产生;若用导线把锌片和铜片连接起来(如图乙装置所示),可观察到铜片上________(填“有”或“没有”)气泡产生。
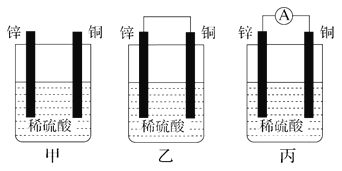
(2)用导线将电流表的两端与溶液中的锌片和铜片相连(如图丙装置所示),观察到电流表的指针发生了偏转,说明导线中有电流通过。锌片上的电极反应:______________;铜片上的电极反应:____________________________。
(3)乙、丙装置是将________能转化为________能的装置。
Ⅱ.断开1molH﹣H键,1molN﹣H键,1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,求:
(1)1molN2生成NH3需_____(填“吸收”或“放出”)能量_____ kJ
(2)1molH2生成NH3需_____(填“吸收”或“放出”)能量_____ kJ(不考虑可逆反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g)△H>0,0~15s内c(HI)由0.lmol/L降到0.07mol/L,则下列说法正确的是
H2(g)+I2(g)△H>0,0~15s内c(HI)由0.lmol/L降到0.07mol/L,则下列说法正确的是
A. 当HI、H2、I2浓度之比为2:1:1时,说明该反应达平衡
B. c(HI)由0.07mol/L降到0.05mol/L所需的反应时间小于10s
C. 升高温度正反应速率加快,逆反应速率减慢
D. 0~15s内用I2表示的平均反应速率为:v(I2)=0.001mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成都市近年来常常发生“毒奶粉”事件.劣质奶粉制造商为牟取暴利,大大降低了奶粉中蛋白质的含量,导致食用这种奶粉的众多婴幼儿严重营养不良乃至死亡.为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质.其原理是把蛋白质中的氮元素完全转化为氨气(化学式为NH3),再用稀硫酸吸收氨气,反应的化学方程式为:2NH3+H2SO4=(NH4)2 SO4现取该奶粉样品100g,用“盖尔达法”分解其中的蛋白质,产生的氨气用7.5g溶质质量分数为19.6%的稀硫酸恰好完全吸收. 计算并回答下列问题:
(1)产生氨气的质量是多少?(计算结果精确到0.01,下同)
(2)含氮元素的质量多少?
(3)该奶粉中氮的含量是否达到了国家规定的标准.(奶粉中蛋白质的含量国家标准为:每100g婴幼儿奶粉中含12g~25g.蛋白质含氮元素的质量分数为16%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为倡导“节能减排”和“低碳经济”,目前工业上有一种方法是用CO2来生产燃料乙醇。一定条件下发生反应:2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) ΔH<0。
CH3CH2OH(g)+3H2O(g) ΔH<0。
(1)在一定条件下,在20 L密闭容器中按物质的量比为1∶3充入CO2和H2,温度在450 K,n(H2)随时间变化如表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 6 | 5 | 5 |
在450 ℃、0~1 min,v(CH3CH2OH)=________;此温度下该反应的化学平衡常数为________(结果保留三位有效数字)。
(2)在5 MPa下测得平衡体系中各物质的体积分数随温度的变化曲线如图所示:

曲线乙表示的是 ________(填物质的化学式)的体积分数,图像中A点对应的体积分数b=________%(结果保留三位有效数字)。
(3)下列措施中能使化学平衡向正反应方向移动的是________。
A.升高温度
B.将CH3CH2OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l mol CO2和3 mol H2
(4)25 ℃、1.01×105Pa时,9.2 g液态乙醇完全燃烧,当恢复到原状态时,放出273.4 kJ的热量,写出表示乙醇燃烧的热化学方程式:________________________。
(5)以石墨为电极,氢氧化钠、乙醇、水、氧气为原料,可以制成乙醇的燃料电池,写出发生还原反应的电极反应式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明溶液中,下列各组中的离子一定能大量共存的是
A. K+、Fe2+、NO3-、H+ B. Na+、Ca2+、Cl-、NO3-
C. Na+、H+、Cl-、CO32- D. Na+、Cu2+、OH-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com