
【题目】漂白粉在空气中容易变质的原因是( )
A. CaCl2易吸收空气中的水分
B. Ca(ClO)2易与盐酸反应
C. Ca(ClO)2见光易分解
D. Ca(ClO)2易与空气中的CO2和水作用
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)2SO2(g)+O2(g) △ v 2 O 5 2SO3(g);△H=﹣196.6KJ/mol,是制备硫酸的重要反应.下列关于该反应的叙述正确的是 . (填字母)
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1 , c2 , 则时间间隔t1~t2内,SO3(g)生成的平均速率为u= c 2 c 1 t 2 t 1
E.使用催化剂V2O5能提高SO2的转化率
F.使用催化剂V2O5会改变该反应的△H
(2)判断该反应达到平衡状态的标志是 .(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.在体积不变的容器中,气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.在体积不变的容器中混合气体,的密度保持不变
f.SO2、O2、SO3的浓度比保持不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式错误的是( )
A.用硅酸钠与盐酸反应制备硅胶:SiO ![]() +2H+═H2SiO3(胶体)
+2H+═H2SiO3(胶体)
B.FeI2溶液中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl﹣
C.少量NaHSO4 溶液与Ba(OH)2 溶液反应:H++OH﹣+SO ![]() +Ba2+═H2O+BaSO4↓
+Ba2+═H2O+BaSO4↓
D.FeCl3溶液中通入SO2 , 溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO ![]() +4H+
+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )
A.FeCl3溶液、溴水
B.碳酸钠溶液、溴水
C.酸性高锰酸钾溶液、溴水
D.酸性高锰酸钾溶液、FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质是按单质、氧化物、混合物的顺序排列的是( )
A. 氧气、水、空气B. 氮气、氯酸钾、乙醇汽油
C. 可燃冰、干冰、冰水混合物D. 石墨、氯化钠、石油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体5.6L(标准状况),同时溶液质量增加9.3g,下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25mol
B.原溶液中的HNO3浓度是2.0mol/L
C.反应后的溶液中还可以溶解9.6g铜
D.反应后的溶液中c(Fe2+):c(Fe3+)=1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体5.6L(标准状况),同时溶液质量增加9.3g,下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25mol
B.原溶液中的HNO3浓度是2.0mol/L
C.反应后的溶液中还可以溶解9.6g铜
D.反应后的溶液中c(Fe2+):c(Fe3+)=1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下面的装置中,A是实验室制备Cl2的发生装置,圆底烧瓶中盛放的是二氧化锰,C、D为气体净化装置;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶:烧杯G为尾气吸收装置。试回答:
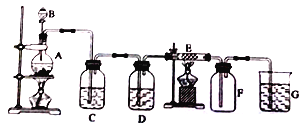
(1)C装置中试剂为______。
(2)E中的现象为______。
(3)写出在A、G中发生反应的离子方程式:A: ___________。G: ________________。
(4)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:2 KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①考试用“单线桥”标出电子转移的方向和数目: __________。
②该反应中被氧化和未被氧化的HCl的物质的量之比是________,如果将20mL、12mol/L的浓盐酸与足量KMnO4充分反应,实际能收集到氯气在标准状况下的体积为_______。
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com