
【题目】实验室有一包白色固体,可能含有NaCl、NaHCO3和NH4Cl中的一种或多种。下列根据实验事实得出的结论正确的是
A. 取一定量固体,在空气中充分加热,有白色物质残留,则原白色固体中含NaCl
B. 取一定量固体,加水溶解,向溶液中加入少量NaOH溶液,再滴加AgNO3溶液,有白色沉淀生成,则该白色沉淀是AgCl
C. 取一定量固体,加水溶解,向溶液中滴加足量NaOH溶液,加热,将得到气体直接通入足量浓硫酸,浓硫酸增重3.40 g,则原白色固体中含NH4Cl 10.7 g
D. 取一定量固体,加水溶解,向溶液中滴加足量Ba(OH)2溶液,有白色沉淀生成,将沉淀过滤、洗涤、干燥,得到沉淀质量为3.94 g,则原白色固体中含NaHCO3 1.68 g
【答案】D
【解析】
A. 取一定量固体,在空气中充分加热,NaHCO3受热分解生成碳酸钠、二氧化碳和水,NH4Cl受热分解生成氯化氢和氨气,故若有白色物质残留,则原白色固体中可能含NaCl、NaHCO3或两者均有,选项A错误;
B. 取一定量固体,加水溶解,向溶液中加入少量NaOH溶液,若为NaHCO3,则与氢氧化钠反应生成碳酸钠,再滴加AgNO3溶液,有白色沉淀生成,则该白色沉淀可能是碳酸银,选项B错误;
C. 取一定量固体,加水溶解,向溶液中滴加足量NaOH溶液,加热,将得到气体直接通入足量浓硫酸,浓硫酸增重3.40 g,氨气及水均能被浓硫酸吸收,故无法计算氨气的物质的量,则原白色固体中含NH4Cl可能小于或等于10.7 g,选项C错误;
D. 取一定量固体,加水溶解,向溶液中滴加足量Ba(OH)2溶液,有白色沉淀生成,将沉淀过滤、洗涤、干燥,得到沉淀质量为3.94 g,即n(BaCO3)=![]() ,根据碳原子守恒,则原白色固体中含NaHCO3 0.02mol×84g/mol=1.68 g,选项D正确。
,根据碳原子守恒,则原白色固体中含NaHCO3 0.02mol×84g/mol=1.68 g,选项D正确。
答案选D。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】A~G各物质间的关系如下图所示,其中B、D为气体单质。则下列说法错误的是

A.已知C的浓溶液在催化剂存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO2强
B.反应②的离子方程式为![]()
C.新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止Fe2+被空气氧化成Fe3+,后者可抑制Fe2+的水解
D.若反应①在常温下进行,则1molA在反应中能转移1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,实验操作步骤有:
A.在天平上称取所需硫酸铜固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并恢复至室温
B.把所得的溶液小心地转移到容量瓶中
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡
E.将容量瓶瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)___________________。
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒、药匙,还缺少的仪器是______、___________。
(3)实验过程中需用天平量取___________g无水硫酸铜。
(4)下列情况会使所配溶液浓度偏高的是(填序号)_________________。
a.某同学观察液面的情况如图所示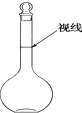
b.没进行上述的操作步骤D
c.加蒸馏水时,不慎超过了刻度线
d.砝码上沾有杂质
e.容量瓶使用前内壁沾有水珠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______,直到因加入一滴盐酸后,溶液由________色变为________色,并________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
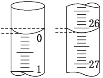
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为_______mL,终点读数为_______mL,所用盐酸溶液的体积为_______mL。
(4)某学生根据3次实验分别记录有关数据如下表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 盐酸的体积/mL | ||
滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在汽车尾气处理装置中发生如下反应:4CO+2NO2![]() 4CO2+N2。下列有关该反应的说法中正确的是
4CO2+N2。下列有关该反应的说法中正确的是
A. NO2是还原剂B. CO被氧化
C. NO2发生氧化反应D. CO得到电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。高铁酸钾为暗红色粉末状晶体,干燥的晶体80℃以下十分稳定,它极易溶于水,难溶于异丙醇。实验室模拟生产工艺流程如图:
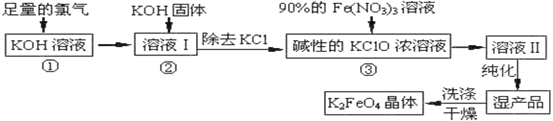
已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③K2FeO4在水溶液中易水解:4FeO42-+10H2O![]() 4Fe(OH)3(胶体)+8OH-+3O2↑
4Fe(OH)3(胶体)+8OH-+3O2↑
回答的下列问题:
实验室可以利用如图装置完成流程①和②
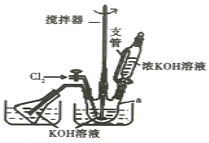
(1)恒压滴液漏斗支管的作用是_____,两水槽中的水为____(填“热水”或“冷水”)。
(2)反应一段时间后,停止通氯气,再往仪器a中加入浓KOH溶液的目的是______;判断浓KOH溶液已过量的实验依据是___。
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为____。
(4)用重结晶法提纯粗产品:将粗产品先用KOH稀溶液溶解,再加入饱和KOH溶液,冷却结晶,过滤,用少量异丙醇洗涤,最后低温真空干燥。
①粗产品用KOH溶解的目的是_____。
②如何判断K2FeO4晶体已经洗涤干净____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)三月万物复苏,很多人会外出踏青旅游。
①自驾游出行方便。制造汽车轮胎的主要材料是____(填字母)。
a.铝合金 b.橡胶 c.玻璃
②高速列车出行快捷。建设铁路需要大量水泥。工业上生产水泥的主要原料是石灰石和____(填字母)。
a.黏土 b.纯碱 c.石英
③轮船出行舒适。为防止轮船钢板被腐蚀,可在钢板上镶嵌____(填字母)。
a.铜块 b.锡块 c.锌块
(2)旅游期间,在娱乐、购物、旅游时要讲究文明、保护环境。
①用过的聚乙烯塑料食品袋要投入贴有可回收物标志的垃圾箱中。聚乙烯的结构简式是____。
②不法商贩会用由铜锌合金打造的假金首饰欺骗消费者。请写出检验金首饰真假的化学方法和结论____。
③不能携带烟花爆竹乘坐公共交通工具。制作烟花爆竹的黑火药是用木炭、硝酸钾、硫磺配制,黑火药爆炸时会生成氮气、硫化钾和二氧化碳。写出该反应的化学方程式____。
(3)在外出行要注意饮食健康。
①面包、牛奶是常见的食物之一,面包对人体的主要作用是____。牛奶中的蛋白质在人体内水解可生成____。
②为保证营养均衡,应摄入适量蔬菜。蔬菜中的膳食纤维对人体的作用是____。
③橙汁是常用饮品。某品牌橙汁中含有维生素C、白砂糖、精制盐、柠檬黄和苯甲酸钠等成分,这几种物质中属于着色剂的是____。缺少维生素C可能会引发的疾病是____。
④饮食不当会引起胃痛。胃舒平[主要成分是Al(OH)3]可治疗胃酸过多,写出Al(OH)3与胃酸反应的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员以Zn和尖晶石型锰酸锌(ZnMn2O4)为电极材料,研制出一种水系锌离子电池。该电池的总反应方程式:xZn + Zn1xMn2O4![]() ZnMn2O4(0 < x < 1)。下列说法正确的是
ZnMn2O4(0 < x < 1)。下列说法正确的是
A. 充电时,Zn2+向ZnMn2O4电极迁移
B. 充电时,阳极反应:ZnMn2O4 2xe—=Zn1-xMn2O4+xZn2+
C. 放电时,每转移1mol e-,ZnMn2O4电极质量增加65g
D. 充放电过程中,只有Zn元素的化合价发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为______________________________________。
(2)②在水中的电离方程式为______________________________。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式_________________;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式________。
(4)写出下列反应的离子方程式:
向Ba(OH)2溶液中逐滴加入硫酸溶液___________________________。
向Ba(OH)2溶液中通入过量的CO2_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com