
【题目】在密闭容器中,合成氨的反应N2+3H2![]() 2NH3,现将2mol N2和2mol H2通入该容器中反应,20s后生成0.8 mol的NH3,则H2的转换率是多少( )
2NH3,现将2mol N2和2mol H2通入该容器中反应,20s后生成0.8 mol的NH3,则H2的转换率是多少( )
A. 70% B. 60% C. 50% D. 40%
科目:高中化学 来源: 题型:
【题目】(14分)硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红等产品的流程如下图所示

回答下列问题:
(1)若焙烧时还原剂碳燃烧产生的气体能将铁的多种氧化物还原成铁单质,则该气体与Fe2O3反应的化学方程式为 。
(2)酸浸时间一般不超过20 min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因用离子方程式表示为 。
(3)加碳酸氢铵合成时反应温度一般需控制在35℃以下,其目的是 。
(4)若产品Ⅱ的主要成分是K2SO4,则试剂X为 ,反应的离子方程式为 。
(5)空气中煅烧FeCO3生成产品Ⅰ的化学反应方程式为 。
(6)检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液, 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃和1.01×105Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.76 kJ·mol-1,自发进行的原因是
A.吸热反应B.放热反应C.熵减少的反应D.熵增大效应大于热效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一种金属离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙[Ca(NO3)Cl]。则下列化合物中属于混盐的是( )
A.CaOCl2B.(NH4)2Fe(SO4)2C.BiONO3D.K3[Fe(CN)6]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过你的观察和推理,判断下列实验室中对于少量Na的保存方法正确的是 ( )
A. 保存在水中 B. 密封,保存在广口瓶中
C. 用铝箔包裹,密封在广口瓶中 D. 密封,保存在煤油中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废液中Cr2O7可通过下列反应转化成铬黄(PbCrO4):
Cr2O![]() (aq)+2Pb2+(aq)+H2O(l)
(aq)+2Pb2+(aq)+H2O(l) ![]() 2PbCrO4(s)+2H+(aq) ΔH<0
2PbCrO4(s)+2H+(aq) ΔH<0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是 ( )。
A. 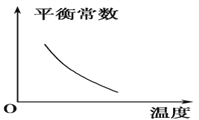 B.
B. 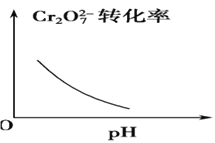
C.  D.
D. 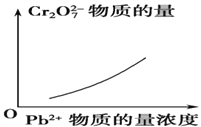
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铵(NH4H)与氯化铵的结构相似,电子式为 ![]() ,又知NH4H与水反应有H2生成,下列叙述中不正确的是( )
,又知NH4H与水反应有H2生成,下列叙述中不正确的是( )
①NH4H是离子化合物,含有离子键和共价键
②NH4H溶于水所形成的溶液显酸性
③NH4H与水反应时,NH4H是氧化剂
④NH4H固体投入少量的水中,有两种气体生成.
A.①②
B.②③
C.①②③
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A,B,C,D,E,F六种常见短周期元素,已知:
①元素的原子序数按A、B、C、D、E、F依次增大,原子半径按E、F、B、C、D、A顺序依次减小;
②A、E同主族,A是所有元素中原子半径最小的元素;B能形成天然存在的最硬的单质甲和最软的矿物乙;D元素原子最外层电子数是次外层电子数的3倍;
③C、E、F三者的最高价氧化物的水化物依次为丙、丁、戊,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含D元素;
④C、F两种元素原子最外层电子数之和等于A、D、E三种元素原子最外层电子数之和.
(1)F在元素周期表中的位置为 , A、D两元素原子形成1:1型化合物的电子式为 .
(2)B的某种原子常用于考古时测定一些文物的年代,该原子符号为 .
(3)写出丁+戊在溶液中反应的离子方程 .
(4)物质甲和乙间的相互转化(填“是、不是”)氧化还原反应.
(5)C的最高价氧化物对应的水化物和E的简单氢化物反应可生成一种盐和一种气体,写出该反应的化学方程式 . 该反应中氧化产物与还原产物的质量之比为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com