
下列叙述正确的是
A.在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应吸热
B.同温同压下,4Al(s)+3O2(g)===2Al2O3(s)在常温和点燃条件下的ΔH不同
C.稀溶液中:H+(aq)+OH—(aq) ===H2O(l);ΔH=—53.7KJ/mol ,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于53.7KJ
D.由C(石墨)=== C(金刚石) △H= +1.90 kJ·mol-1 可知,金刚石比石墨稳定
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见下图)。下列说法正确的是( )

A.CO、SO2、SO3均是酸性氧化物 B.除去与水反应,图示转化反应均为氧化还原反应
C.工业上利用Cl2和澄清石灰水反应来制取漂白粉
D.用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在生产和生活中有着广泛的应用。
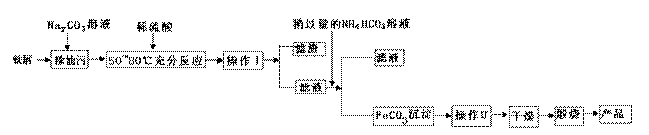
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是____ 、____。
②写出在空气中煅烧FeCO3的化学方程式 ;
③.煅烧如果不充分,产品中将有Fe2+ 存在,试设计实验检验产品中有无Fe2+ 。
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。
a. 称取2.850g绿矾(FeSO4·7H2O)产品,配成250mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①写出酸性KMnO4溶液与FeSO4 溶液反应的离子方程式
②计算上述样品中FeSO4·7H2O的质量分数为 [ 已知M(FeSO4·7H2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为
④下列操作会导致样品中FeSO4·7H2O的质量分数的测定结果偏高的有_____________。
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定结束时仰视刻度线读数
d.量取待测液的滴定管没有润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
燃烧热是指一定条件下1 mol可燃物完全燃烧生成稳定的氧化物时放出的热量。已知热化学方程式:①CO(g)+1/2 O2(g)====CO2(g)ΔH = -283.0 kJ·mol-1
②H2(g)+ 1/2O2(g)====H2O(g)ΔH = -241.8 kJ·mol-1
则下列说法正确的是( )
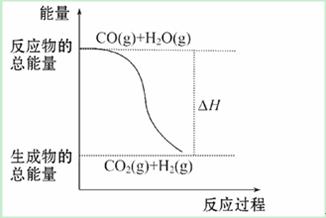
A. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)==== CO2(g)+H2(g)ΔH = -41.2 kJ·mol-1
B. H2的燃烧热为241.8 kJ·mol-1
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g)+1/2O2(g)==== H2O(l)ΔH > -241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
A. A﹥B﹥E﹥D B. A﹥B﹥D﹥E C. D﹥E﹥A﹥B D. D﹥A﹥B﹥E
查看答案和解析>>
科目:高中化学 来源: 题型:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液c ;
A、B是两块电极板,通过导线与直流电相连。请回答以下问题:
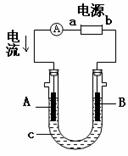 (1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
① B是 极(填“阴”或“阳”), B极逸出
(填:黄绿或无色)气体,同时B极附近溶液呈 色。
② 电解池中A极上的电极反应式为 。
B极上的电极反应式为 。
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
① A电极的材料是 ,电极反应式是 。
② B电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
③下列说法正确的是________。
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为12.8 g ,则阳极上产生的气体在标准状况下的体积为 L 。
(4)利用反应2Cu+O2+2H2SO4===2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用 ,阳极材料是用 ,阴极电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,CO和水蒸气各1mol放在密闭容器中反应:
CO(g) + H2O(g)  CO2(g) + H2(g)达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为 ( )
CO2(g) + H2(g)达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为 ( )
A.等于0.6mol B.等于1mol C.大于0.6mol小于1mol D.大于1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com