
【题目】A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子的2p能级有3个电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。回答下列问题:
(1)写出基态E+的价电子排布式:_________。基态A原子的第一电离能比B的大,其原因是__________。
(2)A5+由美国空军研究实验室推进科学与先进概念部Karl .O. Christed 于1999年成功合成,其结构呈‘V'形且该离子中各原子均达到8电子稳定结构,则A5+的结构式为________。
(3)B3分子的空间构型为______,其中B原子的杂化类型是______,与B3分子互为等电子体的微粒有_________(写一种离子)。
(4)向E的硫酸盐溶液中通入A的气态氢化物至过量,产生蓝色沉淀,随后沉淀溶解得到深蓝色溶液,向溶液中加入适量乙醇,析出蓝色晶体。加入乙醇的目的___________。 写出该配合物中配离子的结构简式__________。
(5)由长周期元素组成的镧镍合金、铜钙合金有相同类型的晶体结构XYn,它们有很强的储氢能力,其中铜钙合金的晶体的部分结构如图所示。
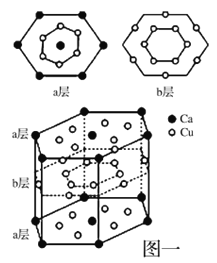
己知镧镍合金(LaNin)晶体中的重复结构单元如图一所示,该结构单元的体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶体空隙,体积不变),则LaNin中n=___ (填数值);氢在合金中的密度为_______g/L。
【答案】 3d10 N原子价电子排布式为2S22P3,O原子为2s22p4,N的2p轨道达半满,更为稳定 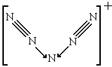 v形 SP2 NO2- 降低[Cu(NH3)4]SO4·H2O的溶解度
v形 SP2 NO2- 降低[Cu(NH3)4]SO4·H2O的溶解度 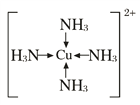 n=5 密度是250g/L
n=5 密度是250g/L
【解析】B、C、D、E五种原子序数依次增大的元素(原子序数均小于30),A的基态原子2p能级有3个单电子,原子核外电子排布为1s22s22p3,则A是N元素;C的基态原子2p能级有1个单电子,且C的原子序数大于A,其原子核外电子排布为1s22s22p5,所以C是F元素,结合原子序数可推知B是O元素;E原子核外有成单电子,其次外层有3个能级且均排满电子,且原子序数小于30,则E处于第四周期,其基态原子的价电子排布式3d104s1,则E是Cu元素;D与E同周期,价电子数为2,则D是Ca元素;
(1)Cu的核电荷数为29,基态Cu原子的电子排布式是1s22s22p63s23p63d104s1,则价电子排布式为3d104s1。基态N原子的核外电子排布为1s22s22p3,p轨道为半充满结构,较稳定,故其第I电离能比O的大;
(2). N5+共有24个价电子,其结构呈‘V'形且该离子中各原子均达到8电子稳定结构,则N5+的结构式为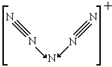
(3)O3中O原子的杂化类型是SP2,所以空间构型为v形,与O3分子互为等电子体的微粒有应具有3个原子和18个价电子,符合条件且为离子的可以是 NO2-。
(4)向CuSO4的水溶液中逐滴加入氨水,离子方程式为:Cu2++2NH3H2O=Cu(OH)2↓+2H2O,至过量,观察到溶液由天蓝色最终变为深蓝色,生成[Cu(NH3)4]2+,反应的离子方程式为:Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++2OH-+4H2O;
①该蓝色晶体的化学式为[Cu(NH3)4]SO4·H2O,加入乙醇的目的是向深蓝色透明溶液加入乙醇,由于[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,所以会析出深蓝色的晶体:Cu(NH3)4SO4H2O,则加入乙醇的作用是降低了[Cu(NH3)4]SO4H2O的溶解度;
②[Cu(NH3)4]2+的结构式为![]() ;
;
(5)铜、钙合金中,N(Cu)=12![]() +6
+6![]() +6=15。N(Ca)=12×
+6=15。N(Ca)=12×![]() +2×
+2×![]() =3,
=3, ![]() =
=![]() =
=![]() ,所以n=5;因为合金的化学式为LaNinH4.5而一个晶胞中实际拥有三个La原子、5个Ni原子,所以实际含有氢原子4.5×3=13.5。ρ·9.0×10-23cm3·NA=M,其中氢在合金中的密度为
,所以n=5;因为合金的化学式为LaNinH4.5而一个晶胞中实际拥有三个La原子、5个Ni原子,所以实际含有氢原子4.5×3=13.5。ρ·9.0×10-23cm3·NA=M,其中氢在合金中的密度为![]() 0.25 g·cm-3=250g/L。
0.25 g·cm-3=250g/L。


科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑
B. 钠与水的反应:Na+2H2O=Na++2OH-+H2↑
C. 铜片跟稀硝酸的反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O
D. 将氯气通入氯化亚铁溶液:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
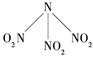
A. 分子中N、O间形成的共价键是非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 15.2g该物质含有的原子数为6.02×1024
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
HCN | S8 | SF6 | B12结构单元 | |
结构模型 示意图 |
|
|
|
|
备注 | — | 易溶于CS2 | — | 熔点1 873 K |
A. HCN的结构式为H—C≡N,分子中含有2个σ键和2个π键
B. 固态硫S8属于原子晶体
C. SF6是由极性键构成的非极性分子
D. 单质硼属原子晶体,结构单元中含有30个B—B键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究证明高铁酸钠(Na2FeO4) 是一种“绿色环保高效”消毒剂, 比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.用氯气和氢氧化钠溶液反应制备NaClO溶液
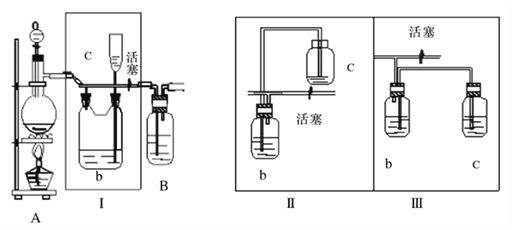
(1)A是氯气发生装置,写出实验室用此装置制取氯气的离子方程式__________。
(2)I装置的作用是__________ 。
(3)用图示的II或III代替I是否可行? __________。简要说明理由__________ 。
(4)将产生的氯气通入D装置中制NaClO溶液
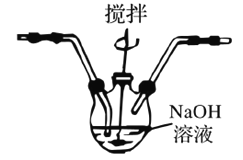
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
II.制备Na2FeO4
(1)将Fe(NO3)3溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是______。过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是__________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置探究铁粉在高温下与水蒸气反应的实验。
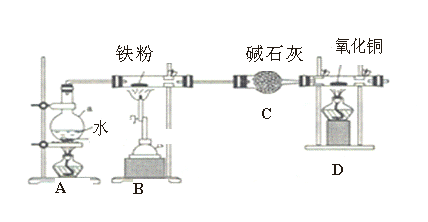
(1)A装置加热作用是___________________________;
(2)B中反应的化学方程式:_________________________________________,标准状况下,若该反应生成22.4L气体,则反应转移的电子数为______________。
(3)装置D中的现象是___________________,写出D中反应方程式:_________________。
(4)A 、B两处酒精灯点燃顺序:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
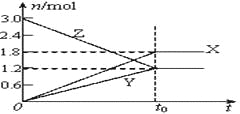
【题目】在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )
A. 该反应的化学方程式为:3X+2Y![]() 2Z
2Z
B. 若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0
C. 若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
D. 若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z发生的反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线。下列说法正确的是( )
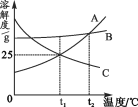
A. t1℃时,A的饱和溶液中溶质质量分数为25%
B. t2℃时,A、B、C三种物质的溶解度大小关系为A=B>C
C. 将t1℃时A、C的饱和溶液升温到t2℃时,A、C两溶液都会变成不饱和溶液
D. B中含有少量A,要提纯B可采用冷却热饱和溶液、趁热过滤的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:
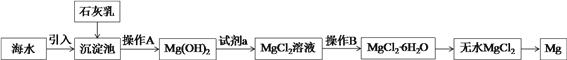
操作A是____________,下列仪器中操作B必须使用的有__________(填字母符号)。
A、锥形瓶 B、玻璃棒 C、表面皿 D、蒸发皿 E、坩埚
Ⅱ、乙醇镁[(CH3CH2O)2Mg] 为白色固体,难溶于乙醚和烃类,略溶于乙醇,在空气中会水解,常用作烯烃聚合催化剂载体和制备精密陶瓷的原料。某小组同学用镁粉(受潮会发生自燃、自爆)与乙醇在实验室中制备乙醇镁:
(1)干燥管中盛装的试剂为_____________,其作用为__________________________。
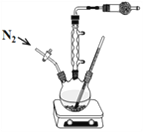
(2)下列操作的合理顺序为:______________。
a、将干燥的氮气通入装置,连续操作数次;
b、称取镁粉,量取无水乙醇加入反应器内;
c、加热回流,控制温度在80℃,反应1小时;
d、开启冷凝水和磁力搅拌器。
(3)将温度控制在80℃的原因是________________,写出生成乙醇镁的化学方程式____________________________。
(4)请你设计实验证明有乙醇镁生成(简述实验的方法):_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com