
【题目】Ⅰ.25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11` | 3.0×10-8 |
请回答下列问题:
(1)写出碳酸的第一级电离方程式:________。
(2)物质的量浓度相同的三种溶液:a.CH3COONa b.NaHCO3 c.NaClO
三种溶液的pH由小到大排列的顺序是___<___< ___(用编号填写)
(3)写出向NaClO溶液中通入少量CO2的化学方程式________。
Ⅱ.(4)碳酸钠溶液呈碱性的原因是:______。(写出离子方程式)。0.01mol/L Na2CO3溶液的pH____0.1mol/LNa2CO3溶液的pH。(填“>”或“<”或“==”)
(5)浓度均为0.1mol/L的①CH3COONa溶液②NH4Cl溶液③稀HCl④Na2SO4溶液按pH由大到小的排列顺序为____
(6)打开无水FeCl3的试剂瓶,常冒出许多“白烟”,发生反应的化学方程式为________
【答案】H2CO3![]() HCO3-+H+ a b c NaClO+CO2+H2O=HClO+NaHCO3 CO32-+H2O
HCO3-+H+ a b c NaClO+CO2+H2O=HClO+NaHCO3 CO32-+H2O![]() HCO3-+OH- < ①④②③ FeCl3+3H2O
HCO3-+OH- < ①④②③ FeCl3+3H2O![]() Fe(OH)3+3HCl
Fe(OH)3+3HCl
【解析】
Ⅰ.(1)碳酸是二元弱酸,分步电离;
(2)强碱弱酸盐溶液中,酸根离子对应酸的酸性越强,该离子的水解程度越小,溶液的pH越小;
(3)弱酸的电离平衡常数越大,则酸越强,由于电离平衡常数CH3COOH>H2CO3>HCO3->HClO,则酸性强弱顺序为CH3COOH>H2CO3>HCO3->HClO;
Ⅱ.(4)碳酸钠溶液中存在CO32-的二级水解,导致溶液显碱性;在强碱弱酸盐溶液中,加水促进弱酸根离子的水解;
(5)①CH3COONa是强碱弱酸盐,溶液显弱碱性;②NH4Cl是强酸弱碱盐,溶液显弱酸性;③稀HCl是强酸,溶液显酸性;④Na2SO4是强酸强碱盐,溶液显中性;
(6))FeCl3在溶液中遇水水解,生成氢氧化铁和HCl;
Ⅰ.(1)碳酸是二元弱酸,其第一级电离方程式H2CO3![]() HCO3-+H+;
HCO3-+H+;
(2)三种溶液的溶质都是强碱弱酸盐,水解程度大小为:CO32->ClO->HCO3->CH3COO-,水解均显碱性,水解程度越大,碱性越强,所以碱性顺序是: NaClO>NaHCO3>CH3COONa,即pH由小到大的排列顺序为:CH3COONa<NaHCO3<NaClO,即:pH由大到小的顺序为:abc;
(3)弱酸的电离平衡常数越大,则酸越强,由于电离平衡常数CH3COOH>H2CO3>HCO3->HClO,则酸性强弱顺序为CH3COOH>H2CO3>HCO3->HClO,根据强酸制弱酸的原则,向NaClO溶液中通入少量CO2发生反应的化学方程式为NaClO+CO2+H2O=HClO+NaHCO3;
Ⅱ.(4)碳酸钠溶液中存在CO32-的二级水解,导致溶液显碱性,其水解反应的离子方程式为CO32-+H2O![]() HCO3-+OH-;在强碱弱酸盐溶液中,加水促进弱酸根离子的水解,但溶液的碱性变弱,则0.01mol/L Na2CO3溶液的pH<0.1mol/LNa2CO3溶液的pH;
HCO3-+OH-;在强碱弱酸盐溶液中,加水促进弱酸根离子的水解,但溶液的碱性变弱,则0.01mol/L Na2CO3溶液的pH<0.1mol/LNa2CO3溶液的pH;
(5)浓度均为0.1mol/L的,①CH3COONa是强碱弱酸盐,溶液显弱碱性;②NH4Cl是强酸弱碱盐,溶液显弱酸性;③稀HCl是强酸,溶液显酸性,溶液中H+浓度为0.1mol/L;④Na2SO4是强酸强碱盐,溶液显中性,则按pH由大到小的排列顺序为①④②③;
(6)打开无水FeCl3的试剂瓶,常冒出许多“白烟”, 是FeCl3在溶液中水解生成氢氧化铁和HCl的缘故,发生反应的化学方程式为FeCl3+3H2O![]() Fe(OH)3+3HCl。
Fe(OH)3+3HCl。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】甲班学生做完实验室制备氧气和还原金属氧化物的实验后,剩余物质倒入同一废液缸里。乙班课外兴趣小组同学进行了如图所示的探究。请回答:
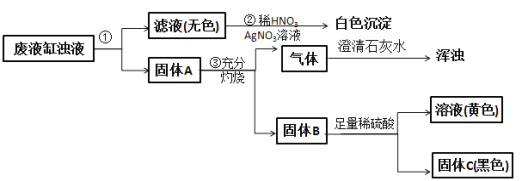
(1)步骤①的操作名称是___________,所用到的玻璃仪器有漏斗、玻璃棒和___________。
(2)由步骤②实验现象推知,甲班同学制取氧气所用的固体反应物是___________(写化学式)。
(3)由步骤④所得溶液加入氢氧化钠可得红棕色沉淀,该反应的化学方程式为______________________。
(4)由步骤③产生的气体判断固体A中一定含有___________(写名称);综合步骤③④现象推理,固体A中还可能含有的物质是______________________(写至少两种物质的化学式)。
(5)根据上述实验和分析判断固体C是___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)乙炔的电子式__________________。
(2)![]() 分子式:_________________。
分子式:_________________。
(3)![]() 其苯环上的一氯代物有______种
其苯环上的一氯代物有______种
(4)结构简式为![]() 此烃名称为___________________。
此烃名称为___________________。
(5) 4,4,5﹣三甲基﹣2﹣己炔(写出结构简式) ____________。
(6)结构简式为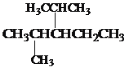 的烃可命名为:____________________。
的烃可命名为:____________________。
(7)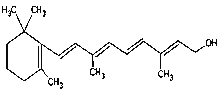 1mol该物质消耗_______molH2.
1mol该物质消耗_______molH2.
(8)鉴别苯,碘化钾溶液,硝酸银溶液,己烯,四氯化碳时,只能用一种试剂,该试剂是_________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一未知浓度的盐酸,某同学在实验室中进行实验测定盐酸的浓度。请完成下列填空:
配制100mL0.10molL-1NaOH标准溶液。需用托盘天平称量___g的氢氧化钠固体。
取20.00mL待测盐酸放入锥形瓶中,并滴加 2~3滴酚酞作指示剂,用配制的标准 NaOH溶液进行滴定。重复上述滴定操作 2~3次,记录数据如下:
滴定次数 | 待测盐酸的体积/mL | 0.10 mol/L NaOH 溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 20.00 | 2.00 | 28.15 |
第二次 | 20.00 | 1.50 | 29.50 |
第三次 | 20.00 | 0.20 | 26.55 |
①该实验滴定达到终点的标志是_________
②根据上述数据,可计算出该盐酸的浓度约为______。(保留两位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。(双选)
A 滴定终点读数时俯视读数 B 酸式滴定管使用前,水洗后未用待测盐酸润洗
C 锥形瓶水洗后未干燥 D 碱式滴定管尖嘴部分有气泡,滴定后消失
E 称量NaOH 固体时,混入少量KOH杂质
④现用以上实验配制的0.10molL-1NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完全时,下列叙述中正确的是_____
A 溶液呈中性,可选用甲基橙或酚酞作指示剂
B 溶液呈中性,只能选用石蕊作指示剂
C 溶液呈碱性,可选用甲基橙或酚酞作指示剂
D 溶液呈碱性,只能选用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气是重要燃料和化工原料,可用水蒸气通过炽热的碳层制得:C (s) +H2O(g)![]() CO(g) +H2(g) △H=+131.3kJmol-1
CO(g) +H2(g) △H=+131.3kJmol-1
(1)该反应的化学平衡常数表达式K=___,若某温度下,K值的大小为0.5,此时向体积为1L的密闭容器中加入1mol H2O(g)和足量C(s),H2O(g)的平衡转化率为___
(2)对于该反应,一定可以提高平衡体系中H2的百分含量,又能加快化学反应速率的措施是____。
a.升高温度 b.增大水蒸气的浓度 c.加入催化剂 d.降低压强
(3)上述反应达到平衡后,移走体系中部分C(s),平衡_____,将产生的CO全部移走,平衡___(以上两空选填“向左移”、“向右移”、“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜, 主要作用是在反应过程中只让Li+通过。结构如图所示。
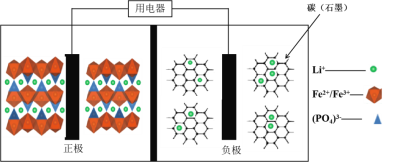
原理如下:(1-x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC。
LiFePO4+nC。
下列说法不正确的是( )
A. 放电时,正极电极反应式:xFePO4+xLi++xe-===xLiFePO4
B. 放电时,电子由负极经导线、用电器、导线到正极
C. 充电时,阴极电极反应式:xLi++xe-+nC===LixCn
D. 充电时,Li+向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能表示H2(g)+ I2(g)![]() 2HI(g)已经达到平衡状态的标志是( )
2HI(g)已经达到平衡状态的标志是( )
①c(H2)=c(I2)=c(HI)时
②c(H2):c(I2):c(HI)=1:1:2时
③c(H2)、c(I2)、c(HI)不再随时间而改变
④单位时间内生成nmolH2的同时生成2nmolHI
⑤单位时间内生成nmolH2的同时生成nmolI2
⑥反应速v(H2)=v(I2)=1/2v(HI)
⑦一个H-H键断裂的同时有两个H-I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
条件一定,混合气体的平均相对分子质量不再变化
A.③④⑦⑨⑩B.③④⑦⑨C.②③④⑦⑨D.②③④⑥⑦⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解方程式的书写不正确的是( )
A.NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
B.S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C.CH3COONa+H2O![]() CH3COOH+NaOH
CH3COOH+NaOH
D.MgCO3 + H2O![]() Mg(OH)2 + CO2
Mg(OH)2 + CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学课上围绕浓硫酸的化学性质进行如下实验探究,将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。请回答下列问题:
(1)生成的这种黑色物质(单质)是(填化学式)________。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,这种刺激性气味气体为(填化学式)___,反应的化学方程式为________。
(3)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母) _______。
A 酸性 B 吸水性 C 脱水性 D 强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,探究SO2与品红作用的可逆性,请写出实验操作及现象______。;将(2)中产生的有刺激性气味的气体通入氯水中,发生反应的化学方程式为_______。
(5)工厂煤燃烧产生的烟气若直接排放到空气中,引发的主要环境问题有_____。
A 温室效应 B 酸雨 C 粉尘污染 D 水体富营养化
工业上为实现燃煤脱硫,常通过煅烧石灰石得到生石灰,以生石灰为脱硫剂,与烟气中SO2反应从而将硫固定,其产物可作建筑材料。写出其中将硫固定的化学方程式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com