
����Ŀ���������ȣ�ClO2�������ڴ��������ˮ��ijѧϰС����ʵ������̽��ClO2��Na2S�ķ�Ӧ��
��֪���� ClO2�Ǽ�������ˮ�Ļ���ɫ���壬�ж����е�Ϊ11�档
�� SO2 + NaClO3 + H2SO4�� ClO2 + NaHSO4��δ��ƽ��
�� ClO2 + NaOH��NaCl + NaClO3 + H2O��δ��ƽ��
��ش��������⣺
��1���������װ���Ʊ�ClO2

��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ__________________________________��
��װ��B�з�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ___________��
�����ռ�һ������ClO2��ѡ����ͼ�е�װ�ã�������˳��Ϊa��g��h��_________________��d��
��2��̽��ClO2��Na2S�ķ�Ӧ
�������ռ�����ClO2��N2ϡ������ǿ���ȶ��ԣ�����������ϡ�ͺ��ClO2ͨ����ͼ��ʾװ���г�ַ�Ӧ���õ���ɫ������Һ��һ��ʱ���ͨ������ʵ��̽�����з�Ӧ�IJ���
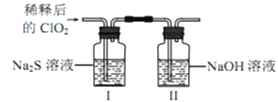
�������� | ʵ������ | ���� |
ȡ����������Һ�����Թܼ��У��μ�Ʒ����Һ�����ᡣ | Ʒ����Һʼ�ղ���ɫ | ����_______���ɡ� |
��ȡ����������Һ�����Թ����У�����Ba(OH)2��Һ�����ᣬ�� | ��___________ | ��SO42-���� |
�ۼ������Թ����м���Ba(OH)2��Һ�����������ã�ȡ�ϲ���Һ�����Թܱ��У�______________�� | �а�ɫ�������� | ��Cl-���� |
��ClO2��Na2S��Ӧ�����ӷ���ʽΪ_________________________________________�����ڴ��������ˮʱ��ClO2�����Cl2���ŵ���_____________________________________________����дһ������
���𰸡�Cu + 2H2SO4��Ũ��![]() CuSO4 + SO2�� + 2H2O 2:1 b��c��e��f SO2 �а�ɫ���� �������������ữ��AgNO3��Һ 8ClO2 + 5S2- + 4H2O
CuSO4 + SO2�� + 2H2O 2:1 b��c��e��f SO2 �а�ɫ���� �������������ữ��AgNO3��Һ 8ClO2 + 5S2- + 4H2O![]() 8Cl- + 5SO42- + 8H+ ������ԭΪCl-ʱ��ClO2�õ��ĵ�������Cl2��2.5��������ClO2�������٣�����������������ȶ���ClO2��������ף� ��ClO2�������ɿ��ܶ������к����л��Ȼ���ȣ��������ɣ�
8Cl- + 5SO42- + 8H+ ������ԭΪCl-ʱ��ClO2�õ��ĵ�������Cl2��2.5��������ClO2�������٣�����������������ȶ���ClO2��������ף� ��ClO2�������ɿ��ܶ������к����л��Ȼ���ȣ��������ɣ�
��������
��װ��A��Cu��Ũ���ᷴӦ�Ʊ����������仯ѧ����ʽΪ��Cu+2H2SO4(Ũ)![]() CuSO4+SO2��+2H2O���ʴ�Ϊ��Cu+2H2SO4(Ũ)
CuSO4+SO2��+2H2O���ʴ�Ϊ��Cu+2H2SO4(Ũ)![]() CuSO4+SO2��+2H2O��
CuSO4+SO2��+2H2O��
��������֪װ��B�з�ӦΪSO2 + 2NaClO3 + H2SO4= 2ClO2 + 2NaHSO4�������������뻹ԭ�������ʵ���֮��Ϊ2:1���𰸣�2:1��
�۶��������a������Ϊ��ֹ��������Ӧ��B֮ǰ�а�ȫƿ����a��g��h��Ϊ��Ӧ��֣���������Bװ���е�b���������ȷе�ϵͣ�����D�б�ˮԡ�ռ���Ϊ�����ȴ�������ռ���������e�������������������δ��Ӧ��Ķ�������ֹ��Ⱦ����������˳��Ϊ��a��g��h��b��c��e��f��d���ʴ�Ϊ��b��c��e��f��
���ڢ��з�Ӧ�������Һ����Ʒ�죬Ʒ��ʼ�ղ���ɫ��˵����������SO2��Ư�����õ�����ɫ����������SO2���ɡ��𰸣�SO2��
�ڢ��з�Ӧ�������Һ����Ba(OH)2����������SO42-���ɣ����Է�Ӧ����BaSO4������ӦΪ��ɫ�������𰸣���ɫ������
�����ɿ���֤��Cl-���ڵİ�ɫ��������ô����ӦΪ��������ϡ�����ữ��AgNO3��Һ���𰸣��������������ữ��AgNO3��Һ��
������������֪����������SO42-��Cl-�����ܼ�H2O��ȫ��Ӧ����ʽ���������ӷ���ʽΪ8ClO2 + 5S2- + 4H2O![]() 8Cl- + 5SO42- + 8H+��ClO2�����Cl2�ŵ������ ClO2����Ч�����ף���������������ȶ���ClO2��ˮ�е��ܽ�ȴ�ʣ���ClO2�������������Ⱦ��������ԭΪCl-ʱ��ClO2�õ��ĵ�������Cl2��2.5���ȡ�
8Cl- + 5SO42- + 8H+��ClO2�����Cl2�ŵ������ ClO2����Ч�����ף���������������ȶ���ClO2��ˮ�е��ܽ�ȴ�ʣ���ClO2�������������Ⱦ��������ԭΪCl-ʱ��ClO2�õ��ĵ�������Cl2��2.5���ȡ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѽ�����ѧƽ���ij���淴ӦX(g)+2Y(g)![]() 2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����
2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����
�����������������һ�����ӣ�������������һ�����ӣ� ����Ӧ���ת����һ������
����Ӧ���Ũ��һ�����ͣ�������Ӧ����һ�������淴Ӧ���ʣ���һ��ʹ�ô���
A���٢ڢ� B���ۢܢ� C���ڢ� D���ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У���ʹ�õ�װ�ã��г�װ���ԣ����Լ��Ͳ�����������������
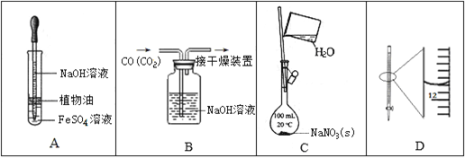
A. �۲�Fe(OH)2������
B. ��ȥCO�е�CO2
C. ����һ�����ʵ���Ũ�ȵ�NaNO3��Һ
D. 25 mL�ζ��ܶ���Ϊ11.80 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һƿ���ҵĻ�����֪���ҵ�ijЩ�������±���ʾ��
���� | �۵�/ �� | �е�/ �� | �ܶ�/ g��cm3 | ˮ�е��ܽ��� |
�� | -98 | 57.5 | 0.93 | ���� |
�� | -84 | 77 | 0.90 | ���� |
�ݴˣ������һ������ķ�����
A. ���� B. ������ C. ��ȡ�� D. ���˷�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���з�Ӧ��
��![]() ����H=
����H=![]() 196��6kJmol-1
196��6kJmol-1
��![]() ����H��0
����H��0
��![]() ����H��
����H��![]() 92.4 kJmol-1
92.4 kJmol-1
��1����һ����������һ�ܱ������г���1mol SO2��0.5mol O2,��ַ�Ӧ�ų�������_________���������������������98.3kJ��������_____________________��
��2����Ӧ�ڵĻ�ѧƽ�ⳣ������ʽK��___________���¶Ƚ���ʱ��Kֵ_______�����������С������Ӱ�족����
��3����0.2L���ܱ������У�����1.0mol N2 �� 3.0mol H2���÷�Ӧ�ﵽƽ��ʱ�����ƽ�������������ʵ���Ϊ3 mol����ƽ��ʱ������ת���ʣ�___________��
��4����Ӧ����Ϊ��Ч���������ת���ʣ������Ͽɲ�ȡ�Ĵ�ʩ��____________________��
A.�����¶� B.����ѹǿ C.��Сѹǿ D.��ʱ�Ƴ��� E.ѭ�����úͲ��ϲ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.0mL0.10molL-1��ˮ�е���0.10molL-1�����ᣬ��Һ��pH����������������ϵ��ͼ����֪0.10molL-1��ˮ�ĵ����Ϊ1.32%����������������ǣ� ��

A. �õζ�����Ӧ��ѡ�������Ϊָʾ�� B. M���Ӧ���������С��20.0mL
C. M�㴦����Һ��c(H��)=c(OH��) D. N�㴦����Һ��pH>12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ɱ���ܱ������о�����1mol��A2��2mol��B2������Ӧ��A2(g)+2B2(g)![]() 2AB2(g) ��H��ά������������ѹǿ�ֱ�Ϊp1��p2���ڲ�ͬ�¶��´ﵽƽ�⣬���ƽ��ʱAB2������������¶ȵı仯��ͼ��ʾ��
2AB2(g) ��H��ά������������ѹǿ�ֱ�Ϊp1��p2���ڲ�ͬ�¶��´ﵽƽ�⣬���ƽ��ʱAB2������������¶ȵı仯��ͼ��ʾ��
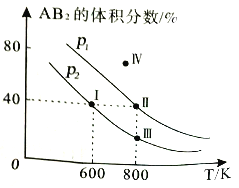
��֪:ͼ�Т������������ϣ�IV�㲻��������
����������ȷ����
A. ���͢�㷴Ӧ������� B. IV��ʱ��Ӧδ����ƽ��v(��)<v(��)
C. I��ʱ��A��ƽ��ת����Ϊ40% D. ����II����Ӧ������ȴ��600K���ɱ�ɵ�I
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��������ݻ���ͬ�ĺ����ܱ������а���ͬ�ķ�ʽͶ�뷴Ӧ�������Ӧ N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4kJ/mol,��÷�Ӧ������������±�:
2NH3(g) ��H=-92.4kJ/mol,��÷�Ӧ������������±�:
������ | ������ | ������ | |
��Ӧ�¶�/�� | 400 | 400 | 500 |
��Ӧ��Ͷ���� | 1molN2��3molH2 | 4molNH3 | 1molN2��3molH2 |
ƽ��ʱv(��)(H2)/mol/(Ls) | v1 | v2 | v3 |
ƽ��ʱc(NH3)/(mol/L) | c1 | c2 | c3 |
ƽ��ʱ��ѹǿP/Pa | P1 | P2 | P3 |
���ʵ�ƽ��ת����a | a1(N2) | a2(NH3) | a3(N2) |
ƽ�ⳣ��K | K1 | K2 | K3 |
���й�ϵ��ȷ����
A. v1<v2��c1<2c2 B. c2>2c3��a2(NH3)+a3(N2)<1
C. K1>K3�� P2>2P3 D. v1<v3��a1(N2)<a3(N2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Ч���ÿ��Ի�������ЧӦ����Դ��ȱ���⡣
��1����̬ CO2���ɱ���������������___________��������ѧ������Ϊ__________(��Ǽ��Լ������Լ��������Ӽ�����ͬ)��CO2��Na2O2��Ӧ�����γɻ�ѧ������Ϊ______________________________��
��2���п�Ժ�Ŀ�����Ա��Na-Fe3O4��HMCM-22 �ı��潫CO2ת��Ϊ���������������ͼ��
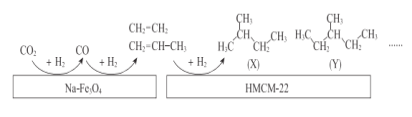
��Na-Fe3O4��HMCM-22 �ڷ�Ӧ�е�����Ϊ_______________��
��д��(X)������ͬ���칹��ṹ��ʽ_______________��
�۹���X��Y��˵����ȷ����__________(����š���
a.���ʽ��ͬ b.����4��һ�ȴ���
c.����ʹ����KMnO4��Һ��ɫ d.X��Y����ͬϵ��
(3)ͬ��ͬѹ�£������ܶ�������15��������(M)��д������������Ӧ����һ�ȴ����ķ���ʽ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com