
【题目】达喜是常用的中和胃酸的药物,其有效成分是含结晶水的铝镁碱式盐。取该碱式盐6.02g,向其中逐滴加入4.00mol·L-1的盐酸,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时恰好反应完全。
(1)计算该碱式盐样品中碳酸根与氢氧根的物质的量之比:__。
(2)若达喜中镁、铝元素的物质的量之比为3:1,则氢元素的质量分数为__。
【答案】1:16 4.00%
【解析】
碱式碳酸盐与盐酸反应过程中先中和碱,再和碳酸盐生成碳酸氢盐,然后才会放出CO2气体,涉及到的化学反应有:①OH-+H+=H2O;②CO32-+H+═HCO3-;③HCO3-+H+═H2O+CO2↑;利用质量守恒,结合化学方程式计算。
(1)当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,所发生的反应分别为:①OH+H+=H2O;②CO32+H+═HCO3;③HCO3+H+═H2O+CO2↑;可得n(CO2)=n(CO32)=(45.0-42.5)×103L×4mol/L=0.01mol,而中和OH需要盐酸42.5mL2.5mL=40mL,所以n(OH)=40×103L×4mol/L=0.16mol,则n(CO32):n(OH) =1:16;
(2)镁、铝元素物质的量之比为3:1,令镁元素物质的量为3xmol,铝元素物质的量为xmol,根据化合价的代数和为0,则有6x+3x=0.16+0.01×2,解得x=0.02mol,结晶水的质量为(6.020.06×240.02×270.16×170.01×60)g=0.72g,n(H2O)=![]() =0.04mol,因此H元素质量分数为:
=0.04mol,因此H元素质量分数为:![]() ×100%≈4%。
×100%≈4%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】稀土元素包括钪、钇和镧系(含Ce、Eu )共17种元素, 是重要的战略资源,我省稀土资源非常丰富.某彩色电视机显示屏生产过程中产生大量的废荧光粉末含 ( Eu2O3、SiO2、Fe2O3、CeO2、MnO 等物质).某课题组以此粉末为原料, 设计如下工艺流程对资源进行回收,得到较为纯净的CeO2和Eu2O3 (氧化铕).
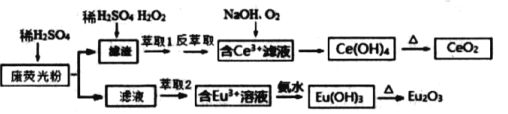
已知:CeO2 不溶于桸硫酸,也不溶于NaOH 溶液,Eu2O3可溶于稀硫酸
(1)往滤渣中加稀硫酸和H2O2进行酸浸,反应的离子方程式____________ 。为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是________________________________。
(2)有机物HR能将Ce3+从水溶液中萃取出来.该过程可表示为:Ce3+(水层)+3HR(有机层)![]() CeR3(有机层)+3H+(水层)。向 CeR3(有机层)中加入稀硫酸进行反萃取能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________________________。
CeR3(有机层)+3H+(水层)。向 CeR3(有机层)中加入稀硫酸进行反萃取能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________________________。
(3)流程中由含 Ce3+滤液生成Ce(OH)4的离子方程式____________________。
(4)取上述流程中得到的Ce(OH)4 产品 0.52 g, 加硫酸溶解后,用浓度为 0.1000molL-1FeSO4标准溶液滴定至终点时,铈被还原为Ce3+ , 消耗 24.00 mL 标准溶液。该产品中 Ce(OH)4的质量分数为___________。
(5)已知含 Ce3+溶液也可以先加碱调 pH后再通入氧气氧化可得到Ce(OH)4。298K 时,Ksp[Ce(OH)3]=5×10-20,若溶液中c(Ce3+)=0.05molL-1, 加碱调节pH 到_____时Ce3+开始沉淀(忽略加碱过程中溶液体积变化).
(6)萃取剂对金属离子的萃取率与 pH的关系如图所示.流程中为了用萃取剂除去金属杂质离子,进行萃取2 最适宜的pH 是_______(填选项序号).其原因是 _____。
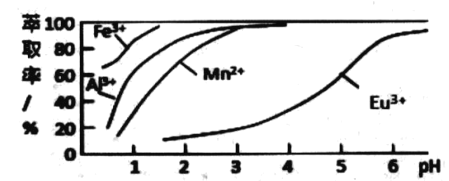
A. 2.0 左右 B . 3.0 左右 C. 5.0 左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A. 标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2NA
B. 标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数等于2NA
C. NO2和H2O反应每生成2 mol HNO3时转移的电子数目为2NA
D. 1 mol Fe在氧气中充分燃烧失去3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置中,M为金属活动性顺序表中位于氢之前的金属,N为石墨棒,下列关于此装置的叙述中不正确的是

A.N上有气体放出
B.M为负极,N为正极
C.是化学能转变为电能的装置
D.导线中有电流通过,电流方向是由M到N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某同学做如下实验,以探究反应中的能量变化。
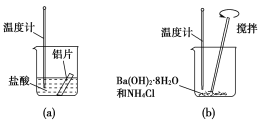
(1)在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是________热反应;(b)中温度降低,由此可以判断(b)中反应是________热反应。
(2)根据能量守恒定律,(b)中反应物的总能量应该________生成物的总能量。
II.某学习小组依据氧化还原反应原理:2Ag++Cu=Cu2++2Ag设计成的原电池如右图所示。
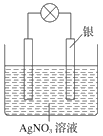
(3) 从能量转化角度分析,上述原电池将化学能转化为_________ ;
(4) 负极的电极材料为_____________;
(5) 正极发生的电极反应__________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、M均为短周期主族元素。25℃时,各元素最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH和原子半径的关系如图所示。下列说法不正确的是( )
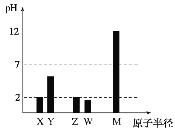
A. 从图中得出同浓度下W的最高价氧化物对应的水化物的pH比Z小,故非金属性:W>Z
B. X、Z的最简单气态氢化物在常温下可以反应生成离子化合物
C. X、Y、Z、W、M五种元素单质中Y常见单质熔点最高
D. 简单离子半径大小顺序:X>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期的多数元素及其化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1) 基态Ti原子中,最高能层电子的电子云轮廓形状为___,与Ti同周期的所有过渡元素的基态原子中,写出任意一种最外层电子数与钛不同的元素外围电子排布式_____。
(2) 琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_________________。
(3) SCN— 可用于Fe3+的检验,写出与SCN— 互为等电子体的一种微粒:_____。
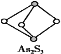
(4) 成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如图,As原子的杂化方式为______,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式:__________________。SnCl4分子的立体构型为_______。
(5)金红石(TiO2)是含钛的主要矿物之一,具有典型的四方晶系结构,其晶胞结构(晶胞中相同位置的原子相同)如图所示(注意:D不在体心):
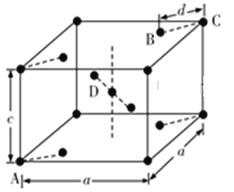
①4个微粒A、B、C、D中,属于氧原子的是________________。
②若A、B、C原子的坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D原子的坐标为D(0.19a,____, ____);若晶胞底面边长为x,则钛氧键的键长d=_______(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO、NaNO3、Na2SO3等钠盐在多领域有着较广的应用。
(1)上述三种盐所涉及的五种元素中,半径较小的原子是______________;原子核外最外层p亚层上电子自旋状态只有一种的元素是_____________。
(2)碱性条件下,铝粉可除去工业废水中的NaNO2,处理过程中产生一种能使湿润红色石蕊试纸变蓝的气体。产物中铝元素的存在形式_____________(填化学符号);每摩尔铝粉可处理_____________gNaNO2。
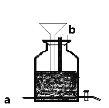
(3)新冠疫情发生后,有人用电解食盐水自制NaClO消毒液,装置如图(电极都是石墨)。电极a应接在直流电源的_____________极;该装置中发生的化学方程式为_____________
(4)Na2SO3溶液中存在水解平衡![]() +H2O
+H2O![]()
![]() +
+![]() 设计简单实验证明该平衡存在__________________。0.1mol/L Na2SO3溶液先升温再降温,过程中(溶液体积变化不计)PH如下。
设计简单实验证明该平衡存在__________________。0.1mol/L Na2SO3溶液先升温再降温,过程中(溶液体积变化不计)PH如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
PH | 9.66 | 9.52 | 9.37 | 9.25 |
升温过程中PH减小的原因是_____________;①与④相比;C(![]() )①____________④(填“>”或“<”).
)①____________④(填“>”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:

为制备纯净干燥的气体,下表中缺少的药品是:
装置Ⅰ | 装置Ⅱ | ||
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ①___ | ②___ |
制备纯净NO | Cu | ③___ | ④___ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________。
③装置Ⅶ的作用是____________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气, 该反应的化学方程式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com