
【题目】下列有关物质的性质与用途具有对应关系的是
A.Fe2(SO4)3易溶于水,可用作净水剂
B.Al2O3熔点高,可用作耐高温材料
C.铁比铜金属性强,可用FeCl3腐蚀Cu刻制印刷电路板
D.NaHCO3溶于水呈碱性,可作抗酸药,服用时喝些醋能提高药效
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
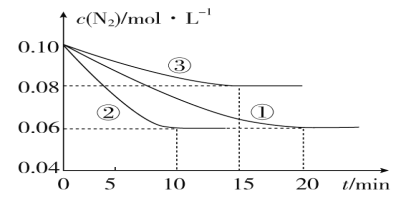
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=____________;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的________、________(填字母编号)。
a.增大压强 b.减小压强
c.升高温度 d.降低温度
e.使用催化剂
(2)800 K时向下列起始体积相同的密闭容器中充入2 mol N2、3 mol H2,甲容器在反应过程中保持温度压强不变,乙容器保持温度体积不变,丙容器是绝热容器保持体积不变,三容器各自建立化学平衡。
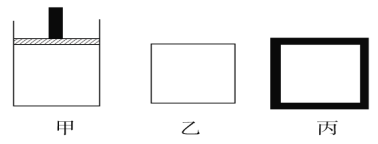
①达到平衡时,平衡常数K甲________K乙________K丙(填“>”“<”或“=”)。
②达到平衡时N2的浓度c(N2)甲________c(N2)乙,c(N2)乙________c(N2)丙(填“>”“<”或“=”)。
③对甲、乙、丙三容器的描述,以下说法正确的是____________。
A.甲容器气体密度不再变化时,说明此反应已达到平衡状态
B.在乙中充入稀有气体He,化学反应速率加快
C.丙容器温度不再变化时说明已达平衡状态
D.向丙容器中充入氨气,正向速率减小,逆向速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500~600℃的铁屑中通入氯气生产氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行实验。

回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为 ,装置B中加入的试剂是 。
(2)制取无水氯化亚铁的实验中,装置A用来制取 。尾气的成分是 。若仍用D的装置进行尾气处理,存在的问题是 。
(3)若操作不当,制得的FeCl2 会含有少量FeCl3 ,检验FeCl3常用的试剂是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下:

Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入3 mL浓硫酸、12.2 g苯甲酸、20 mL甲醇(密度约为0.79 g/cm3)。
(1)液体混合时,正确的加入顺序是 。
(2)为防止圆底烧瓶中的液体在实验时发生暴沸,在加热前应采取的措施是 。
(3)在该反应中反应物甲醇应过量,其理由是 。
Ⅱ.粗产品的精制
(4)现拟用下列流程精制苯甲酸甲酯,请根据流程图填入恰当操作方法的名称:操作1为 ,操作2为 。

(5)苯甲酸甲酯的产率为 。
(6)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,某同学做了如下检验。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
① CO(g)+2H2(g)![]() CH3OH(g) △H 1=-90.7 kJ·mol-1
CH3OH(g) △H 1=-90.7 kJ·mol-1
② 2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) △H 3=-41.2kJ·mol-1
CO2(g)+H2(g) △H 3=-41.2kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。
(2)反应②达平衡后采取下列措施,能提高CH3OCH3产率的有 。
A.加入CH3OH B.升高温度 C.增大压强 D.移出H2O E.使用催化剂
(3)以下说法能说明反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)达到平衡状态的有____。
CH3OCH3(g)+CO2(g)达到平衡状态的有____。
A.H2和CO2的浓度之比为3:1
B.单位时间内断裂3个H-H同时断裂1个C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) ![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(P分)=气体总压(P总)×体积分数。
①该反应△H_____0(填“>”、“<”或“=”),550℃时,平衡后若充入惰性气体,平衡_______(填“正移”、“逆移”或“不移动”)
②650℃时,反应达平衡后CO2的转化率为__________________(保留2位有效数字)。
③T时,用平衡分压代替平衡浓度表示的化学平衡常数KP=_________P总。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
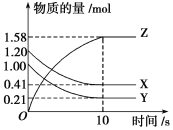
(1)从反应开始到10 s时,用Z表示的反应速率为_____________________________。
(2)该反应的化学方程式为__________________________________________________。
Ⅱ.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明2SO2(g)+O2(g)![]() 2SO3(g)达到平衡状态的是_______(填序号,下同)。
2SO3(g)达到平衡状态的是_______(填序号,下同)。
(2)一定能证明I2(g)+H2(g)![]() 2HI(g)达到平衡状态的是 ____________。
2HI(g)达到平衡状态的是 ____________。
(3)一定能证明A(s)+2B(g)![]() C(g)+D(g)达到平衡状态的是_________。
C(g)+D(g)达到平衡状态的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂。实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:


(1)电解时的阳极反应方程式为____________________________________。
(2)除去ClO2中的NH3可选用的试剂为是_____(填标号)
A.水 B.浓硫酸 C.碱石灰 D.饱和食盐水
(3)用右图装置可以测定混合气中ClO2的含量:
I.在锥形瓶中加入足量的碘化钾,用50ml水溶解后,再加入3ml稀硫酸;
II.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
III.将一定量的混合气体通入锥形瓶中吸收;
IV.将玻璃液封装置中的水倒入锥形瓶中;
V.用0.2000mol/L 硫代酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32—===2I—+S4O62—),指示剂显示终点时共用去20.00ml硫代酸钠溶液。在此过程中:
①玻璃液封装置的作用是_________。
② V中加入的指示剂通常为______,滴定至终点的现象是______。
③测定混合气中ClO2的质量为______g。
④用此方法测定混合气中ClO2的质量常常偏高,可能的原因是_____(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、 F是周期表中短周期的六种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 地壳中含量最多的元素 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
(1)请写出B、D、F三种元素的名称: 、 、 。
(2)A与C以原子个数比为1:1形成的化合物的电子式为 ,
将4mol该化合物投入到2L1mol/L BE3溶液中的离子方程式
为 、 。
(3)写出实验室制备F的氢化物的化学方程式 。
(4)下图可用于实验证明D、E的非金属性的强弱。

①溶液a和b分别为 , (写化学式)。
②非金属性D E(填大于或小于),请从原子结构的角度解释原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下非金属氧化物与其引起的环境问题及主要来源对应正确的是 ( )
氧化物 | 环境问题 | 主要来源 | |
A | CO2 | 酸雨 | 化石燃料的燃烧 |
B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
C | NO2 | 温室效应 | 工厂废气的排放 |
D | CO | CO中毒 | 燃料的不完全燃烧 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com