
【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下:

Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入3 mL浓硫酸、12.2 g苯甲酸、20 mL甲醇(密度约为0.79 g/cm3)。
(1)液体混合时,正确的加入顺序是 。
(2)为防止圆底烧瓶中的液体在实验时发生暴沸,在加热前应采取的措施是 。
(3)在该反应中反应物甲醇应过量,其理由是 。
Ⅱ.粗产品的精制
(4)现拟用下列流程精制苯甲酸甲酯,请根据流程图填入恰当操作方法的名称:操作1为 ,操作2为 。

(5)苯甲酸甲酯的产率为 。
(6)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,某同学做了如下检验。

【答案】(1)先加入12.2 g苯甲酸和20 mL甲醇,再小心加入3 mL浓硫酸
(2)加入几粒沸石或碎瓷片
(3)该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,故可增加甲醇的量,以提高苯甲酸的转化率
(4)分液 蒸馏
(5)65%
(6)如表
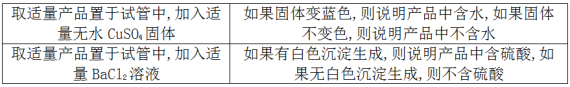
【解析】本题主要考查常见物质的制备、检验、分离提纯,意在考查考生的基本实验技能。
(1)当浓硫酸与其他溶液混合时,应先加密度较小的溶液,再缓慢加入浓硫酸,并不断搅拌,防止暴沸而使溶液溅出。(2)加热时为防止液体暴沸,应加入沸石或碎瓷片。(3)制取苯甲酸甲酯的反应为可逆反应,通常采用提高价廉物质的浓度使平衡右移,从而提高贵重原料的转化率,提高经济效益。(4)有机物大部分不溶于水且与水分层,故可以采用分液的方法加以分离;有机混合物常利用沸点的差异(相差20 ℃以上)通过蒸馏进行分离。
(5)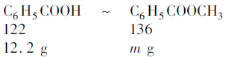
计算可得m=13.6,所以苯甲酸甲酯的产率=×100%=×100%=65%。


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g) + O2(g) ![]() 2NO(g) △H1=+180.5 kJ·mol-1
2NO(g) △H1=+180.5 kJ·mol-1
② C和CO的燃烧热(△H)分别为-393.5 kJ·mol-1和-283 kJ·mol-1
则2NO(g) + 2CO(g) ![]() N2(g) + 2CO2(g)的△H=_____kJ·mol-1
N2(g) + 2CO2(g)的△H=_____kJ·mol-1
(2)将0.20 mol NO和0.10 mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
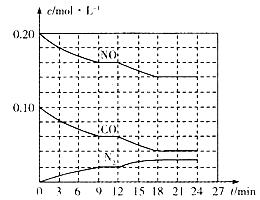
①CO在0-9min内的平均反应速率v(CO)=________mol·L-1·min-1(保留两位有效数字);第12 min时改变的反应条件可能为________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24 min时达到平衡状态,CO2的体积分数为________(保留三位有效数字),化学平衡常数值为________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收,若将一定量的SO2气体通入到300mL NaOH的溶液中,再在所得溶液中逐滴加入稀盐酸至过量,产生的气体与反应的HCl两者物质的量的关系如图所示(气体的溶解和HCl的挥发忽略,NaHSO3水溶液为酸性):
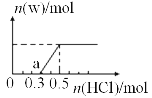
①O点溶液中所含溶质的化学式为_________________;
②a点溶液中各离子溶度大小关系为______________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)下列操作中,容量瓶所不具备的功能有________(填序号)。

A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为______g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1(填“大于”“等于”或“小于”,下同)。若NaOH溶液在转移至容量瓶时未经冷却,则所得溶液浓度________0.1 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图.其中A是面粉的主要成分;C和E反应能生成F,F具有香味.
![]()
在有机物中,凡是具有﹣CHO结构的物质,具有如下性质:
(1)与新制的氢氧化铜悬浊液反应,产生砖红色的沉淀;
(2)在催化剂的作用下,﹣CHO被氧气氧化为﹣COOH,即:
2R﹣CHO+O2 ![]() 2R﹣COOH
2R﹣COOH
根据以上信息及各物质的转化关系完成下列各题:
(1)A的分子式为 ,B中含有的官能团有 ,与B互为同分异构体的一种物质的名称 。
(2)A→F中,能与新制氢氧化铜悬浊液产生砖红色的沉淀的物质有 (填名称)。
(3)E与小苏打溶液反应的离子方程式为 。
(4)C→D的化学方程式为
反应类型为 反应。
(5)C+E→F的化学方程式为 。
(6)写出符合下列条件的F的所有同分异构体的结构简式
①与F具有相同的官能团
②没有支链。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)d在元素周期表的位置是__________。
(2)d、e、f常见简单离子的半径由大到小为___________(用化学式表示,下同);y、f、g、h的最高价氧化物对应的水化物的酸性由强到弱是:______________________________。
(3)用电子式表示由x和g两种元素形成的化合物的形成过程____________________。由x、y、d三种元素形成的相对分子质量最小的化合物可作为燃料电池的燃料,以KOH溶液为电解质溶液,写出负极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是实验室用浓硫酸、溴化钠(先生成HBr)与乙醇反应来制备溴乙烷(C2H5Br)的装置,反应需要加热,图中省去了夹持与加热装置,有关物质的性质如下表。


(1)分别写出A、B两种仪器的名称 、 。
(2)冷却剂应从 (填“h”或“i”)口进入冷凝管C中,制备操作中,加入的浓硫酸必须进行适当稀释,其目的(或原因)是 (填字母)。
a.水是反应的催化剂 b.减少Br2的生成 c.减少HBr的挥发
(3)加热的目的是 ,使用D进行冷却的原因是 。
(4)A中液面上有深红棕色气体出现,写出生成它的化学方程式 ,写出A中生成溴乙烷的化学方程式 。
(5)将E中产品转入到分液漏斗中,再向漏斗中加入适量Na2SO3溶液,振荡静置后分液。加入Na2SO3溶液的目的是 ,分液时目标产物离开漏斗的方式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A.Fe2(SO4)3易溶于水,可用作净水剂
B.Al2O3熔点高,可用作耐高温材料
C.铁比铜金属性强,可用FeCl3腐蚀Cu刻制印刷电路板
D.NaHCO3溶于水呈碱性,可作抗酸药,服用时喝些醋能提高药效
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
A.CO2是氧化产物
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.ClO2作水处理剂时,利用了其强氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com