
【题目】为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g) + O2(g) ![]() 2NO(g) △H1=+180.5 kJ·mol-1
2NO(g) △H1=+180.5 kJ·mol-1
② C和CO的燃烧热(△H)分别为-393.5 kJ·mol-1和-283 kJ·mol-1
则2NO(g) + 2CO(g) ![]() N2(g) + 2CO2(g)的△H=_____kJ·mol-1
N2(g) + 2CO2(g)的△H=_____kJ·mol-1
(2)将0.20 mol NO和0.10 mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
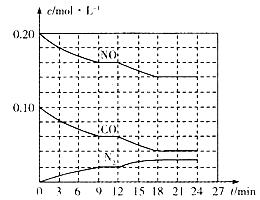
①CO在0-9min内的平均反应速率v(CO)=________mol·L-1·min-1(保留两位有效数字);第12 min时改变的反应条件可能为________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24 min时达到平衡状态,CO2的体积分数为________(保留三位有效数字),化学平衡常数值为________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收,若将一定量的SO2气体通入到300mL NaOH的溶液中,再在所得溶液中逐滴加入稀盐酸至过量,产生的气体与反应的HCl两者物质的量的关系如图所示(气体的溶解和HCl的挥发忽略,NaHSO3水溶液为酸性):
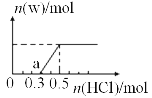
①O点溶液中所含溶质的化学式为_________________;
②a点溶液中各离子溶度大小关系为______________;
【答案】(1)-746.5;(2)①4.4×10 -3 ,D; ②22.2%,3.4;
(3)①NaOH,Na2SO3;②c(Na+) >c(Cl-)>c(HSO3-) >c(H+)>c(SO32-) c(OH-)。
【解析】
试题分析:(1)N2(g)+O2(g)=2NO(g) △H1=+180.5kJ·mol-1 ①,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1 ②,CO(g)+1/2O2(g)=CO2(g) △H=-283kJ·mol-1 ③,③×2-①得出:△H=(-283×2-180.5)kJ·mol-1=-746.5kJ·mol-1;
(2)根据化学反应速率的定义,v(CO)=(0.1-0.6)/9mol/(L·min)=4.4×10-3 mol/(L·min),NO、CO的物质的量浓度降低,N2物质的量浓度增大,说明反应向正反应方向移动,A、此反应是放热反应,根据勒夏特列原理,升高温度平衡向逆反应方向进行,故错误;B、增加NO的量,12min开始时NO的浓度增大,但图像中不变,故错误;C、使用催化剂,平衡不影响,故错误;D、降低温度,平衡向正反应方向进行,故正确;②此反应是物质的量减少的过程,当有2molNO参加反应,物质的量减少1mol,24min时CO减少物质的量为(0.1-0.04)mol=0.06mol,反应后的总物质的量为(0.3-0.06/2)mol=0.27mol,生成n(CO2)=0.06mol,则CO2的体积分数为0.06/0.27×100%=22.2%,达到平衡时n(N2)=0.03mol,根据化学平衡常数的定义,K=c2(CO2)×c(N2)/[c2(CO)×c2(NO)]=0.062×0.03/[0.142×0.042]=3.4;
(3)SO2和NaOH溶液反应,溶质可能是NaOH、Na2SO3,Na2SO3,Na2SO3、NaHSO3,NaHSO3,根据图像,从开始到出现气体,消耗的盐酸的物质的量大于0.3~0.5段消耗的盐酸的物质的量,因此O点溶质为NaOH、Na2SO3;②a点溶液溶质为NaCl、NaHSO3,HSO3-电离大于水解,因此溶液显酸性,HSO3-电离程度微弱,离子浓度大小为c(Na+)>c(HSO3-)>c(H+)。c(SO32-)>c(OH-)。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.垃圾资源化的主要途径是卫生填埋
B.人类的活动不影响氮、硫元素在自然界的循环
C.推广使用新能源,可以减少二氧化碳等温室气体的排放
D.在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分为Cu2(OH)2CO3,还含少量二价铁和三价铁的氧化物及硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:
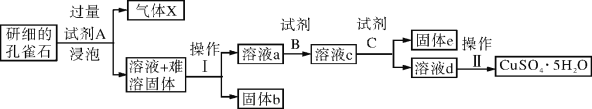
(1)试剂A的化学式是_____________;操作Ⅰ的名称是______________;
(2)生成气体X的化学方程式为:_________________________________。
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用_________
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)已知:
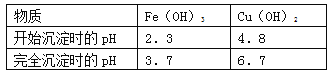
①试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离。试剂C宜选用__________:
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
②为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为__________。
(5)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论) ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列液体中,不会出现丁达尔效应的分散系是 ( )
①鸡蛋白溶液 ②水 ③淀粉溶液 ④硫酸钠溶液 ⑤沸水中滴入饱和FeCl3溶液
A.④ B.③④ C.②④ ⑤ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:


查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如右图是所示。
(1)右图中的线2表示的组分为 (填化学式)。
(2)实验时,“反应II”中加入NaOH溶液的目的是 (用化学方程式表示)。
(3)国家标准规定产品中Na2SO3的质量分数≥97.0%为优等品,≥93.0%为一等品。为了确定实验所得产品的等级,研究小组采用了两种方法进行测定。
①方法I:称取2.570g产品,用蒸馏水溶解,加入足量的双氧水使Na2SO3完全氧化生成Na2SO4,再加入过量的BaCl2溶液,所得沉淀经过过滤、洗涤、干燥后称量,质量为4.660g,通过计算确定产品中Na2SO3的质量分数(写出计算过程)
②方法II:称取1.326g产品,配成100mL溶液,取25.00mL该溶液,滴加0.1250mol/L I2溶液,恰好使Na2SO3完全氧化生成Na2SO4时,消耗I2溶液20.00mL。通过计算确定产品中Na2SO3的质量分数(写出计算过程)
③判断Na2SO3产品的等级,并说明理由。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
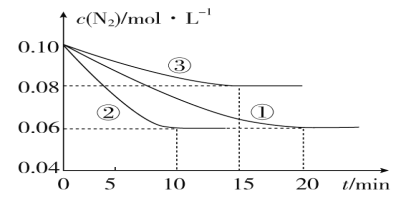
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=____________;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的________、________(填字母编号)。
a.增大压强 b.减小压强
c.升高温度 d.降低温度
e.使用催化剂
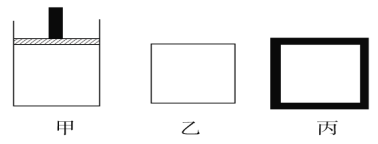
(2)800 K时向下列起始体积相同的密闭容器中充入2 mol N2、3 mol H2,甲容器在反应过程中保持温度压强不变,乙容器保持温度体积不变,丙容器是绝热容器保持体积不变,三容器各自建立化学平衡。
①达到平衡时,平衡常数K甲________K乙________K丙(填“>”“<”或“=”)。
②达到平衡时N2的浓度c(N2)甲________c(N2)乙,c(N2)乙________c(N2)丙(填“>”“<”或“=”)。
③对甲、乙、丙三容器的描述,以下说法正确的是____________。
A.甲容器气体密度不再变化时,说明此反应已达到平衡状态
B.在乙中充入稀有气体He,化学反应速率加快
C.丙容器温度不再变化时说明已达平衡状态
D.向丙容器中充入氨气,正向速率减小,逆向速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种盐X与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后的产物再溶于水可得Z溶液,Y和Z溶液反应又可生成X,则盐X是
A.NH4NO3 B.NH4Cl C.(NH4)2SO4 D.NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下:

Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入3 mL浓硫酸、12.2 g苯甲酸、20 mL甲醇(密度约为0.79 g/cm3)。
(1)液体混合时,正确的加入顺序是 。
(2)为防止圆底烧瓶中的液体在实验时发生暴沸,在加热前应采取的措施是 。
(3)在该反应中反应物甲醇应过量,其理由是 。
Ⅱ.粗产品的精制
(4)现拟用下列流程精制苯甲酸甲酯,请根据流程图填入恰当操作方法的名称:操作1为 ,操作2为 。

(5)苯甲酸甲酯的产率为 。
(6)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,某同学做了如下检验。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com