



 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 请按下列要求填空
请按下列要求填空查看答案和解析>>
科目:高中化学 来源: 题型:

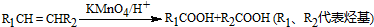

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、K+、SO42-、Cl-、AlO2- |
| B、Fe2+、H+、Br-、NO3-、Cl- |
| C、Cu2+、NO3-、OH-、Cl- |
| D、Al3+、Na+、Cl-、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①②③④ |
| C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知Ⅰ.N-N键键能为167kJ?mol-1,N≡N键键能为942kJ?mol-1,
已知Ⅰ.N-N键键能为167kJ?mol-1,N≡N键键能为942kJ?mol-1,| A、+1066.4 kJ?mol-1 |
| B、-1066.4 kJ?mol-1 |
| C、+697.6 kJ?mol-1 |
| D、-697.6 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com