
����Ŀ��1807�껯ѧ�Ҵ�ά����������������Ƶ��ƣ�4NaOH(����)![]() O2��+4Na+2H2O��������������������������������������Ҳ�Ƶ��ƣ�3Fe+4NaOH=Fe3O4+2H2��+4Na���������й�˵����ȷ����
O2��+4Na+2H2O��������������������������������������Ҳ�Ƶ��ƣ�3Fe+4NaOH=Fe3O4+2H2��+4Na���������й�˵����ȷ����
A. ��ά�����ƣ������ĵ缫��ӦʽΪ��Na++e-=Na��
B. ���������˷�����ԭ�����������Ľ����Ա��Ƶ�ǿ
C. ���ô�ά������������˷��Ƶõ������ƣ�������ת�Ƶ����������
D. �������õ�������Ȼ��Ʒ�����
���𰸡�D
��������
A.��ά�����ƣ������ĵ缫��ӦʽΪ��Na++e-=Na����������OH-ʧȥ���ӣ�����������Ӧ���缫��ӦʽΪ4OH--4e-=2H2O+ O2����A����
B.������Naǿ��Fe�����������˷�����ԭ���Ǹ����Ƶķе�ϵ͡��״ӷ�Ӧ������з���������Ӷ�ʹ��ѧƽ���������ƶ���B����
C.���ݷ�Ӧ����ʽ��֪�ô�ά����ȡ�����ƣ�ÿ��Ӧ����4molNaת�Ƶ��ӵ����ʵ�����4mol�����ø��������˷��Ƶ�4mol���ƣ�ת�Ƶ��ӵ����ʵ�����8mol�������ȡ�����Ľ����ƣ�ת�Ƶ��ӵ����ʵ�������ȣ�C����
D.����NaCl�����ӻ����NaCl����Ȼ�纬���ḻ������ڹ�ҵ�Ͽ��õ�������Ȼ��Ƶķ����ƽ����ƣ�D��ȷ��
�ʺ���ѡ����D��


 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������NOx��SO2����������Ҫ�ɷ֡�
��NOx��Ҫ��Դ������β����
��֪��N2��g����O2��g��![]() 2NO��g�� ��H����180.50 kJ��mol��1
2NO��g�� ��H����180.50 kJ��mol��1
2CO��g����O2��g��![]() 2 CO2��g�� ��H����566.00kJ��mol��1
2 CO2��g�� ��H����566.00kJ��mol��1
��1��Ϊ�˼��������Ⱦ���������������β�������ܿڲ��ô�����NO��COת��������Ⱦ����������ѭ����д���÷�Ӧ���Ȼ�ѧ����ʽ_________________��
��2��T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У������¶Ⱥ�������䣬��Ӧ���̣�0��15min����NO�����ʵ�����ʱ��仯�Ĺ�ϵ����ͼ��ʾ��


��T��ʱ�û�ѧ��Ӧ��ƽ�ⳣ��K��_______________��ƽ��ʱ�������¶Ȳ��䣬���������г���CO��N2��0.8mol��ƽ�⽫_______�ƶ���������������������������������
��ͼ��a��b�ֱ��ʾ��һ���¶��£�ʹ��������ͬ���������ͬ�Ĵ���ʱ���ﵽƽ�������n(NO)�ı仯���ߣ����б�ʾ����������ϴ��������__________������a������b������
��15minʱ�����ı���練Ӧ����������n(NO)������ͼ��ʾ�ı仯����ı������������_______��
����SO2��Ҫ��Դ��ú��ȼ�ա�ȼú��������������Ǽ��ٴ����к�������Ⱦ�Ĺؼ���
��3���ô�����Һ����SO2�ɽ���ת��ΪHSO3�����÷�Ӧ�����ӷ���ʽ��___________________��
��4����ͼ���װ�ÿɽ������е�NO��SO2�ֱ�ת��ΪNH4+��SO42��������A�Ļ�ѧʽΪ_____________�������ĵ缫��Ӧʽ��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ�ǣ� ��
A. ��ˮ��ͨ��������Cl2+H2O2H++Cl��+ClO��
B. ����������Ũ���ᷴӦ��MnO2+4HCl��Ũ��![]() Mn2++2Cl2��+2H2O
Mn2++2Cl2��+2H2O
C. ̼��������Һ�ӹ�������ʯ��ˮ��2HCO3��+Ca2++2OH���TCaCO3��+2H2O+CO32��
D. ������������ͭ��Һ��Ӧ��2Na+2H2O+Cu2+�T2Na++Cu��OH��2��+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������⣩����(��Ҫ��Ⱦ��SO2��NO��NO2)�Ĵ����ŷ�������صĴ�����Ⱦ�����ڽ����о��ɹ��Dz���������Ϊ��ԭ������������һ�廯������
(1)�����ܷ�Ӧ��SO2(g)��CO(NH2)2(aq)��2H2O(l)��1/2O2(g)��(NH2)SO4(aq)��CO2(g)����֪�÷�Ӧ���Է����У���������____(�������������������������κ��¶���)��
(2)���ϡ�����Ʊ�O3(ԭ����ͼ)�������O3�ĵ缫��ӦʽΪ______��


(3)�����£������ݵķ�Ӧ���м���̶����ʵ�����SO2��NO��ͨ��O3��ֻ�ϡ���Ӧ��ͬʱ�����ֵ����ʵ�����n(O3)��n(NO)�ı仯����ͼ��
�� n(NO2)��n(O3)��n(NO)�ı仯�����Ӻ���٣�ԭ����____��
�� �������Է�ӦSO2(g)��O3(g)��SO3(g)��O2(g)��Ӱ�첻�����ù���̬���۽��Ϳ���ԭ��__��
(4)ͨ�����Ʊ������о��ѳ�Ч�ʵ�Ӱ�����صõ���������ͼ��ʾ������˵����ȷ����____��
A. ������������Һ�еķ�Ӧ��v(����)��v(����)
B. ������ҺpH�ı仯������Ч�ʵ�Ӱ����ڶ�����Ч�ʵ�Ӱ��
C. ǿ���������²��������ضԵ���������ѳ�
D. pH=7��������Һ����Ч�����


(5)���ص��Ʊ���2NH3(g)��CO2(g)![]() CO(NH2)2(s)��H2O(g) ��H��0��һ�������£���10 L�����ܱ������г���2 mol NH3��1 mol CO2��
CO(NH2)2(s)��H2O(g) ��H��0��һ�������£���10 L�����ܱ������г���2 mol NH3��1 mol CO2��
�� �÷�Ӧ10 min ��ﵽƽ�⣬��������������ܶ�Ϊ4.8 g��L��1��ƽ�ⳣ��K=__��

�� ��ͼ�Ǹ������£�ϵͳ�����ص����ʵ����淴Ӧʱ��ı仯���ƣ�����Ӧʱ��ﵽ3min ʱ��Ѹ�ٽ���ϵ���£�����ͼ�л���3~10 min �����������ص����ʵ����ı仯��������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij������ľ�������������С��Ԫ���öѻ����ɵ�,���ڸû���������������д������

![]()
A. 1 mol�û���������1 mol Y B. 1 mol�û���������1 mol Ba
C. 1 mol�û���������7 mol O D. �û�����Ļ�ѧʽ��YBa2Cu3O7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(FexNy)�ڴż�¼�����������Ź㷺��Ӧ��ǰ����ijFexNy���Ʊ���������������ͪ���Ҵ����롣
��1��Fe��̬ԭ�ӽṹʾ��ͼ__________��
��2����ͪ( )�����и�Ԫ�ص縺�ԴӴ�С˳����________��1 mol��ͪ�����к��ЦҼ�����ĿΪ________��
)�����и�Ԫ�ص縺�ԴӴ�С˳����________��1 mol��ͪ�����к��ЦҼ�����ĿΪ________��
��3��ijFexNy�ľ�����ͼ1��ʾ��Cu������ȫ����þ�����aλ��Fe����bλ��Fe���γ�Cu����Ͳ���Fe(x��n)CunNy��FexNyת��Ϊ����Cu����Ͳ���������仯��ͼ2��ʾ�����и��ȶ���Cu����Ͳ���Ļ�ѧʽΪ________��


��4����ѧ���Ƶ���20��̼ԭ����ɵ� ������״����C20������״�ṹ��������������ι��ɣ���ͼ����

��ش�:һ�� C20���ӹ���_______����ߣ��Ʋ�C20�����Ӳ��_______����ϴ���С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȩ��Ũ����������Һ�з���Cannizzaro��Ӧ����Ӧ����ʽ���£��������Ʊ�������ͱ��״���
2![]() +KOH
+KOH![]()
![]() \
\
![]() +HCl
+HCl![]()
��֪��
����������ˮ�����л������õ��ܼ����е�34.6�棬���ӷ����ڿ����еķе�160�档
�ڱ�������ˮ�е��ܽ��0.17g(25��),0.95g(50��),6.8g(95��)
ʵ�鲽�裺
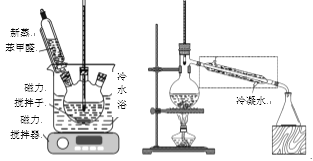
����50mL����ƿ�м���4.5g KOH��4.5mLˮ����װ��������ˮԡ�У���������������������5mL ��������ȩ(�ܶ�1.04g/mL)��ʹ��Ӧ���ֻ��(������ͼ)������Ϊ��ɫ��״�����24h���ϡ�
����Ӧ���������������ˮ����ʹ����ȫ�ܽ����_____(��װ������)�У���10mL ������ȡ3�Σ��ϲ�������ȡҺ����������3mL�������������ơ�5mL 10% Na2CO3��Һ��5mLˮϴ�ӣ��ֳ������Ѳ�����ˮNa2CO3���
�۸�����������Һ��ˮԡ����ȥ���ѣ�Ȼ���ʵ���������װ��(������ͼ)���������������ռ�198�桫204��ı��״���֣�����Ϊ2.16g��
��������ȡ���ˮ��Һ(ˮ��)����Ũ�����ữ�������ȴ��ʹ��������ȫ���������ˣ��ֲ�Ʒ��ˮ�ؽᾧ�õ������ᣬ������2g��
(1)���Ͻ���Ȼ�����24h��Ŀ����____________________________________
(2)����ں��ߴ�װ��������___________________________
(3)��ȡҺ��ϴ����3�Σ�����10% ̼������Һ����ȥ��������_______(�ѧʽ)

(4)ʹ��ˮԡ��ȥ���ѵ��ŵ���_____________
(5)��ȥ���Ѻ��ʵ��ĵ�������װ�ã�Ӧ������ͼ���߿��е�װ�û�Ϊ________��
(6)�������ؽᾧʱ��������ˮϴ�ӹ��壬��Ŀ����______���������ؽᾧʱ����IJ���������__________________
���ձ� ���Թ� ����ƿ �ܾƾ��� ����Ͳ �̾�����©�� �߲�����
(7)��ʵ����Cannizzaro��Ӧ��ת������_____%(����1λС��)��ͨ������ʵ���б�����IJ��ʻ�ȱ��״����ͣ�������ij��ʵ���в�δ����ƿ�������±�����IJ�������ƫ�ߣ��������ܵ�ԭ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������е�һ����������巢����Ӧ��x A(g) + y B(g) ![]() z C(g)��ƽ��ʱ���A��Ũ��Ϊ0.5 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴδﵽƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.3 mol/L�������й��ж���ȷ���ǣ� ��
z C(g)��ƽ��ʱ���A��Ũ��Ϊ0.5 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴδﵽƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.3 mol/L�������й��ж���ȷ���ǣ� ��
A��x + y < z B��B��ת���ʽ���
C��ƽ��������Ӧ�����ƶ� D��C�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[���ʽṹ������]
������ͭ�ķ�Ӧ֮һΪ2CuFeS2��O2![]() Cu2S��2FeS��SO2��
Cu2S��2FeS��SO2��
(1) Cu����̬��������Ų�ʽΪ________________��

(2) Cu��Zn�ĵڶ������ܣ�I2(Cu)________(����>����<����������)I2(Zn)��
(3) SO2������Sԭ�ӵĹ���ӻ�����Ϊ________�����ӵĿռ乹��Ϊ________����SO2��Ϊ�ȵ�����ķ�����________(дһ��)��
(4) [Cu(CH3CN)4]���Ƿdz��ȶ���������ӣ���������������������֮��Ϊ________��
(5) Fe2����Fe3������CN����ϣ���ṹ��ͼ��ʾ�������ӿ��γ��������Σ��ü��εĻ�ѧʽΪ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com