
【题目】锶(Sr)为第5周期ⅡA族元素。高纯六水氯化锶晶体(SrCl2.6H2O)具有很高的经济价值,61℃时晶体开始失去结晶水,100℃时失去全部结晶水。用工业碳酸锶粉末(含少量Ba、Fe的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。

请回答:
(1)常温下,氯化锶溶液pH___ 7(填“大于”、“等于”或“小于”);
(2)写出步骤②在浆液中加入盐酸时发生反应的离子方程式 ___;
(3)步骤③所得滤渣的主要成分是____(填化学式),调节溶液pH至8~10,宜选用的试剂为 ___。
A.稀硫酸 B.氢氧化锶粉末 C.氢氧化钠 D.氧化锶粉末
(4)步骤⑤中,洗涤氯化锶晶体最好选用____。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
(5)工业上用热风吹干六水氯化锶,选择的适宜温度范围是____(填字母)。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(6)若滤液中Ba2+浓度为1×10-6 mol/L,依据下表数据可以推算滤液中Sr2+物质的量浓度为 ________。

【答案】 等于 SrCO3+2H+═Sr2++H2O+CO2↑ BaSO4、Fe(OH)3 BD D A 0.003mol/L
【解析】(1)同主族元素最外层电子数相同,自上而下电子层数增多,元素的金属性增强;所以Sr金属性比钙强,氯化钙溶液显中性,所以氯化锶溶液也显中性,pH=7,故答案为:等于;
(2)碳酸锶与盐酸反应生成氯化锶、水、二氧化碳.碳酸锶不溶于水,氯化锶易溶于水.反应离子方程式为:SrCO3+2H+═Sr2++H2O+CO2↑,故答案为:SrCO3+2H+═Sr2++H2O+CO2↑;
(3)由于前面加入了稀硫酸故有硫酸钡生成,所以沉淀有两种即BaSO4、Fe(OH)3;调节pH除去Fe3+等,要不能引入杂质,最好选用氢氧化锶粉末或氧化锶粉末;故答案为:BaSO4、Fe(OH)3;BD;
(4)为了减少氯化锶溶解,所以用氯化锶饱和溶液洗涤晶体,故答案为:D;
(5)由题中信息可知热风吹干六水氯化锶时温度不能太高,当高于61℃时晶体会失去结晶水,故选A;
(6)滤液中Ba2+浓度为1×10-6molL-1,则c(SO42-)= =
=![]() =1.1×10-4mol/L;所以滤液中Sr2+物质的量浓度为c(Sr2+)=
=1.1×10-4mol/L;所以滤液中Sr2+物质的量浓度为c(Sr2+)= =
=![]() =0.003mol/L,故答案为:0.003mol/L。
=0.003mol/L,故答案为:0.003mol/L。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某酸性溶液中只有Na+、CH3COO﹣、H+、OH﹣四种离子.则下列描述正确的是
A. 该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B. 该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C. 加入适量NaOH,溶液中离子浓度为c(CH3COO﹣)>c(Na+ )>c(OH﹣)>c(H+)
D. 加入适量氨水,c(CH3COO﹣)一定大于c(Na+)、c(NH4+)之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学设计如图装置:


回答下列问题:
(1)乙中铜片为________极 (填“正”或“负”),其电极反应式为________。
(2)一段时间后,将甲和乙两池溶液混合,加入H2O2和一定量稀硫酸后,有Fe(OH)3沉淀出现,但没有Cu(OH)2沉淀出现,此时溶液中c(Fe3+)=2.6×10-18 mol·L-1,求溶液中Cu2+的最大物质的量浓度________。(写出计算步骤)(已知2Fe2++H2O2+2H+=2Fe3++2H2O,Ksp[Fe(OH)3]=2.6×10-39,Ksp[Cu(OH)2]=2.2×10-20)。
(3)丙中电源的A极为________极(填“正”或“负”)。
(4)若丙池盛放足量的CuSO4溶液:
①在丙池铁棒这极的现象是________。
②在丙池中阳极的电极反应是________。
(5)若丙池中盛放滴加少量酚酞的足量的饱和NaCl溶液1L(假设溶液体积电解前后无变化)。
①丙池通电一段时间后,________极附近溶液呈红色(填Fe或C),总反应的离子方程式:________。
②25℃时,当丙池中有0.1mol电子发生转移时切断电源,则理论上标准状况下共有________ L气体生成。此时溶液的pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组制取氯气并进行氯气的性质实验,其装置如图所示,回答下列问题:
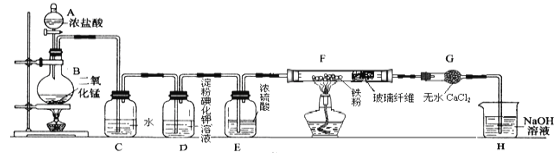
(1)仪器A的名称是 ______,实验中制备氯气的反应方程式为 ____________________。
(2)C中发生反应的化学方程式为 ______ .若将干燥的有色布条放入C中,观察到的现象是 ______,原因是 ___________________________。
(3)实验中观察到D溶液变蓝色,查资料得知淀粉碘化钾溶液是淀粉和碘化钾(KI)的混合溶液,写出D装置中发生反应的离子方程式______________________。
(4)F中氯气与铁粉反应制备无水三氯化铁,查资料知该化合物呈棕红色、易吸水潮解, 100℃左右时升华.双通管F中玻璃纤维(不参与反应)的作用是 ______ ;在F和H装置之间安装G装置的目的是____。
(5)H中NaOH溶液的作用是 _______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下.有浓度均为0.1 mol·L-l的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液

(1)这4种溶液pH由大到小的顺序是____(填序号),其中②由水电离的H+浓度为____。
(2)①中各离子浓度由大到小的顺序是 ___。
(3)④的水解平衡常数Kh=___mol/L。
(4)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③___ ④(填“>”、“<"、“=”)
(5)25℃时,测得HCN和NaCN的混合溶液的pH=11,则![]() 约为____。向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:____。
约为____。向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下实验。实验装置如图所示(已知NO、NO2能与NaOH溶液反应):

(1)设计装置A的目的是________________________________________,为达此目的应进行的操作____________________________________________________________________________;A中反应的化学方程式是_________________________________________________________。
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是_______;B中反应的离子方程式是_________________________________________________________。
(3)装置E和F的作用是__________________________________________________________,为实现此目的,操作方法是_______________________________________________________。
(4)D装置的作用是_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;④将得到的产物熔融电解得到镁。下列说法不正确的是
A. 此法的优点之一是原料来源丰富
B. ①②③步骤的目的是从海水中获取MgCl2
C. 第④步电解得到,镁的方程式为MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
D. 提取镁的过程涉及化合、分解、置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述不正确的是
A. 25 ℃、1.01×105 Pa时,44 g CO2中含有的氧原子数为2NA
B. 3.2g由O2和O3组成的混合物中含有的原子数目为0.2NA
C. 在过氧化钠与水的反应中,每消耗0.1mol过氧化钠,转移电子的数目为0.1NA
D. 在KClO3+6HCl(浓) ===KCl+3Cl2↑+3H2O反应中,若产生标准状况下6.72LCl2时,转移电子数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组做完高温下铁与水蒸气反应的实验后得到一种黑色粉末。他们为探究该黑色粉末中是否有未反应完的铁粉,又进行了如下实验,装置如图1所示。请回答下列问题:
(1)铁与水蒸气反应的化学方程式是_____________________;
(2)按图1连接好仪器后,检查装置的气密性的操作方法是_______________;
(3)仪器b的名称是_____,往仪器b中加入的试剂可能是______(填一种);
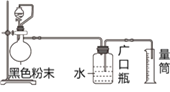
(4)实验中观察到烧瓶中有气泡产生,则黑色粉末中_______(填“有”或“无”)铁粉,产生气泡的离子方程式是________________________;
(5)如果黑色粉末的质量为w g,当时实验条件下产生的气体的密度为ρg/cm3 ,多次试验求出量筒中液体平均体积为a mL,则黑色粉末中铁的氧化物的质量分数为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com