
【题目】过氧化钙晶体(CaO2·8H2O)常温下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
⑴过氧化钙晶体可用下列方法制备:CaCl2+H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4Cl。
用如下制取装置制备过氧化钙晶体。

①装置A中发生反应的化学方程式为______。
②仪器X的名称为______;Y是______。
③为提高CaO2·8H2O产率,装置B的温度需控制在0℃,可采取的方法是______。
⑵测定产品中CaO2·8H2O含量的实验步骤如下:
步骤一:准确称取0.5000 g产品于有塞锥形瓶中,加入适量蒸馏水和过量的KI晶体,再滴入2 mol·L—1的硫酸溶液,充分反应。
步骤二:向上述锥形瓶中加入几滴淀粉溶液,逐滴加入浓度为0.200 mol·L—1的Na2S2O3溶液至反应完全,滴定至终点,消耗Na2S2O3溶液体枳为20.00 mL。求产品中CaO2·8H2O的质量分数。(写出计算过程)_____________
已知:CaO2·8H2O+2KI+2H2SO4=CaSO4+2K2SO4+I2+10H2O
I2+2S2O32-=2I-+ S4O62-
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 分液漏斗 稀硫酸 将装置B置于冰水浴中 n(Na2S2O3)=0.200 mol·L-1×20.00 mL×10﹣3=0.004 mol,由关系式“CaO2·8H2O~I2~2S2O32-”可知,n(CaO2·8H2O)= 0.5×0.004mol=0.002 mol,m(CaO2·8H2O)=0.002mol×216g·mol-1=0.432 g,则样品中CaO2·8H2O的质量分数为:ω(CaO2·8H2O)=
CaCl2+2NH3↑+2H2O 分液漏斗 稀硫酸 将装置B置于冰水浴中 n(Na2S2O3)=0.200 mol·L-1×20.00 mL×10﹣3=0.004 mol,由关系式“CaO2·8H2O~I2~2S2O32-”可知,n(CaO2·8H2O)= 0.5×0.004mol=0.002 mol,m(CaO2·8H2O)=0.002mol×216g·mol-1=0.432 g,则样品中CaO2·8H2O的质量分数为:ω(CaO2·8H2O)= ![]() =86.4%。
=86.4%。
![]()
【解析】
根据装置图可知,A是用氯化铵与氢氧化钙加热制氨气,据此书写化学方程式;根据仪器的结构和性能确定仪器X的名称;利用反应Ca2++H2O2+2NH3+8H2O═CaO28H2O↓+2NH4+,在碱性环境下制取CaO2,常用冰水浴控制温度在0℃左右,其可能的原因为:温度低可减少过氧化氢的分解,提高过氧化氢的利用率,该反应是放热反应,温度低有利于提高CaO28H2O产率;根据反应的离子方程式:CaO2+4H++2I-═Ca2++2H2O+I2,I2+2S2O32-→2I-+S4O62-,可得关系式“CaO2·8H2O~I2~2S2O32-”,并以此进行计算。
(1)①根据装置图可知,A是用氯化铵与氢氧化钙加热制氨气,反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
②仪器X为分液漏斗,Y是稀硫酸,用于吸收挥发出来的氨气;故答案为:分液漏斗;稀硫酸;
③装置B的温度需控制在0℃,可采取的方法是将装置B置于冰水浴中,故答案为:将装置B置于冰水浴中;
(2)根据反应的离子方程式:CaO2+4H++2I-═Ca2++2H2O+I2,I2+2S2O32-→2I-+S4O62-,可得关系式CaO2~2S2O32-,n(Na2S2O3)=0.200 mol·L-1×20.00 mL×10﹣3=0.004 mol,由关系式“CaO2·8H2O~I2~2S2O32-”可知,n(CaO2·8H2O)=0.5×0.004mol=0.002 mol,m(CaO2·8H2O)=0.002mol×216g·mol-1=0.432 g,则样品中CaO2·8H2O的质量分数为:ω(CaO2·8H2O)= ![]() =86.4%。
=86.4%。


科目:高中化学 来源: 题型:
【题目】一种磁性材料的磨削废料(含镍质量分数约21%)主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍,工艺流程如下:
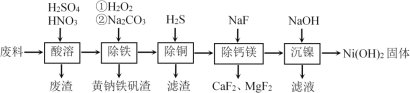
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有N2生成。写出金属镍溶解的离子方程式________________________。
(2)“除铁”时H2O2的作用是____________________,为了证明添加的H2O2已足量,应选择的试剂是____________________(填“铁氰化钾”或“硫氰化钾”)溶液。黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点,则x∶y∶m∶n=1∶3∶2∶________。
(3)“除铜”时,反应的离子方程式为_________________________,若用Na2S或Na2S2O3代替H2S除铜,优点是__________________________。
(4)已知除杂过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是_______________________________。
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31kg,则镍回收率的计算式为_______。
(6)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2![]() HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式________。
HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸具有止血功效, 存在于多种中药中, 其结构简式如下图, 则下列有关说法正确的是
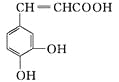
A. 该物质苯环上的一氯代物有2种
B. 1 mol该物质可以与1.5 mol碳酸钠溶液反应生成1.5 mol的CO2
C. 既能发生取代反应, 也能发生加成反应
D. 所有碳原子不可能都在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于分子式为C4H8O2的有机物的同分异构体的说法中,不正确的是( )
A. 属于酯类的有4种
B. 属于羧酸类的有2种
C. 既含有羟基又含有醛基的有3种
D. 存在分子中含有六元环的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应属于取代反应的是
A.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
B.nCH2=CH2![]()
![]()
C.2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下所示
(提出猜想)
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被H2、CO还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
(实验探究)
I.解决问题1
(1)需用到的药品除1mol L-1 CuSO4溶液、稀硫酸外,还需_________(填试剂的化学式)溶液。
(2)用胆矾晶体配制1molL-1 CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、玻璃棒、胶头滴管、量简外,还有________(填仪器名称)。
(3)为达到实验目的,你认为应进行哪些相关实验?
实验内容和步骤:①_________;②_______________。
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃时得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答冋题:
(1)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:_____________。
(2)从实验Ⅱ可得出的结论是_______________________。
Ⅲ.解决问题3
设计如下装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水CuSO4变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的CuO燃烧管完全反应后,消耗0.01molX,测得B装置增重0.36g,并收集到0.28g单质气体Y。
(1)X气体的摩尔质量是_________________。
(2)C装置中发生反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,氢氟酸电离常数Ka=6.8×10-4mol·L-1,醋酸电离常数Ka=1.8×10-5mol·L-1。如图表示25℃时氟化钠和醋酸钠溶液的浓度和Y的关系。则Y可以表示( )

A.溶液的pHB.水解平衡常数
C.水解百分率D.溶液中阴离子浓度之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
①N2O4的消耗速率与NO2的生成速率之比为1∶2;②NO2的生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧
C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀硫酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在O2中的燃烧反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com