
ЎҫМвДҝЎҝПВБРКЗІҝ·Ц¶МЦЬЖЪЦРөЪ¶юЎўөЪИэЦЬЖЪФӘЛШөДФӯЧУ°лҫ¶ј°ЦчТӘ»ҜәПјЫЎЈ
ФӘЛШҙъәЕ | ўЩ | ўЪ | ўЫ | ўЬ | ўЭ | ўЮ | ўЯ | ўа |
ФӯЧУ°лҫ¶ЈЁnmЈ© | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
ЦчТӘ»ҜәПјЫ | Ј«1 | Ј«2 | Ј«1 | Ј«3 | Ј«5ЎўЈӯ3 | Ј«7ЎўЈӯ1 | Ј«5ЎўЈӯ3 | Јӯ2 |
»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ўаФЪФӘЛШЦЬЖЪұнЦРөДО»ЦГКЗЈЁЦЬЖЪЎўЧеЈ© Ј»
ЈЁ2Ј©8ёцФӘЛШөДЧоёЯјЫСх»ҜОпөДЛ®»ҜОпЦРЈ¬ЛбРФЧоЗҝөДКЗ ЈЁМо»ҜС§КҪЈ©Ј»
ЈЁ3Ј©ФӘЛШўЭЎўўЯЎўўа·ЦұрРОіЙөДјтөҘЖшМ¬Зв»ҜОпЦРЈ¬ўЯөДөзЧУКҪОӘ Ј¬ОИ¶ЁРФЧоЗҝөДЗв»ҜОпөДҪб№№КҪОӘ Ј»
ЈЁ4Ј©РҙіцўЩЎўўЬөДЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпЦ®јд·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪ Ј»
ЈЁ5Ј©УГөзЧУКҪұнКҫФӘЛШўЩУлўЮРОіЙ»ҜәПОпөД№эіМ ЎЈ
Ўҫҙр°ёЎҝЈЁ1Ј©өЪ¶юЦЬЖЪөЪўцAЧе ЈЁ2Ј©HClO4 ЈЁ3Ј©![]() Ј¬ HЈӯOЈӯH
Ј¬ HЈӯOЈӯH
ЈЁ4Ј© AlЈЁOHЈ©3 + OH--="=" AlO2--+ 2H2O ЈЁ5Ј©
ЎҫҪвОцЎҝКФМв·ЦОцЈәёщҫЭФӘЛШФӯЧУ°лҫ¶әНЦчТӘ»ҜәПјЫҝЙЦӘЈ¬ўЩЎ«ўаФӘЛШ·ЦұрКЗNaЎўMgЎўLiЎўAlЎўPЎўClЎўNЎўOЎЈ
ЈЁ1Ј©СхФӘЛШФЪФӘЛШЦЬЖЪұнЦРөДО»ЦГКЗөЪ¶юЦЬЖЪөЪўцAЧеЎЈ
ЈЁ2Ј©·ЗҪрКфРФФҪЗҝЈ¬ЧоёЯјЫСх»ҜОпөДЛ®»ҜОпөДЛбРФФҪЗҝЈ¬ФтФЪХв8ЦЦФӘЛШөДЧоёЯјЫСх»ҜОпөДЛ®»ҜОпЦРЈ¬ЛбРФЧоЗҝөДКЗHClO4ЎЈ
ЈЁ3Ј©ФӘЛШўЭЎўўЯЎўўа·ЦұрРОіЙөДјтөҘЖшМ¬Зв»ҜОпЦРЈ¬ўЯКЗ°ұЖшЈ¬өзЧУКҪОӘ![]() Ј»·ЗҪрКфРФФҪЗҝЈ¬Зв»ҜОпФҪОИ¶ЁЈ¬ФӘЛШўЭЎўўЯЎўўаЦРСхФӘЛШ·ЗҪрКфРФЧоЗҝЈ¬ФтОИ¶ЁРФЧоЗҝөДЗв»ҜОпКЗЛ®Ј¬Ҫб№№КҪОӘHЈӯOЈӯHЎЈ
Ј»·ЗҪрКфРФФҪЗҝЈ¬Зв»ҜОпФҪОИ¶ЁЈ¬ФӘЛШўЭЎўўЯЎўўаЦРСхФӘЛШ·ЗҪрКфРФЧоЗҝЈ¬ФтОИ¶ЁРФЧоЗҝөДЗв»ҜОпКЗЛ®Ј¬Ҫб№№КҪОӘHЈӯOЈӯHЎЈ
ЈЁ4Ј©ўЩЎўўЬөДЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОп·ЦұрКЗЗвСх»ҜДЖәНЗвСх»ҜВБЈ¬¶юХЯЦ®јд·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘAlЈЁOHЈ©3 + OH--="=" AlO2--+ 2H2OЎЈ
ЈЁ5Ј©ФӘЛШўЩУлўЮРОіЙ»ҜәПОпКЗАлЧУ»ҜәПОпВИ»ҜДЖЈ¬ЖдРОіЙ№эіМҝЙұнКҫОӘ ЎЈ
ЎЈ


 И«ДЬБ·ҝјҫнПөБРҙр°ё
И«ДЬБ·ҝјҫнПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРУР»ъОпөДГьГыХэИ·өДКЗ
AЈ®2Ј¬2-¶юјЧ»щОмНй
BЈ®1-јЧ»щұыНй
CЈ®2-ТТ»щОмНй
DЈ®2-јЧ»щ-3-¶ЎП©
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР№ШУЪNH4+ЎўNH3ЎўNH2-ИэЦЦОўБЈөДЛө·ЁІ»ХэИ·өДКЗ
AЈ®ИэЦЦОўБЈЛщә¬УРөДөзЧУКэПаөИ
BЈ®ИэЦЦОўБЈЦРөӘФӯЧУөДФУ»Ҝ·ҪКҪПаН¬
CЈ®ИэЦЦОўБЈөДҝХјд№№РНПаН¬
DЈ®јьҪЗҙуРЎ№ШПөЈәNH4+ЈҫNH3ЈҫNH2-
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР»ҘОӘН¬О»ЛШөДКЗЈЁ Ј©
A. H2D2 B. 14N14C C. 16O17O D. O2O3
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДі»ҜәПОпAөДҪб№№јтКҪОӘ![]() Ј¬ОӘБЛСРҫҝXөДҪб№№Ј¬Ҫ«»ҜәПОпAФЪТ»¶ЁМхјюПВЛ®ҪвЦ»өГөҪB(·ЦЧУКҪОӘC8H8O3)әНC(·ЦЧУКҪОӘC7H6O3)ЎЈCУцFeCl3Л®ИЬТәПФЧПЙ«Ј¬УлNaHCO3ИЬТә·ҙУҰУРCO2ІъЙъЎЈ
Ј¬ОӘБЛСРҫҝXөДҪб№№Ј¬Ҫ«»ҜәПОпAФЪТ»¶ЁМхјюПВЛ®ҪвЦ»өГөҪB(·ЦЧУКҪОӘC8H8O3)әНC(·ЦЧУКҪОӘC7H6O3)ЎЈCУцFeCl3Л®ИЬТәПФЧПЙ«Ј¬УлNaHCO3ИЬТә·ҙУҰУРCO2ІъЙъЎЈ
Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©»ҜәПОпAөД·ЦЧУКҪ ЎЈ
ЈЁ2Ј©»ҜәПОпBДЬ·ўЙъПВБР·ҙУҰАаРНөДУР________ЎЈ
aЈ®ИЎҙъ·ҙУҰ bЈ®јУіЙ·ҙУҰ cЈ®ЛхҫЫ·ҙУҰ dЈ®ПыИҘ·ҙУҰ
ЈЁ3Ј©»ҜәПОпCДЬҫӯПВБР·ҙУҰөГөҪG(·ЦЧУКҪОӘC8H6O2Ј¬·ЦЧУДЪә¬УРОеФӘ»·)Ј»

ТСЦӘЈәЈЁўсЈ©RCOOH![]() RCH2OHЈ»
RCH2OHЈ»
ЈЁўтЈ©ҫӯКөСйІв¶ЁЦРјдЙъіЙОпEУцFeCl3ПФЧПЙ«Ј»
ЈЁўуЈ©RЎӘBr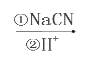 RЎӘCOOHЎЈ
RЎӘCOOHЎЈ
ўЩИ·ИП»ҜәПОпCөДҪб№№јтКҪОӘ__________________________ЎЈ
ўЪ»ҜәПОпEУР¶аЦЦН¬·ЦТм№№МеЈ¬ЖдЦРДіР©Н¬·ЦТм№№Меә¬УРұҪ»·Ј¬ЗТұҪ»·ЙПУРБҪЦЦІ»Н¬»ҜС§»·ҫіөДЗвЈ¬РҙіцХвР©Н¬·ЦТм№№МеЦРИОТвБҪЦЦөДҪб№№јтКҪЈә______________________________ЎЈ
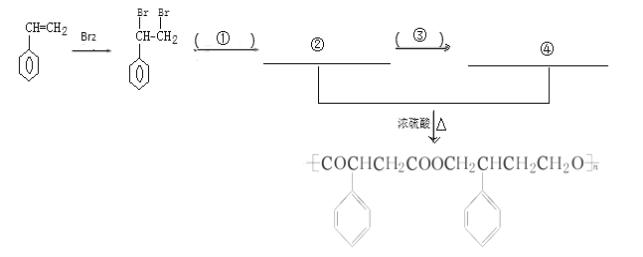
ЈЁ4Ј©НкіЙПВБРТФ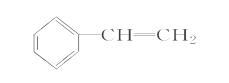 ОӘЦчТӘФӯБПЦЖұё
ОӘЦчТӘФӯБПЦЖұё
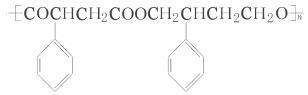 өДәПіЙВ·ПЯБчіМНј(ОЮ»ъКФјБИОСЎ)ЎЈ
өДәПіЙВ·ПЯБчіМНј(ОЮ»ъКФјБИОСЎ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝСРҫҝөӘј°Жд»ҜәПОпөДЧӘ»ҜФЪКөјК№ӨТөЙъІъЎўЙъ»оЦРҫЯУРЦШТӘөДТвТеЎЈ
ЈЁ1Ј©ТСЦӘ![]()
![]()
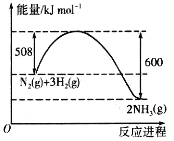
![]() өДДЬБҝұд»ҜИзНјЛщКҫЈ¬ФЪТ»¶ЁОВ¶ИПВЈ¬Пт2LөДәгИЭГЬұХИЭЖчЦРН¶Ил2.2 molN2әН2.6 mol H2Ј¬ҫӯ10 minҙпөҪЖҪәвЈ¬ІвөГ·ЕіцөДИИБҝОӘ18.4 kJЈ¬Фт
өДДЬБҝұд»ҜИзНјЛщКҫЈ¬ФЪТ»¶ЁОВ¶ИПВЈ¬Пт2LөДәгИЭГЬұХИЭЖчЦРН¶Ил2.2 molN2әН2.6 mol H2Ј¬ҫӯ10 minҙпөҪЖҪәвЈ¬ІвөГ·ЕіцөДИИБҝОӘ18.4 kJЈ¬Фт![]() ______ЎЈёГОВ¶ИПВЈ¬·ҙУҰөДЖҪәвіЈКэK=________(molЎӨL-1)-2ЎЈЖҪәвәуЈ¬ФЩПтМеПөЦРН¶Ил1.1 mol N2әН1.3 mol H2Ј¬ЦШРВҙпөҪЖҪәвәуN2өДМе»э·ЦКэ________(МоЎ°ФцҙуЎұЎ°јхРЎЎұ»тЎ°І»ұдЎұ)ЎЈ
______ЎЈёГОВ¶ИПВЈ¬·ҙУҰөДЖҪәвіЈКэK=________(molЎӨL-1)-2ЎЈЖҪәвәуЈ¬ФЩПтМеПөЦРН¶Ил1.1 mol N2әН1.3 mol H2Ј¬ЦШРВҙпөҪЖҪәвәуN2өДМе»э·ЦКэ________(МоЎ°ФцҙуЎұЎ°јхРЎЎұ»тЎ°І»ұдЎұ)ЎЈ
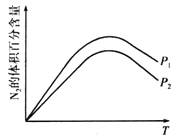
ЈЁ2Ј©АыУГігИИөД»оРФМҝҝЙТФҙҰАнNO2Ј¬·ҙУҰФӯАнОӘ![]()
![]()
![]() ЎЈ
ЎЈ
ўЩМҪҫҝОВ¶ИЎўС№Зҝ¶ФёГ·ҙУҰөДУ°ПмИзНјЛщКҫЈ¬ФтёГ·ҙУҰөД![]() ___________0(МоЎ°>ЎұЎ°<Ўұ»тЎ°=Ўұ)Ј¬P1_____________P2(МоЎ°>ЎұЎ°<Ўұ»тЎ°=Ўұ)ЎЈ
___________0(МоЎ°>ЎұЎ°<Ўұ»тЎ°=Ўұ)Ј¬P1_____________P2(МоЎ°>ЎұЎ°<Ўұ»тЎ°=Ўұ)ЎЈ
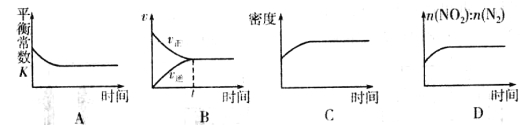
ўЪТ»¶ЁОВ¶ИПВЈ¬Ҫ«Т»¶ЁБҝөД»оРФМҝәНNO2јУИлТ»әгИЭГЬұХИЭЖчЦРЈ¬ПВБРКҫТвНјХэИ·ЗТДЬЛөГч·ҙУҰҙпөҪЖҪәвЧҙМ¬өДКЗ____________(МоРтәЕ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ»ҜС§КҪОӘC2H6OөД»ҜәПОпAҫЯУРИзПВРФЦКЈәAЈ«NaЁDЎъВэВэІъЙъЖшЕЭ
AЈ«CH3COOH![]() УРПгО¶өДІъОп
УРПгО¶өДІъОп
ЈЁ1Ј©ёщҫЭЙПКцРЕПўЈ¬¶ФёГ»ҜәПОпҝЙЧчіцөДЕР¶ПКЗ( )ЎЈ
AЈ®Т»¶Ёә¬УРЎӘOH BЈ®Т»¶Ёә¬УРЎӘCOOH CЈ®AОӘТТҙј DЈ®AОӘТТИ©
ЈЁ2Ј©ә¬AөДМе»э·ЦКэОӘ75%өДЛ®ИЬТәҝЙТФУГЧч_______________________ЎЈ
ЈЁ3Ј©AУлДЖ·ҙУҰөД»ҜС§·ҪіМКҪЈә______________________________________________ЎЈ
ЈЁ4Ј©»ҜәПОпAУлCH3COOH·ҙУҰЙъіЙөДУРПгО¶өДІъОпөДҪб№№јтКҪОӘЈә________ЎЈ
ЈЁ5Ј©РҙіцA·ЦЧУФЪҙЯ»ҜјБҙжФЪМхјюПВјУИИәНСхЖш·ҙУҰөД»ҜС§·ҪіМКҪЈә___________________ЎЈ
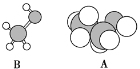
ЈЁ6Ј©ИзНјКЗB·ЦЧУөДЗт№чДЈРНәНA·ЦЧУөДұИАэДЈРНЈ¬ИфAәНBөД№ШПөКЗН¬ПөОпЈ¬ФтBөДҪб№№јтКҪ_____ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪПВБРФӘЛШЦРЈ¬І»КфУЪЦчЧеФӘЛШөДКЗЈЁ Ј©
A. p B. Fe C. Ca D. I
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝөӘЎўБЧЎўБтЎўВИЎўЙйөИКЗЕ©Т©ЦРөДЦШТӘЧйіЙФӘЛШЎЈЗл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©»щМ¬ЙйөДјЫөзЧУЕЕІјКҪКЗ___________________________Ј»
ЈЁ2Ј©°ұЖшұИPH3·РөгёЯөДФӯТтКЗ______________________Ј»
ЈЁ3Ј©ПВБРУР№ШөӘЎўБЧЎўБтЎўВИөДЛө·ЁХэИ·өДКЗ__________Ј»
aЈ®өЪТ»өзАлДЬУЙРЎөҪҙуөДЛіРтКЗSЈјPЈјCl
bЈ®PO43-ЎўSO42-ЎўClO4-»ҘОӘөИөзЧУМеЈ¬ЛьГЗөДҝХјд№№РНҫщОӘЛДГжМе
cЈ®БЧЎўБтЎўВИ»щМ¬ФӯЧУөДОҙіЙ¶ФөзЧУКэТАҙОФц¶а
dЈ®1mol(C2H5O)P=0·ЦЧУЦРә¬УРөДҰДјьөДКэДҝОӘ24ЎБ6.02ЎБ1023
ЈЁ4Ј©өӘ»ҜЕрәНБЧ»ҜЕрКЗКЬөҪёЯ¶И№ШЧўөДДНёЯОВЎўДНДҘНҝБПЈ¬БҪХЯҪб№№ПаЛЖЎЈБЧ»ҜЕрҫ§°ыҪб№№ИзНјЛщКҫЈ¬ФтБЧ»ҜЕрҫ§МеЦРГҝёцЕрФӯЧУЦЬО§ҫаАлЧоҪьөДБЧФӯЧУКэДҝОӘ__________Ј»ҫ§МеҪб№№ЦРҙжФЪөД»ҜС§јьУР_______(МоРтәЕ)Ј»

aЈ®АлЧУјьbЈ®№ІјЫјьcЈ®·ЦЧУјдЧчУГБҰdЈ®ЕдО»јь
өӘ»ҜЕрҫ§МеөДИЫөгТӘұИБЧ»ҜЕрҫ§МеёЯЈ¬ЖдФӯТт______________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com