
����Ŀ���о������仯�����ת����ʵ�ʹ�ҵ�����������о�����Ҫ�����塣
��1����֪![]()
![]()
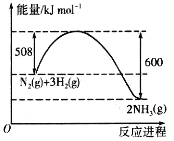
![]() �������仯��ͼ��ʾ����һ���¶��£���2L�ĺ����ܱ�������Ͷ��2.2 molN2��2.6 mol H2����10 min�ﵽƽ�⣬��÷ų�������Ϊ18.4 kJ����
�������仯��ͼ��ʾ����һ���¶��£���2L�ĺ����ܱ�������Ͷ��2.2 molN2��2.6 mol H2����10 min�ﵽƽ�⣬��÷ų�������Ϊ18.4 kJ����![]() ______�����¶��£���Ӧ��ƽ�ⳣ��K=________(mol��L-1)-2��ƽ���������ϵ��Ͷ��1.1 mol N2��1.3 mol H2�����´ﵽƽ���N2���������________(�������С�����䡱)��
______�����¶��£���Ӧ��ƽ�ⳣ��K=________(mol��L-1)-2��ƽ���������ϵ��Ͷ��1.1 mol N2��1.3 mol H2�����´ﵽƽ���N2���������________(�������С�����䡱)��
��2�����ó��ȵĻ���̿���Դ���NO2����Ӧԭ��Ϊ![]()
![]()
![]() ��
��
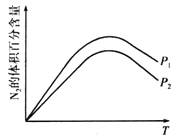
��̽���¶ȡ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ����÷�Ӧ��![]() ___________0(�>����<����=��)��P1_____________P2(�>����<����=��)��
___________0(�>����<����=��)��P1_____________P2(�>����<����=��)��
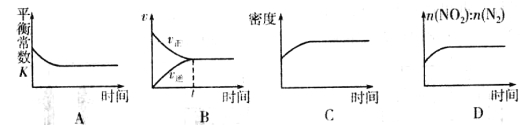
��һ���¶��£���һ�����Ļ���̿��NO2����һ�����ܱ������У�����ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����____________(�����)��
���𰸡���1��0.03mol��L-1��min-1 0.04 ��С ��2���٣� �� ��BC
��������
�����������1������ͼ���д���Ȼ�ѧ����ʽΪN2(g)+3H2(g)![]() 2NH3(g) ��H=-92kJ/mol��10 min�ﵽƽ�⣬��÷ų�������Ϊ18.4 kJ���跴Ӧ�ĵ���Ϊx mol��1:92=x:18.4�����x=0.2mol�����ݻ�ѧ����ʽ��Ӧ�������������ʵ���Ϊ0.6mol����v (H2)=0.6mol��(2L��10min)= 0.03mol��L-1��min-1 ��ƽ��ʱ�����������ʵ���Ϊ2mol�����������ʵ���Ϊ2mol�����������ʵ���Ϊ0.4mol������¶��£���Ӧ��ƽ�ⳣ��K=��0.2��0.2���£�1��13��=0.04��ƽ�����ʼ���ʵ�����0.5����������ʣ��൱������ѹǿ��ƽ�������ƶ�����ƽ����������������С��
2NH3(g) ��H=-92kJ/mol��10 min�ﵽƽ�⣬��÷ų�������Ϊ18.4 kJ���跴Ӧ�ĵ���Ϊx mol��1:92=x:18.4�����x=0.2mol�����ݻ�ѧ����ʽ��Ӧ�������������ʵ���Ϊ0.6mol����v (H2)=0.6mol��(2L��10min)= 0.03mol��L-1��min-1 ��ƽ��ʱ�����������ʵ���Ϊ2mol�����������ʵ���Ϊ2mol�����������ʵ���Ϊ0.4mol������¶��£���Ӧ��ƽ�ⳣ��K=��0.2��0.2���£�1��13��=0.04��ƽ�����ʼ���ʵ�����0.5����������ʣ��൱������ѹǿ��ƽ�������ƶ�����ƽ����������������С��
��2���ٸ���ͼ�������¶ȣ�����������ٷֺ�����С��˵��ƽ�������ƶ����������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ������Ϊ���ȷ�Ӧ��![]() <0���÷�Ӧ�������������Ŀ��淴Ӧ������ѹǿ��ƽ�������ƶ�������������ٷֺ�����С������P1<P2��
<0���÷�Ӧ�������������Ŀ��淴Ӧ������ѹǿ��ƽ�������ƶ�������������ٷֺ�����С������P1<P2��
��A���¶Ȳ��䣬ƽ�ⳣ�����䣬A�����B����V (��)=V (��)ʱ��Ӧ�ﵽƽ��״̬��B����ȷ��C���ں��������У����ŷ�Ӧ�Ľ��У�������������������ܶ�Ҳ���������ܶȺ㶨����ʱ��Ӧ�ﵽƽ��״̬��C����ȷ��D�����ŷ�Ӧ�Ľ��У�NO2�����ʵ������ϼ��٣�N2�����ʵ����������ӣ�n(NO2):n(O2)���ϼ�С���ǵݼ����ߣ���ͼ����D�����ѡBC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ���ʵ�˵����ȷ����
A��Һ̬HCl�����磬����HCl���ǵ����
B��NH3����ˮ�γɵ���Һ�ܵ��磬����NH3�ǵ����
C��ϡ�����ܵ��磬����ϡ�����ǵ����
D��BaSO4��ˮ��Һ���ѵ��磬������״̬���ܵ��磬����BaSO4�ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)+B(g) ![]() C(g)+D(g)�����е������仯��ͼ��ʾ���ش��������⡣
C(g)+D(g)�����е������仯��ͼ��ʾ���ش��������⡣
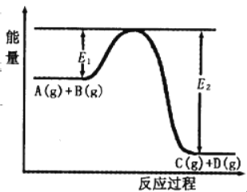
��1���÷�Ӧ��______��Ӧ������ȡ������ȡ�����
��2������Ӧ��ϵ�м����������Ӧ��������E1��E2�ı仯�ǣ�E1______��E2______���������С���������䡱����
��3����Ӧ��ϵ�м�������Է�Ӧ���Ƿ���Ӱ�죿______����������������������ԭ����_______________��
��4������Ӧ�ķ�Ӧ����H=__________kJ/mol������E1��E2��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ����ʽΪ___ ___�����÷�Ӧ6NO2+8NH3��7N2+12H2OҲ���Դ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______L��
��2����֪��2SO2(g)+O2(g) ![]() 2SO3(g) ��H= -196.6kJ/mol
2SO3(g) ��H= -196.6kJ/mol
2NO(g)+O2(g) ![]() 2NO2(g) ��H= -113.0kJ/mol
2NO2(g) ��H= -113.0kJ/mol
��ӦNO2(g)+SO2(g) ��SO3(g)+NO(g)����H=______kJ/mol��
��3������ͼ��ʾ����ͬ�����a��b��c���ܱ�����������c������һ������a��b������Ϊ������������ʼ���������ж�������ͬ����SO2��O2ʹ������ѹǿ��ȣ�һ�������·���2SO2(g)+O2(g) ![]() 2SO3(g)�ķ�Ӧ���ʣ�
2SO3(g)�ķ�Ӧ���ʣ�
����ʼa��c�������ķ�Ӧ���ʴ�С��ϵΪVa_____Vc����������������������������ͬ��
����Ӧһ��ʱ���a��c�����ʴ�С��ϵΪVa_____Vc��
������ʼ��a��c��������ͨ��������He�����ʱ��������ʼѹǿΪPa_____Pb_____Pc����ʼ��Ӧ���ʹ�ϵΪVa_____Vb_____Vc��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Dz��ֶ������еڶ�����������Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼۡ�
Ԫ�ش��� | �� | �� | �� | �� | �� | �� | �� | �� |
ԭ�Ӱ뾶��nm�� | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
��Ҫ���ϼ� | ��1 | ��2 | ��1 | ��3 | ��5����3 | ��7����1 | ��5����3 | ��2 |
�ش��������⣺
��1������Ԫ�����ڱ��е�λ���ǣ����ڡ��壩 ��
��2��8��Ԫ�ص�����������ˮ�����У�������ǿ���� ���ѧʽ����
��3��Ԫ�������������ֱ��γɵļ���̬�⻯���У����ĵ���ʽΪ ���ȶ�����ǿ���⻯��ĽṹʽΪ ��
��4��д��������������������Ӧ��ˮ����֮�䷢����Ӧ�����ӷ���ʽ ��
��5���õ���ʽ��ʾԪ���������γɻ�����Ĺ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2��CO��NO���dz����Ĵ�����Ⱦ�
��1����ҵ�ϳ���SO2��ȥCO��������ΪS��CO2����֪��S(s)+O2(g)=SO2(g) ![]() H=a kJmol-1
H=a kJmol-1
CO(g)+ ![]() O2(g)=CO2(g)
O2(g)=CO2(g) ![]() H=b kJmol-1��ӦSO2(g)+2CO(g)=S(s)+2CO2(g)��
H=b kJmol-1��ӦSO2(g)+2CO(g)=S(s)+2CO2(g)��![]() H= kJmol-1��
H= kJmol-1��
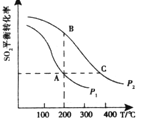
��2��������������ͬ���ܱ������з�����Ӧ��2SO2(g)+O2(g)![]() 2SO3(g)���ֱ���SO2��ƽ��ת�����ڲ�ͬѹǿ���¶��µı仯��������ͼ��ʾ����A��B�����Ӧ�ķ�Ӧ���ʣ�
2SO3(g)���ֱ���SO2��ƽ��ת�����ڲ�ͬѹǿ���¶��µı仯��������ͼ��ʾ����A��B�����Ӧ�ķ�Ӧ���ʣ�![]() (�>������<����=��)��
(�>������<����=��)��
��B��C�����Ӧ�Ļ�ѧƽ�ⳣ����![]() (�>������<����=��)��
(�>������<����=��)��
��3��25��ʱ����100mL0.1mol��L-1��NaOH��Һ����SO2������Һ��![]() ʱ����Һ��_______��(��ᡱ�����С��)����Һ��
ʱ����Һ��_______��(��ᡱ�����С��)����Һ��![]() __________mol��L-1��(��֪��H2SO3�ĵ���ƽ�ⳣ��Kal=1��10-2mol��L-1��Ka2=2��10-7mol��L-1)
__________mol��L-1��(��֪��H2SO3�ĵ���ƽ�ⳣ��Kal=1��10-2mol��L-1��Ka2=2��10-7mol��L-1)
��4�����NO2�Ʊ�NH4NO3���乤��ԭ������ͼ��ʾ��

�������缫��ӦʽΪ________________________��
��Ϊʹ������ȫ��ת��ΪNH4NO3���貹������A����A�Ļ�ѧʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ĿǰӦ����㷺�Ľ������ϣ��˽������ʴ��ԭ�����������������Ҫ���壬�Ը�����Ʒ���п���ʴ���������ʵ��ӳ���ʹ��������
��1������ʴ����ǰ�������г��������������⡣�ֽ�һ����������������������У��������������Һ�з����Ļ��Ϸ�Ӧ�Ļ�ѧ����ʽΪ__________________��
��2��������ͼװ�ã�����ģ�����ĵ绯ѧ������
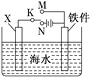
����XΪ̼����Ϊ���������ĸ�ʴ������KӦ����________________����
����XΪп������K����M�����õ绯ѧ��������Ϊ__________��
��3��ͼ����XΪ��ͭ�������к�ˮ�滻Ϊ����ͭ��Һ������K����N����һ��ʱ���������������3.2 gʱ��X�缫�ܽ��ͭ������____3.2 g(����<����>����������)��
��4��ͼ����XΪͭ�������к�ˮ�滻ΪFeCl3��Һ������K����M����ͭ�缫�����ķ�Ӧ��______________________����������K����N�����������ܷ�Ӧ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣��ԭ��Ϊ��
N2(g)��3H2(g)![]() 2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
�ݴ˻ش��������⣺
��1���ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��________��
�ڸ����¶ȶԻ�ѧƽ���Ӱ����ɿ�֪�����ڸ÷�Ӧ���¶�Խ�ߣ���ƽ�ⳣ����ֵԽ________��
��2��ij�¶��£�����1 mol N2��3 mol H2�������Ϊ1L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ����û�������а����������Ϊ1/3������¶��·�Ӧ��K�ļ���ʽ��________(�÷�����ʾ)����˵���÷�Ӧ�ﵽ��ѧƽ��״̬����________(����ĸ)��
a�������ڵ��ܶȱ��ֲ���
b��������ѹǿ���ֲ���
c��v��(N2)��2v��(NH3)
d�����������c(NH3)����
��3�����ںϳɰ���Ӧ���ԣ������й�ͼ��һ����ȷ����(ѡ�����)________��

��4����ͬ�¶��£��к����ܱ�����A�ͺ�ѹ�ܱ�����B���������о�����1 mol N2��3 mol H2����ʱ�������������ȡ���һ�������·�Ӧ�ﵽƽ��״̬��A��NH3���������Ϊa���ų�����Q1 kJ��B��NH3���������Ϊb���ų�����Q2 kJ����a________b(�>������������������ͬ)��Q1________Q2��Q1________92.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ھ��������˵����ȷ���ǣ� ��
A. ֻҪ���н��������ӵľ����һ�������Ӿ���
B. ���Ӿ�����һ��������������
C. �ڹ��ۻ���������и�ԭ�Ӷ��γ�8���ӽṹ
D. ���Ӿ�����۵㲻һ���Ƚ��������۵��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com