
【题目】已知下列热化学方程式:
①CaCO3(s)═CaO+CO2(g)△H=+177.7kJ
②C(s)+H2O(s)═CO(g)+H2(g)△H=﹣131.3kJmol﹣1
③ ![]() H2SO4(1)+NaOH(1)═
H2SO4(1)+NaOH(1)═ ![]() Na2SO4(1)+H2O(1)△H=﹣57.3kJmol﹣1
Na2SO4(1)+H2O(1)△H=﹣57.3kJmol﹣1
④C(s)+O2(g)═CO2(g)△H=﹣393.5kJmol﹣1
⑤CO(g)+ ![]() O2(g)═CO2(g)△H=﹣283kJmol﹣1
O2(g)═CO2(g)△H=﹣283kJmol﹣1
⑥HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(1)△H=﹣57.3kJmol﹣1
⑦2H2(g)+O2(g)═2H2O(1)△H=﹣517.6kJmol﹣1
(1)上述热化学方程式中,不正确的有 , 不正确的理由分别是
(2)根据上述信息,写出C转化为CO的热化学方程式: .
(3)上述反应中,表示燃烧热的热化学方程式有;表示中和热的热化学方程式有 .
【答案】
(1)①②③;①中CaO没标状态,△H单位应该为KJ/mol,②H2O的状态应为“g”,△H=+131.3KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”
(2)C(s)+ ![]() O2(g)=CO(g);△H=﹣110.5KJ/mol
O2(g)=CO(g);△H=﹣110.5KJ/mol
(3)④⑤;⑥
【解析】解:(1)根据热化学方程式的书写方法,①②③都是有错误的,错误之处分别是:①中CaO没标状态,△H单位应该为KJ/mol,②H2O的状态应为“g”,△H=+131.3KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”;所以答案是:①②③;①中CaO没标状态,△H单位应该为KJ/mol,②H2O的状态应为“g”,△H=+131.3KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”;(2)结合化学反应④⑤,利用盖斯定律,反应C(s)+ ![]() O2(g)=CO(g)是④﹣⑤得来,所以焓变△H=﹣110.5KJ/mol,所以答案是:C(s)+
O2(g)=CO(g)是④﹣⑤得来,所以焓变△H=﹣110.5KJ/mol,所以答案是:C(s)+ ![]() O2(g)=CO(g);△H=﹣110.5KJ/mol;(3)上述反应中,④⑤分别是表示C、CO燃烧热的热化学方程式,⑥表示的是中和热的热化学方程式,所以答案是:④⑤;⑥.
O2(g)=CO(g);△H=﹣110.5KJ/mol;(3)上述反应中,④⑤分别是表示C、CO燃烧热的热化学方程式,⑥表示的是中和热的热化学方程式,所以答案是:④⑤;⑥.
【考点精析】解答此题的关键在于理解燃烧热的相关知识,掌握在101kPa时1mol H2物质完全燃烧生成稳定的氧化物时所放出的能量,叫该物质的燃烧热,以及对中和热的理解,了解在稀溶液中,酸和碱发生中和反应而生成1mol H2O,这时的反应热叫做中和热.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】自来水养金鱼时,通常先将自来水日晒一段时间后,再注入鱼缸。其目的是()
A.利用紫外线杀死水中的细菌
B.提高水温,有利金鱼生长
C.增加水中氧气的含量
D.促使水中的次氯酸分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1774年瑞典化学家舍勒用软锰矿(主要成分是二氧化锰)和盐酸共热得到黄绿色气体.甲、乙两个同学分别采取上述反应原理,各制取一瓶氯气,并用其验证Cl2与水反应所得产物的性质.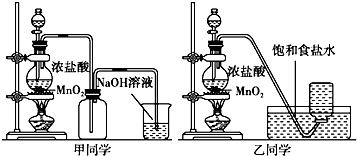
请回答:
(1)写出实验室制备氯气的化学方程式 .
(2)对于乙同学的实验装置,若要停止实验,其操作顺序是 . ①停止加热 ②取出集气瓶盖好 ③将导管伸入到烧碱溶液中
(3)甲、乙两同学分别向收集到的氯气中加入适量水,充分振荡后分成两份,均做验证氯气与水反应所得产物性质的两个实验.实验操作、现象、结论记录如下:
实验序号 | 实验操作 | 现象 | 结论 |
① | 加品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
② | 加入NaHCO2粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
请你填写下表评价甲、乙同学实验①、②的结论(填合理或不合理)
实验序号 | 甲 | 乙 |
① | ||
② |
(4)丙同学查阅资料发现HClO的氧化性大于MnO2 , 拟用下列四组试剂在实验室制取氧气A.CaC12和次氯酸B.浓盐酸NaClO
C.浓盐酸和次氯酸 D.固体NaCl、固体NaClO和浓硫酸
你认为上述四种试剂中组试剂符合实际,且Cl的原子利用率最高.试写出这个反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池反应原理为:Pb(s)+PbO2(s)+2H2SO4(aq) ![]() 2PbSO4(s)+2H2O(l),下列说法正确的是( )
2PbSO4(s)+2H2O(l),下列说法正确的是( )
A.放电时,负极的电极反应式为:Pb﹣2e﹣═Pb2+
B.放电时,正极得电子的物质是PbO2
C.充电时,电解质溶液中硫酸浓度减小
D.充电时,阴极的电极反应式为:PbSO4﹣2e﹣+2H2O═PbO2+4H++SO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】拟用下图所示装置制取并收集下表中的四种气体(图中夹持仪器均已略去;a、b、c表示相应仪器中加入的试剂)能达到实验目的的是( )
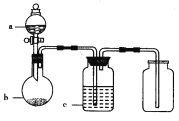
选项 | 气体 | a | b | c |
A | H2 | 稀硫酸 | 锌 | 浓硫酸 |
B | Cl2 | 浓盐酸 | MnO2 | 饱和NaCl溶液 |
C | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 |
D | NO | 稀硝酸 | 铜 | 浓硫酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数据中合理的是
A.用10 mL量筒量取7.13 mL稀盐酸
B.用托盘天平称量25.20 g NaCl
C.用广范pH试纸测得某溶液的pH为2.3
D.用25 mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列实验方法合理的是________。
A.用加热法除去碳酸钠固体中的碳酸氢钠
B.将碘的饱和水溶液中的碘提取出来,可用酒精进行萃取
C.实验室制取Al(OH)3:向AlCl3溶液中加入NaOH溶液至过量
D.向FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质
(2)某研究性学习小组为研究氯气是否具有漂白性,设计如图所示实验装置。试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液。
① 在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的________。
② B中的液体为____________,其作用为_________________________________。
③ A、C中有色布条的颜色变化分别为__________________________________,A、C的实验现象说明氯气是否具有漂白性?________(填“是”或“否”)。
④ D中NaOH溶液的作用是_______________________(用离子方程式说明)。
⑤ 将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去。小组内有甲、乙两种意见:
甲:氯气溶于水后溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色。
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则 ________(填“甲”或“乙”)的意见正确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.使用催化剂能够降低化学反应的反应热△H
B.HCl和NaOH反应的中和热△H=﹣57.3 kJ/mol,则H2SO4和NH3H2O反应的中和热△H=2×(﹣57.3)kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)的△H=+2×283.0 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com