
【题目】按要求填写下列空格
(1)同温同压下,有0.3molO2与0.2molO3 , 它们的质量之比为 , 它们所含的原子数之比为 , 它们的体积之比为 , 它们的密度之比为 .
(2)由 ![]() H和
H和 ![]() O构成的水摩尔质量为 , 10g该水分子的物质的量为 , 含中子mol.
O构成的水摩尔质量为 , 10g该水分子的物质的量为 , 含中子mol.
(3)实验室需要0.1molL﹣1 NaOH溶液480mL.根据溶液的配制情况回答下列问题:根据计算用托盘天平称取NaOH的质量为g.在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度0.1molL﹣1(填“大于”“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度0.1molL﹣1 .
【答案】
(1)1:1;1:1;3:2;2:3
(2)20g?mol﹣1;0.5mol;5
(3)2.0;大于;小于
【解析】解:(1)m(O2)=0.3mol×32g/mol=9.6g,m(O3)=0.2mol×48g/mol=9.6g,它们的质量之比为1:1;由n= ![]() 可知结合它们所含的原子数之比为0.3mol×2:0.2mol×3=1:1;由n=n=
可知结合它们所含的原子数之比为0.3mol×2:0.2mol×3=1:1;由n=n= ![]() 可知,它们的体积之比为0.3:0.2=3:2;由ρ=
可知,它们的体积之比为0.3:0.2=3:2;由ρ= ![]() 可知,它们的密度之比等于相对分子质量之比,为32:48=2:3,所以答案是:1:1;1:1;3:2;2:3;(2)由
可知,它们的密度之比等于相对分子质量之比,为32:48=2:3,所以答案是:1:1;1:1;3:2;2:3;(2)由 ![]() H和
H和 ![]() O构成的水摩尔质量为(1×2+18)g/mol,n=
O构成的水摩尔质量为(1×2+18)g/mol,n= ![]() =
= ![]() =0.5mol,中子的物质的量为0.5mol×10=5mol,所以答案是:20g/mol;0.5mol;5;(3)配制0.1molL﹣1 NaOH溶液480ml,由于无480mL容量瓶,故应选用500mL容量瓶,所需的氢氧化钠的物质的量n=cV=0.1mol/L×0.5L=0.05mol,质量m=nM=0.05mol×40g/mol=2.0g;定容时俯视刻度线,会导致溶液体积偏小,则浓度偏大,若NaOH溶液在转移至容量瓶时,洒落了少许,溶质损失,浓度偏小,
=0.5mol,中子的物质的量为0.5mol×10=5mol,所以答案是:20g/mol;0.5mol;5;(3)配制0.1molL﹣1 NaOH溶液480ml,由于无480mL容量瓶,故应选用500mL容量瓶,所需的氢氧化钠的物质的量n=cV=0.1mol/L×0.5L=0.05mol,质量m=nM=0.05mol×40g/mol=2.0g;定容时俯视刻度线,会导致溶液体积偏小,则浓度偏大,若NaOH溶液在转移至容量瓶时,洒落了少许,溶质损失,浓度偏小,
所以答案是:2.0;大于;小于.
【考点精析】掌握配制一定物质的量浓度的溶液是解答本题的根本,需要知道配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线.


科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1) 下图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1_______K2(填 “>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
A. 升高温度 B. 将CH3OH(g)从体系中分离
C. 使用合适的催化剂 D. 充入He,使体系总压强增大
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示

下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小 ③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(3)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列各组离子能大量共存的是( )
A.K+、Fe3+、SO ![]() 、NO3﹣
、NO3﹣
B.Cu2+、Mg2+、SO ![]() 、Cl﹣
、Cl﹣
C.Ag+、Na+、NO3﹣、Cl﹣
D.K+、Na+、CO ![]() 、OH﹣
、OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下到分析错误的是
A.酸性:HClO4>H3PO4B.离子半径:F- >Mg2+
C.阴离子还原性:Cl->S2-D.H、N、O三种元素可形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“电解质的溶液中所有阳离子所带的正电荷数与所有阴离子所带的负电荷数相等,故显电中性,常称电荷守恒”.某盐的溶液中含有Na+、Mg2+、Cl﹣、SO ![]() 四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣ 为0.4mol,则SO
四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣ 为0.4mol,则SO ![]() 物质的量为( )
物质的量为( )
A.0.1mol
B.0.3mol
C.0.5mol
D.0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是
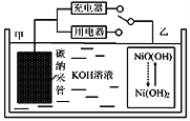
A. 放电时,乙电极反应为:Ni(OH)2+OH- e=NiO(OH)+H2O
B. 放电时,甲电极为正极,OH移向乙电极
C. 电池总反应为H2+2NiO(OH) ![]() 2Ni(OH)2
2Ni(OH)2
D. 充电时,电池的碳电极与直流电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知2NO2(红棕色)![]() N2O4(无色)可以同时相互转化,①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个__________(填“吸热”或“放热”)反应;②在一个恒温恒压容器中,通入稀有气体。颜色_______(填“变深”、“变浅”或“不变”),平衡________移动(填“正向”、“逆向”或“不”下同);③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率________(填“增大”、“减小”或“不变”),颜色_______,再通入稀有气体增大压强,平衡________移动,颜色_________。
N2O4(无色)可以同时相互转化,①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个__________(填“吸热”或“放热”)反应;②在一个恒温恒压容器中,通入稀有气体。颜色_______(填“变深”、“变浅”或“不变”),平衡________移动(填“正向”、“逆向”或“不”下同);③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率________(填“增大”、“减小”或“不变”),颜色_______,再通入稀有气体增大压强,平衡________移动,颜色_________。
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
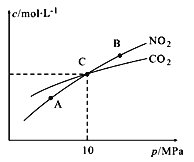
①A、B两点的浓度平衡常数关系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②A、B、C三点中NO2的转化率最高的是_____(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用碳及其化合物的性质,完成下列小题:
(1)长期存放石灰水的瓶子内会出现一层白色固体,请分析这层白色固体产生的原因(用化学方程式表示);用完石灰水后,怎样除去瓶壁上的白色固体,(用化学方程式表示).
(2)除去碳酸钠固体中少量碳酸氢钠的方法是(用化学方程式表示):
(3)向碳酸氢钠溶液滴加NaOH溶液,发生反应的离子方程式为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com