
【题目】化学与我们的生活密切相关,请回答:
(1)在生活中要注意饮食平衡,蛋白质属于_______(填序号,下同)食物,番茄属于______食物;①酸性 ②碱性
(2)有四种常见药物①阿司匹林、②青霉素、③胃舒平、④麻黄碱. 某同学胃酸过多,应该服用______(填序号,下同);从用药安全角度考虑,使用前要进行皮肤敏感性测试的是_____;由于具有兴奋作用,国际奥委会严禁运动员服用的是_________;
(3)苹果汁是人们喜爱的饮品,由于其中含有Fe2+,现榨的苹果汁在空气中会由浅绿色变为棕黄色,若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有________(填序号);①氧化性 ②还原性 ③碱性 ④酸性
(4)食用植物油进入人体后,在酶的作用下水解为高级脂肪酸和_________(写名称),进而被氧化成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料;
(5)硫酸亚铁可用于治疗缺铁性贫血,某贫血患者每天须补充1.4g铁元素,则服用的药物中含硫酸亚铁的质量至少为_________g;
(6)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(﹣NH2)和____(写结构简式或名称).人体中共有二十多种氨基酸,其中人体自身________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸;
(7)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水.写出葡萄糖在体内被氧化的化学方程式:________。
【答案】① ② ③ ② ④ ② 甘油 3.8 ﹣COOH 不能 C6H12O6+6O2![]() 6CO2+6H2O
6CO2+6H2O
【解析】
(1)食品的酸碱性与其本身的pH值无关(味道是酸的食品不一定是酸性食品),主要是食品经过消化、吸收、代谢后,最后在人体内变成酸性或碱性的物质来界定;
(2)根据药物的成分及与酸的反应来分析;青霉素属于消炎常用药物,使用前需要做皮肤敏感性测试;麻黄碱的成分含有能使人兴奋的作用来分析;
(3)根据苹果汁在空气中会由淡绿色变为棕黄色,可知铁元素的化合价升高被氧化,而加入维生素C,能使铁元素的化合价降低,并利用氧化还原反应来分析;
(4)食物油是高级脂肪酸甘油酯;
(5)先计算硫酸亚铁的含铁质量分数,然后利用铁的质量除以铁的质量分数即可求出硫酸亚铁的质量;
(6)氨基酸一定含有的官能团是氨基(-NH2)和羧基(-COOH);必需氨基酸指的是人体自身不能合成或合成速度不能满足人体需要,必须从食物中摄取的氨基酸;
(7)根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式。
(1)含钾、钠、钙、镁等矿物质较多的食物,在体内的最终的代谢产物常呈碱性,产生碱性物质的称为碱性食品,蔬菜、水果、乳类、大豆和菌类食物等;
含氮、碳、硫、氯、等元素较多的食物,经过消化形成酸根留在体内,产生酸性物质的称为酸性食品,如淀粉类;动物性食物;甜食;油炸食物或奶油类;豆类(如花生等),故答案为:①;②;
(2)因胃酸的成分为盐酸,治疗胃酸过多则选择胃舒平,因氢氧化铝与酸反应可减少盐酸;青霉素是应用广泛的抗菌药物,它本身毒性很小,而较常见的却是药物的过敏,引起不良的反应以致死亡,则使用前要进行皮肤敏感性测试;因麻黄碱是一种生物碱,能对人的中枢神经系统起兴奋作用,则国际奥委会严禁运动员服用,故答案为:③;②;④;
(3)在空气中,氧气能够把+2价铁氧化成+3价;而加入维生素C则能防止这种氧化,说明维生素C具有还原性,与三价铁发生氧化还原反应,故答案为:②;
(4)食物油是高级脂肪酸甘油酯,在酸性条件下水解生成高级脂肪酸和甘油,故答案为:甘油;
(5)硫酸亚铁中铁的质量分数是:![]() =
=![]() ,需硫酸亚铁的质量是
,需硫酸亚铁的质量是![]() =3.8g
=3.8g
故答案为:3.8;
(6)氨基酸一定含有的官能团是氨基(-NH2)和羧基(-COOH);必需氨基酸指的是人体自身不能合成或合成速度不能满足人体需要,必须从食物中摄取的氨基酸,
故答案为:-COOH;不能;
(7)葡萄糖在体内发生缓慢氧化生成二氧化碳和水,反应的化学方程式为:C6H12O6+6O2![]() 6CO2+6H2O。
6CO2+6H2O。


科目:高中化学 来源: 题型:
【题目】工业废催化剂中含有多种金属元素,某废催化剂主要含有SiO2、ZnO、ZnS和CuS,为充分利用资源,变废为宝,在实验室中探究回收废催化剂中的锌和铜,具体流程如图所示,回答下列问题:
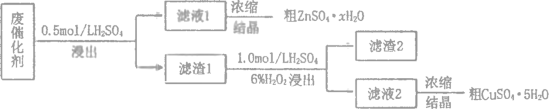
已知:ZnS与稀硫酸反应且化合价不变;CuS既不溶于稀硫酸也不与稀硫酸反应。
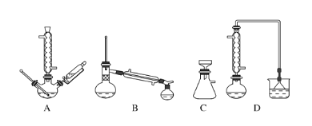
(1)下列玻璃仪器或装置中,第一次浸出时尾气净化需要使用的装置为___________(填标号),“浓缩结晶”需要使用的仪器是_______________(填名称)。
(2)滤渣1的主要成分是 ___________。
(3)第二次浸出时,向盛有滤渣1的反应器中先加入稀硫酸,后滴入过氧化氢溶液。反应器中有淡黄色沉淀生成,写出反应的离子方程式___________;若顺序相反,会造成___________。
(4)第二次浸出时需要加热且控温,采用的合适加热方式是___________。
(5)某同学在实验完成之后,得到23.3g提纯的硫酸锌晶体(ZnSO4·xH2O)。为确定晶体化学式,取5.0g晶体,用蒸馏水完全溶解.再加入足量的氯化钡溶液,充分反应后过滤、___________、___________、称重得固体4.1g,则硫酸锌晶体的化学式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
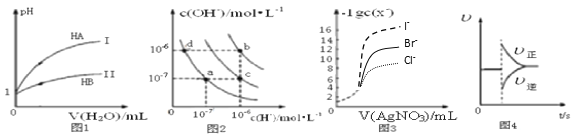
A. 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
B. 图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性
C. 用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
D. 图4表示在N2(g)+3H2(g) ![]() 2NH3(g)达到平衡后,减小NH3浓度时速率的变化
2NH3(g)达到平衡后,减小NH3浓度时速率的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲中可能含有NO、CO2、NO2、NH3、N2中的几种,将100mL气体甲经过如图所示实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
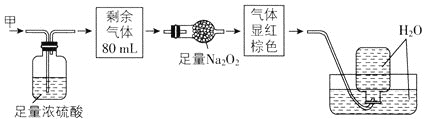
A.NO2、NH3、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物阿比朵尔具有很好的抗病毒活性,其合成路线如下:
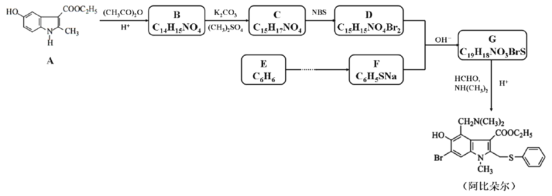
已知:①![]() +HCHO+
+HCHO+
![]()

②RX![]() RLiX
RLiX![]() RSH
RSH
请回答:
(1)下列说法正确的是___________。
A.化合物A能发生加成、取代和氧化反应,不发生还原反应
B.化合物B具有弱碱性
C.化合物D与FeCl3溶液发生显色反应
D.阿比朵尔的分子式是C22H25N2O3BrS
(2)写出化合物D的结构简式___________。
(3)写出G→阿比朵尔的化学方程式___________。
(4)设计从E→F的合成路线(用流程图表示,无机试剂任选)___________。
(5)写出化合物A同时符合下列条件的同分异构体的结构简式___________。
①1H-NMR谱和IR谱检测表明:分子中共有4种氢原子,含氮氧单键和碳氧双键;
②含有苯环和含氮五元杂环,且两环共棱连接。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是热量高、无污染的燃料,天然气储量丰富是理想的制氢原料,研究甲烷制氢具有重要的理论和现实意义。
(1)甲烷水蒸气重整制氢:CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H1=+216kJmol-1,温度1200k,压强0.2Mpa,水碳起始物质的量之比3:1,达到平衡时氢气的物质的量分数为0.3,甲烷转化率为____,Kp=____(Mpa)2 。理论上近似水碳比为____,氢气的物质的量分数将达到最大。
CO(g)+3H2(g)△H1=+216kJmol-1,温度1200k,压强0.2Mpa,水碳起始物质的量之比3:1,达到平衡时氢气的物质的量分数为0.3,甲烷转化率为____,Kp=____(Mpa)2 。理论上近似水碳比为____,氢气的物质的量分数将达到最大。
(2)①将甲烷水蒸气重整和甲烷氧化重整两种方法结合,理论上按照空气、甲烷、水蒸气约15:7:1体积比进料(空气中氧气体积分数约为0.2),可以实现反应器中能量自给(不需要补充热量)。
甲烷氧化重整制氢:2CH4(g)+O2(g)=2CO(g)+4H2(g) △H2=____kJmol-1
②实际生产中,空气、甲烷、水蒸气按照约1:1:2体积比进料,增加水蒸气的作用是____,还能发生____(用化学方程式表示)反应,从而获得更多的氢气。
(3)甲烷水蒸气重整过程中,温度1000K,原料气以57.6Kgh-1通入容积为1L镍基催化反应器中,2-5s甲烷质量分数由7.32%变为5.32%,用甲烷表示2-5s的反应速率为____molmin-1 ,随着反应的进行反应速率会急速下降,可能的原因是甲烷等高温不稳定,造成____。有人提出将甲烷水蒸气重整和甲烷氧化重整两种方法结合则能解决这个问题,原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3—CH=CH2+HBr→CH3—CHBr—CH3(主要产物),1 mol某烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下面所示的一系列变化。
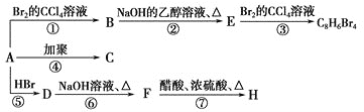
(1)A的化学式:________,A的结构简式________。
(2)上述反应中,①是________反应,⑦是________反应。(填反应类型)
(3)写出C,D,E,H物质的结构简式:
C_________,D_________,E_______,H________。
(4)写出DF反应的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO42H2O)是白色菱形结晶体,毒性较低,对环境污染污染程度低,可作新型水处理剂和金属腐蚀抑制剂。工业上利用钼精矿(主要成分是不溶于水的 MoS2)制备钼酸钠的两种途径如图所示。
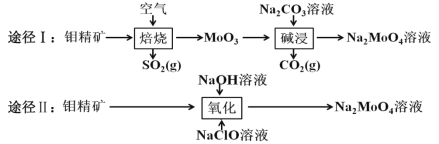
(1)途径Ⅰ焙烧过程中,为了提高焙烧效率,除增大空气量外还可以采用的措施有___; 在该过程的主要反应中,氧化剂与还原剂物质的量之比为________。
(2)途径Ⅱ氧化时还有 Na2SO4 生成,则反应的离子方程式为 ____________。
(3)已知途径Ⅰ的钼酸钠溶液中 c(MoO42-)=0.40 molL-1,c(CO32-)=0.10 molL-1。由钼酸钠溶液制备钼酸钠晶体时,需加入 Ba(OH)2 固体以除去 CO32-。在不损失 MoO42-的情况下,CO32-的最大去除率是 ____________ [已知 Ksp(BaCO3)=1×10-9、Ksp(BaMoO4)=4.0×10-8,忽略溶液的体积变化]。
(4)途径Ⅱ中 Na2MoO4 溶液通过结晶的方法可得到 Na2MoO4 晶体。母液可以循环利用,但循环一定次数后必须对母液进行处理,试解释原因 _________。
(5)途径Ⅱ比途径Ⅰ的优点有 ________________(答出两条)。
(6)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图。
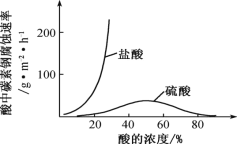
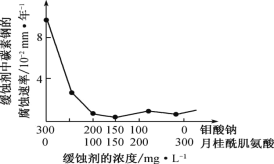
①当硫酸的浓度大于 90%时,碳素钢腐蚀速率几乎为零,原因是________________。
②若缓释剂钼酸钠-月桂酸肌氨酸总浓度为 300 mgL-1,则缓蚀效果最好时钼酸钠(M=206 gmol-1)的物质的量浓度为 ________(计算结果保留 3 位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种二次锂离子电池工作时反应为:LixCn + Li(1-x)CoO2 == LiCoO2 + nC。电池如图所示。下列说法不正确的是
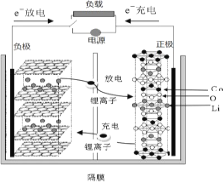
A.放电时,碳材料极失去电子,发生氧化反应,电子经外电路,Li+经内电路同时移向正极
B.放电时正极反应为: Li(1-x)CoO2 + xLi+ + xe- = LiCoO2
C.充电时, Li+从负极脱出,又嵌入正极
D.锂离子二次电池正负极之间充放电时发生传输 Li+的反应,少有副反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com