
【题目】硫单质及其化合物在工农业生产中有着吸要的应用.
(l)已知:2SO2(g)+O2═2SO3(g)△H=-196.6kJmol-1,2NO(g)+O2═2NO2(g)△H=-113.0kJmol-1.则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H= _________;
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料.已知As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O.当生成H3AsO4的物质的量为0.6mol,反应中转移电子的数目为_________。
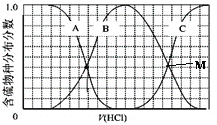
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS-、S2-的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出),滴加过程中,溶液中微位浓度大小关系正确的是_________ (填字母)。
A.c(Na+)=c(H2S)+c(HS-)+2c(S2-)
B.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
C.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
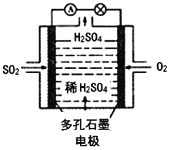
(4)某学习小组以SO2为原料,采用电化学方法制取硫酸。该小组设计的原电池原理如图2所示.写出该电池负极的电极反应式_________;
(5)难溶物ZnS遇CuSO4认溶液会慢慢转化为铜蓝(CuS)。若转化后溶液中c(Zn2+)=3.0×10-2molL-1,则c(Cu2+)= _________ molL-1〔已知Ksp(CuS)=1.0×10-36,Ksp(ZnS)=1.0×10-24
【答案】
(1)-41.8 kJmol-1.
(2)3mol;
(3)C;
(4)SO2-2e-+2H2O═SO42-+4H+;
(5)3.0×10-14;
【解析】
试题分析:(1)已知:①2SO2(g)+O2═2SO3(g)△H=-196.6kJmol-1,②2NO(g)+O2═2NO2(g)△H=-113.0kJmol-1,根据盖斯定律可知:将![]() ×①
×①![]() ×②,可得:NO2(g)+SO2(g)═SO3(g)+NO(g)△H=
×②,可得:NO2(g)+SO2(g)═SO3(g)+NO(g)△H=![]() KJ/mol
KJ/mol![]() KJ/mol=-41.8 kJmol-1故答案为:-41.8 kJmol-1.
KJ/mol=-41.8 kJmol-1故答案为:-41.8 kJmol-1.
(2)由反应可知,As元素的化合价由+3价升高为+5价,S元素的化合价由-2价升高为0,生成2molH3AsO4时,转移电子10mol,则生成H3AsO4的物质的量为0.6mol,反应中转移电子的数目为3mol,故答案为:3mol;
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,A表示含硫微粒浓度减小为S2-,B先增加后减少为HS-,C浓度一直在增加为H2S,向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,因体积相同,设Na2S、NaOH各为1mol,则n(Na)=3n(S),溶液中含硫的微粒为HS-、S2-、H2S,则c(Na+)=3[c(H2S)+c(HS-)+c(S2-)],故选C;
(4)该原电池中,负极上失电子被氧化,二氧化硫到硫酸,硫的化合价升高,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,所以负极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,故答案为:SO2-2e-+2H2O═SO42-+4H+;
(5)ZnS转化为CuS的离子方程式为:ZnS(s)+Cu2+(aq)![]() Zn2+(aq)+CuS(s);Ksp(ZnS)=c(Zn2+)c(S2-)=1.0×10-24,c(Zn2+)=3.0×10-2molL-1,则c(S2-)=
Zn2+(aq)+CuS(s);Ksp(ZnS)=c(Zn2+)c(S2-)=1.0×10-24,c(Zn2+)=3.0×10-2molL-1,则c(S2-)=![]() ×10-22,Ksp(CuS)=1.0×10-36,所以c(Cu2+)=
×10-22,Ksp(CuS)=1.0×10-36,所以c(Cu2+)=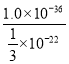 =3.0×10-14,故答案为:3.0×10-14。
=3.0×10-14,故答案为:3.0×10-14。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知:①能量越低的物质就越稳定,②白磷转化成红磷是放热反应。据此,下列判断或说法中正确的是
A.在相同的条件下红磷比白磷稳定
B.在相同的条件下,白磷比红磷稳定
C.红磷和白磷的物理性质相同
D.红磷容易发生自燃而白磷则不会自燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是( )
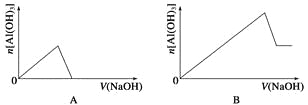
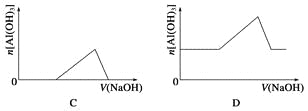
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某研究性学习小组设计的对一种废旧合金各成分(含有Cu、Fe、Si 三种成分)进行分离、回收再利用的工业流程,通过该流程将各成分转化为常用的单质及化合物。

已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=1.9×10-13,
根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ指的是 。
(2)加入过量FeCl3溶液过程中与较活泼的金属反应的离子方程式: 。
(3)过量的还原剂应是 ,溶液b中所含的金属阳离子有 。
(4)① 向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为
② 若用X mol/LKMnO4溶液处理溶液b,当恰好反应时消耗KMnO4溶液Y mL,则最后所得红棕色固体C的质量为 g(用含X、Y的代数式表示)。
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,则三种金属阳离子沉淀的先后顺序为: > > 。(填金属阳离子)
(6)最后一步电解若用惰性电极电解一段时间后,析出固体B的质量为m g,同时测得阴阳两极收集到的气体体积相等,则标况下阳极生成的最后一种气体体积为 L。(用含m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物在空气中燃烧的说法正确的是( )
A. 只有碳的氧化物和水
B. 只有CO2和水
C. 可能有碳的氧化物、水及其他元素的化合物
D. 有CO、CO2、水及其他元素的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种含碳、氢、氧三种元素的有机化合物,可以使溴水褪色,难溶于水,在酸性条件下可发生水解反应,得到一分子B和一分子甲醇。B的分子式为C3H4O2,分子中没有支链(无甲基或乙基),能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有 (选填编号)
① 加成反应 ② 酯化反应 ③ 加聚反应 ④ 氧化反应
(2)B分子所含官能团的名称是 、 。
(3)A与NaOH溶液共热时发生反应的化学方程式是: 。
(4)写出B发生加聚反应的产物的结构简式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是
A. 氯化镁、氢氧化钠 B. 硫酸钠、氢氧化钡
C. 氯化铝、氨水 D. 溴化亚铁、氯水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用CO2、CO对构建低碳社会有重要意义。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g)+2H2(g)![]() CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
①10min后达到平衡时CO的浓度为 ;
②10min内用H2表示的平均反应速率为 ;
③若要加快CH3OH的生成速率,可采取的措施有 (填一种合理的措施)
(2)利用H2 和CO2在一定条件下可以合成乙烯:6H2+2CO2![]() CH2=CH2+4H2O
CH2=CH2+4H2O
①已知:4.4gCO2与H2完全转化为CH2=CH2和水(气态)共放出6.39kJ的热量,
写出该反应的热化学方程式 。
②不同温度对CO2的转化率及催化剂的催化效率的影响如图甲所示。
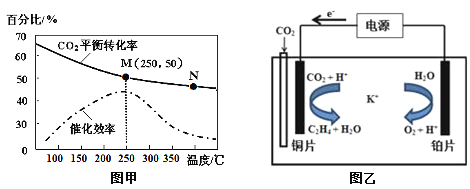
下列有关说法不正确的是 (填序号)。
A.不同条件下反应,N点的速率最大
B.温度在约250℃时,催化剂的催化效率最高
C.相同条件下,乙烯的产量M点比N高
③若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图甲中M点时,产物CH2=CH2的体积分数为 。(保留两位有效数字)
(3)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图乙所示。在阴极上产生乙烯的电极反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com