
【题目】有A、B、C、D四种金属,进行如下实验:①将A与B浸在稀硫酸中用导线相连,A逐渐溶解,B上有气泡逸出;②将A、D分别投入等浓度盐酸中,D比A反应剧烈;③将B浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C
C.D>B>A>C D.B>A>D>C
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】二氧化锰是化学工业中常用的氧化剂和有机合成中的催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3+ O2![]() 2MnO2+2CO2。经研究发现该反应过程为①MnCO3
2MnO2+2CO2。经研究发现该反应过程为①MnCO3![]() MnO+ CO2;②2MnO +O2
MnO+ CO2;②2MnO +O2![]() 2MnO2。
2MnO2。
回答下列问题:
(1)某温度下该平衡体系的压强为P,CO2、O2的物质的量分别为n1和n2,用平衡分压代替平衡浓度,碳酸锰热分解反应的平衡常数K=________(分压=总压×物质的量分数);K与反应①、②的平衡常数K1、K2的关系为_________________。
(2)反应②在低温下能自发进行,则其△H__________0 (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量.下列表示氢氧化钠加入量(x)与溶液中沉淀的量(y)的关系示意图中正确的是( )
A.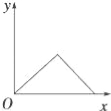 B.
B.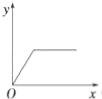 C.
C.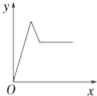 D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子效的3倍。X、Y和Z分属不同的周期,它们的原子序教之和是W 原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二元化合物中.由元素W与Y形成的化合物M的熔点最高。
请回答下列问题:
(1)W元素原子的L层电子排布式为__________,W3分子的空间构型为______;
(2)X单质与水发生主要反应的化学方程式为_____________;
(3)化合物M的化学式为_______,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是_________。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有___________,O-C-O的键角约为_______;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X:Y:Z=___________;
(5)含有元素Z的盐的焰色反应为_____色。许多金属盐都可以发生焰色反应,其原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某盐 A是由三种元素组成的化合物,某研究小组按如图流程探究其组成:
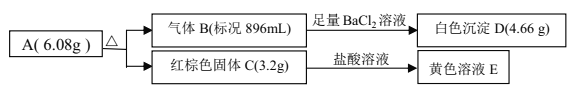
请回答:
(1)写出红棕色固体 C 的化学式____________。
(2)写出 A 受热分解反应的化学方程式____________。
(3)写出气体 B 与溶液 E 反应的离子方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 G(异戊酸薄荷醇酯)是一种治疗心脏病的药物。其合成线路如下:
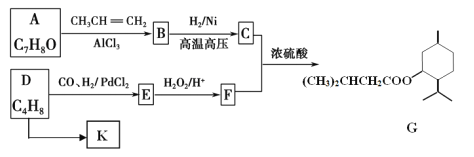
已知:①RCH=CH2+CO+H2![]() RCH2CH2CHO
RCH2CH2CHO
②A能与 FeCl3发生显色反应, K是高分子化合物
③![]()
请填写下列空白:
(1)F中官能团名称_____,A到B的反应类型________。
(2)写出C和F反应生成G的化学方程式___________。
(3)下列说法正确的是_______。
A.有机物 G 的分子式为 C15H28O2
B.有机物 A 溶液能与 Na2CO3 溶液反应产生 CO2
C.有机物 C 不能与浓溴水反应生成白色沉淀
D.有机物 D 生成 K 的反应为缩聚反应
(4)某芳香族化合物 X是B的同分异构体,X分子中含有4种不同化学环境的氢原子,其对应的个数比为 9:2:2:1,写出该化合物可能的结构简式_________。
(5)正戊酸的化学式为CH3(CH2)3COOH,可用作香料、橡胶促进剂等,写出以正丁醇(CH3CH2CH2CH2OH)为原料制备正戊酸的合成路线流程图(无机试剂任用)。
__________
合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常通过高温分解FeSO4的方法制备Fe2O3,为检验FeSO4高温分解的产物,并进行有关探究实验,回答下列问题:
实验一:高温分解FeSO4,利用如图所示的实验装置进行实验。
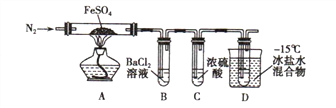
已知:①SO2熔点为-72℃,沸点为-10℃ ② SO3熔点为-16.8℃,沸点为44.8℃
(1)连接装置,检验气密性良好,放入药品,通入一段时间N2然后加热,通入N2的目的是_________________________
(2)隔绝空气加热至650℃,看到B中有白色沉淀,D试管中有无色液体,硬质玻璃管中的固体变为_________色,写出该反应的化学方程式___________________。
(3)反应完毕后,停止加热冷却后,取硬质玻璃管中固体,加盐酸,反应的离子方程式是__________________, 将反应后所得溶液滴入D试管中,溶液变为浅绿色,该反应的离子方程式是 _______________
实验二 探究高温分解 FeSO4生成的气体
(4)用如图所示装置设计实验,验证高温分解FeSO4生成的气态物质
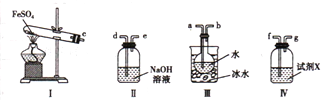
①按气流方向连接各仪器,用字母表示接口的连接顺序:c-__________________________
②试剂X的名称是 ___________________________
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的FeSO4 的质量,向圆底烧瓶中逐渐滴入氯化钡溶液,直到沉淀完全;然后过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。若最终得到沉淀的质量为Wg ,则已分解的FeSO4的质量 ________________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com