
【题目】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
(1)Y、Z、M、G四种元素的原子半径由大到小的顺序是____________ (用元素符号表示)。
(2)Z在元素周期表中的位置为____________,M2Z的电子式为____________。
(3)上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是__________(写化学式)。
(4)X与Y能形成多种化合物,其中既含极性键又含非极性键,且它的产量可以用来衡量一个国家的石油化工发展水平的是____________ (写名称)。
(5)GQ3溶液与过量的MZX溶液反应的化学方程式为_________________________________
(6)常温下,不能与G的单质发生反应的是____________ (填标号)。
a.CuSO4溶液 b.浓硫酸 c.NaOH溶液 d.浓硝酸 e.氧化铜
【答案】![]() 第二周期ⅥA族
第二周期ⅥA族 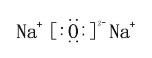
![]() 乙烯 AlCl3+4NaOH=3NaCl+NaAlO2+2H2O e
乙烯 AlCl3+4NaOH=3NaCl+NaAlO2+2H2O e
【解析】
X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大.Z、G分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、G为Al元素;Y的原子最外层电子数是其电子层数的2倍,原子序数小于O,只能处于第二周期,最外层电子数为4,则Y为C元素;X单质在常温下呈气态,则X为H元素,X与M同主族,原子序数大于O,则M为Na;Q单质常温下为气态,原子序数大于Al,则Q为Cl.
(1)同周期自左而右原子半径减小,同主族自上而下原子半径减小,故原子半径![]() ;
;
(2)Z为O元素,在元素周期表中的位置为第二周期ⅥA族,M2Z为氧化钠,电子式为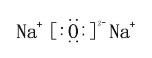 ;
;
(3)上述元素的最高价氧化物对应的水化物酸性最强的是![]() ;
;
(4)X与Y能形成多种化合物,其中既含极性键又含非极性键,且它的产量可以用来衡量一个国家的石油化工发展水平的是乙烯;
(5)GQ3溶液与过量的MZX溶液反应的化学方程式为AlCl3+4NaOH=3NaCl+NaAlO2+2H2O;
(6)常温下,不能与G的单质发生反应的是e氧化铜。


科目:高中化学 来源: 题型:
【题目】1L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.1mol/L和0.4mol/L。若向该混合溶液中加入足量的铜粉,从离子反应的角度分析,则最多能溶解铜粉的质量为( )
A. 9.6gB. 6.4 gC. 3.2 gD. 2.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向某容积恒定的密闭容器中充入1 mol N2、3 mol H2,经充分反应后达到如下平衡:N2(g)+3H2(g)![]() 2NH3(g),下列有关说法中正确的是( )
2NH3(g),下列有关说法中正确的是( )
A. 达平衡后再加入一定量的N2,体系内各物质含量不变
B. N2、H2、NH3的浓度一定相等
C. 反应没有达到平衡时,NH3会不断地分解,达到平衡时则不会再分解
D. 平衡时,N2、H2物质的量之比为1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。下列叙述正确的是
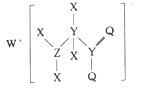
A.WX的水溶液呈中性
B.元素非金属性的顺序为Y>Z>Q
C.Z的最高价氧化物对应的水化物是一元强酸
D.该化合物中与Y单键相连的Q不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述不正确的是
A.1.8g 15NH3含有的电子数为NA
B.1L 0.1 mol·L-1硫酸钠溶液中含有的氧原子数为0.4NA
C.常温常压下,8g硝酸铵中含有的氮原子数为0.2NA
D.通常状况下,22.4LCO2和CO的混合气体,其物质的量小于1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算:
(1)同温同压下,等质量的SO2气体和CO气体密度之比为________;体积比为________;原子个数比为________。
(2)某混合溶液中只含有下列几种离子:Na+、Mg2+、Al3+、Cl-、SO42-,若Na+、Mg2+、Cl-、SO42-的物质的量浓度依次为0.2mol/L、0.25mol/L、0.5mol/L、0.25mol/L,则c(Al3+)=________。
(3)在标准状况下,某混合气体密度是2.86gL-1,该混合气体的平均相对分子质量是________;现有质量比为11:7的CO2和CO的混合气体,该混合气体的摩尔质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、E四种常见物质含有同一种元素,其中E是一种强酸,在一定条件下,它们有如图所示转化关系,下列推断不合理的是( )
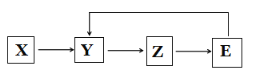
A. X可能是一种氢化物
B. Y不可能转化为X
C. Y可能直接转化为E
D. 若X是单质,则X转化为Y的反应可能是化合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学用一种铝铁合金为原料,模拟相关的工业生产,反应过程如图所示(部分产物和条件已略去),请回答:
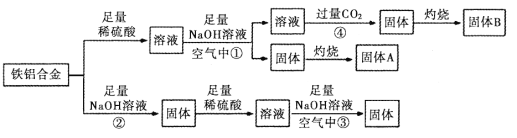
(1)铁铝合金是一种高电磁性能合金,下列有关推测不正确的是_______________(填序号)
a. 铁可由铁和铝熔融制成
b. 铁熔点高于铝和铁
c. 铁铝合金硬度高于纯铝
(2)反应①结束后,需要进行的操作中除使用烧杯外 ,还需使用的玻璃仪器有_____________。
(3)反应②的离子方程式_______________________________________。
(4)反应③发生时观察到的现象是_________________________________________。
(5)反应④中的CO2不宜换成HCl,原因是_________________________________________。
(6)固体A是一种红色颜料。将一定量固体A溶于160mL 5 mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),经检测溶液中无Fe3+,则参加反应的铁粉的质量为_________g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化工厂对海水资源综合利用的示意图。根据以上信息,判断下列相关分析不正确的是
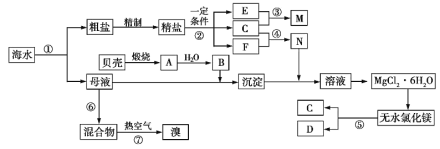
A. 上述提取Mg的流程中,没有涉及的反应类型是置换反应
B. 因氮气的化学性质相对稳定,冷却电解无水氯化镁所得的镁蒸气时,可选择氮气
C. 反应⑥所用的气态氧化剂可从本厂生产烧碱处循环利用或从本厂生产镁单质处循环利用
D. 从母液中提取Mg和Br2的先后顺序:先提取Br2,后提取Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com