
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步操作采取的分离方法是___________________。
(2)根据上述框图反应关系,写出下列B、C、E所含物质的化学式
沉淀固体B________________;C______________________;E_______________
(3)写出①、④四个反应方程式(是离子反应的写离子方程式)
①____________________________ ④__________________________
【答案】过滤 Al2O3 Al2O3、Fe2O3 K2SO4、(NH4)2SO4 (加上NH3·H2O不扣分) Al2O3+2OH- = 2AlO2- + H2O 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】
本题考查化学工艺流程,(1)I、II、III、IV步得到溶液和沉淀,因此操作步骤是过滤;(2)KAl(SO4)2溶于水,Al2O3和Fe2O3不溶于水,即沉淀C为Al2O3和Fe2O3,溶液为KAl(SO4)2溶液,反应②发生Al3++3NH3·H2O=Al(OH)3↓+3NH4+,即溶液E为K2SO4、(NH4)2SO4和过量的NH3·H2O,沉淀是Al(OH)3,Al2O3属于两性氧化物,Fe2O3为碱性氧化物,沉淀C中加入NaOH溶液,发生Al2O3+2OH-=2AlO2-+H2O,沉淀D为Fe2O3,反应③发生AlO2-+H++H2O=Al(OH)3↓,反应④发生2Al(OH)3![]() Al2O3+3H2O,固体B为Al2O3;(3)根据上述分析,反应①的离子方程式为Al2O3+2OH-=2AlO2-+H2O,反应④的化学反应方程式为2Al(OH)3
Al2O3+3H2O,固体B为Al2O3;(3)根据上述分析,反应①的离子方程式为Al2O3+2OH-=2AlO2-+H2O,反应④的化学反应方程式为2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。


科目:高中化学 来源: 题型:
【题目】现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。
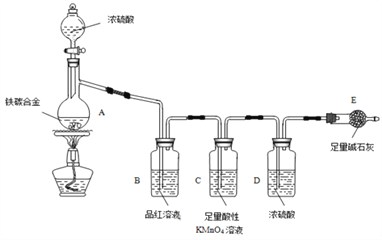
I、探究浓硫酸的某些性质
(1)按图示连接装置,检查装置___________,称量E的质量。
(2)将aɡ铁碳合金样品放入A中,再加入适量的浓硫酸,仪器A的名称为______,未点燃酒精灯前,A、B 均无明显现象,其原因是______________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象,如A中![]() ,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
(4)随着反应的进行,浓硫酸浓度逐渐减小变为稀硫酸,A中还可能发生某些离子反应,写出相应的离子方程式:_________________、____________________。
II、测定铁的质量分数
(5)待A中固体完全消失并不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为___________________(写表达式)。
(6)某同学认为上述方法较复杂,使用如图所示的装置和其他常用的实验仪器测定某些数据即可。为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。

①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量ag
【答案】气密性 蒸馏烧瓶 常温下,铁被浓硫酸钝化 C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 品红溶液逐渐褪色 强氧化 2Fe3++Fe=3Fe2+ Fe+2H+=Fe2++H2↑
CO2↑+2SO2↑+2H2O 品红溶液逐渐褪色 强氧化 2Fe3++Fe=3Fe2+ Fe+2H+=Fe2++H2↑ ![]()
③
【解析】
(1)按图示连接好装置以后,首先检查装置的气密性:(2)根据仪器构造可知仪器A的名称为蒸馏烧瓶;常温下Fe在浓硫酸中钝化,碳不与浓硫酸反应,故无明显现象;(3)浓硫酸具有强氧化性,在加热的条件下碳与浓硫酸反应的方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;二氧化硫具有漂白性,因此B中的现象是品红溶液逐渐褪色,根据以上分析可知浓硫酸具有强氧化性;(4)硫酸浓度减小后,稀硫酸与铁发生置换反应生成硫酸亚铁和氢气,另外铁还能与硫酸铁反应生成硫酸亚铁,离子方程式分别为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+;(5)称取ag铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则ag铁碳合金中含碳元素的质量为
CO2↑+2SO2↑+2H2O;二氧化硫具有漂白性,因此B中的现象是品红溶液逐渐褪色,根据以上分析可知浓硫酸具有强氧化性;(4)硫酸浓度减小后,稀硫酸与铁发生置换反应生成硫酸亚铁和氢气,另外铁还能与硫酸铁反应生成硫酸亚铁,离子方程式分别为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+;(5)称取ag铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则ag铁碳合金中含碳元素的质量为![]() ,则含铁的质量为
,则含铁的质量为![]() ,铁的质量分数为
,铁的质量分数为![]() ;(6)因为铁炭合金中的铁可以与稀硫酸反应生成氢气,瓶总质量的减少量即为氢气的生成量,而铁的质量可以通过氢气的质量求出,答案选③。
;(6)因为铁炭合金中的铁可以与稀硫酸反应生成氢气,瓶总质量的减少量即为氢气的生成量,而铁的质量可以通过氢气的质量求出,答案选③。
【题型】实验题
【结束】
29
【题目】现有一种铜粉和铝粉的混合物样品,为测定该样品中铝的含量,称取5.0g此样品置于锥形瓶中,将100mL稀盐酸加入其中恰好完全反应,剩余固体2.3g.
(1)求该混合物中铝的质量分数为多少?
(2)所用盐酸中溶质的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是____。
A.陶瓷 B.玻璃 C.水泥 D.生石灰
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为____________________,工艺师常用______(填物质名称)来雕刻玻璃。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作______。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.瓷坩埚 D.铁坩埚
(4)工业上常利用反应2C+SiO2![]() Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___(填化学式,下同),氧化剂是____
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___(填化学式,下同),氧化剂是____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容器中充入SO2和只由18O原子组成的氧气(18O2)。在一定条件下达到平衡时,18O存在于
A.只存在于O2中
B.只存在于O2和SO3中
C.只存在于SO2和SO3中
D.SO3、SO2和O2中都有可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的( )
①常温常压下,11.2 L乙烷所含的分子数为0.5NA
②14.2g 硫酸钠固体中含有0.1NA个硫酸钠分子:
③常温下,21gC3H6和C4H8的混合物中含有的碳原子数为1.5NA
④2gD216O中含有的质子数、中子数、电子数均为NA
⑤标准状况下,由H2O2分解制得4.48LO2转移的电子数目为0.2NA
⑥10ml 18mol/L 的浓硫酸与足量的镁反应时转移的电子数为0.18NA
A. ③④ B. ①⑥ C. ④⑤⑥ D. ①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液吸收有毒的硫化氢气体。工艺原理如下图所示。下列说法中不正确的是( )
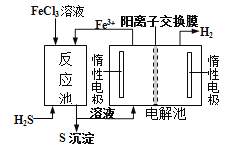
A. H+从电解池左槽迁移到右槽 B. 左槽中发生的反应是:2Cl--2e-=Cl2↑
C. 右槽的反应式: 2H++2e-=H2↑ D. FeCl3溶液可以循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu3N 具有良好的电学和光学性能在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工程等领域中,发挥着广泛的、不可替代的巨大作用。
(1)C、N、O 三种元素的第一电离能由大到小的顺序为_________________。
(2)与N3-含有相同电子数的三原子分子的空间构型是____________。
(3)Cu+的电子排布式为___________,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu,但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO 为何会生成Cu2O:____________________。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙酸,乙醛分子中碳原子的杂化方式是___________,乙醛分子H-C-O的键角___________(填“大于”、“等于”或“小于”)乙醇分子中的H-C-O 的键角。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出Cu(H2O)2Cl2具有极性的分子的结构式:___________。
(6)Cu3N的晶胞结构如右图所示,N3-的配位数为___________,Cu+的半径为apm,N3-的半径为bpm,Cu3N的密度为___________g·cm-3(阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《神农本草经》记载,神农尝百草,日遇七十二毒,得茶而解。茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )
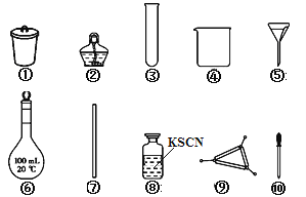
A. 将茶叶灼烧灰化,选用①、②和⑨
B. 用浓盐酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C. 过滤得到滤液,选用④、⑤和⑦
D. 检验滤液中的Fe3+,选用③、⑧和⑩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com