
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵������ȷ�ģ� ��
�ٳ��³�ѹ�£�11.2 L���������ķ�����Ϊ0.5NA
��14.2g �����ƹ����к���0.1NA�������Ʒ��ӣ�
�۳����£�21gC3H6��C4H8�Ļ�����к��е�̼ԭ����Ϊ1.5NA
��2gD216O�к��е�������������������������ΪNA
�ݱ�״���£���H2O2�ֽ��Ƶ�4.48LO2ת�Ƶĵ�����ĿΪ0.2NA
��10ml 18mol/L ��Ũ������������þ��Ӧʱת�Ƶĵ�����Ϊ0.18NA
A. �ۢ� B. �٢� C. �ܢݢ� D. �٢ڢ�
���𰸡�A
�������������³�ѹ�£����������Ħ���������22.4L/mol,11.2 L�����ķ���������0.5NA�����������������ƹ��������Ӿ��壬���������Ӻ���������ӣ��������ӣ�����������![]() ��̼ԭ����
��̼ԭ����![]() ��
��![]() ��̼ԭ����
��̼ԭ����![]() ��������ﺬ�е�̼ԭ����ҲΪ
��������ﺬ�е�̼ԭ����ҲΪ![]() ��������ȷ����
��������ȷ����![]() �����ʵ���Ϊ
�����ʵ���Ϊ![]() ��һ��
��һ��![]() ���Ӻ��е����������������͵�������Ϊ10�����е���ĿΪ
���Ӻ��е����������������͵�������Ϊ10�����е���ĿΪ![]() ��������ȷ����
��������ȷ����![]() ������
������![]() ��ϵ��֪ת�Ƶ�����ĿΪ
��ϵ��֪ת�Ƶ�����ĿΪ![]() ��������ȷ������ʼʱ��Ũ������þ������Ӧ
��������ȷ������ʼʱ��Ũ������þ������Ӧ![]() ������������ת�Ƶ������Ĺ�ϵΪ
������������ת�Ƶ������Ĺ�ϵΪ![]() ����Ӧһ��ʱ�������Ũ�ȼ�С����þ������Ӧ��
����Ӧһ��ʱ�������Ũ�ȼ�С����þ������Ӧ��![]() ��������������ת�Ƶ������Ĺ�ϵΪ
��������������ת�Ƶ������Ĺ�ϵΪ![]() �����
�����![]() Ũ����������þ��Ӧת�Ƶ���������
Ũ����������þ��Ӧת�Ƶ���������![]() ������������ȷ���Ϊ:�ۢ�������������������ȷ��ΪA��
������������ȷ���Ϊ:�ۢ�������������������ȷ��ΪA��


 ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾij�������ӵĿռ�ṹʾ��ͼ(���߲���ʾ���ۼ�)��ͨ���۲����������������ȷ����(����)
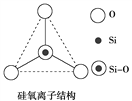
A. ����Ϊ120�� B. ��ѧ���ΪSiO![]()
C. Siԭ�Ӳ���sp2����ӻ���ʽ D. ��ѧ���ΪSiO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:25 C ʱ,Ksp[Zn(OH)2]= 1.0��10-18�� Ka(HCOOH)= 1.0��10-4�����¶��£�����˵���������
A. HCOO����ˮ��ƽ�ⳣ��Ϊ 1.0��10-10
B. �� Zn(OH)2 ����Һ�м����� HCOOH,��Һ�� c(Zn2+)����
C. Zn(OH)2����ˮ�γɵı�����Һ��,c(Zn2��)>1.0��10-6 mol/L
D. Zn(OH)2(s) +2HCOOH(aq)![]() Zn2+(aq) +2HCOO��(aq) +2H2O(l)��ƽ�ⳣ�� K= 100
Zn2+(aq) +2HCOO��(aq) +2H2O(l)��ƽ�ⳣ�� K= 100
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A�� B�� C�� D�� E�� F Ϊǰ������Ԫ����ԭ�����������������л�̬ A ԭ�ӵĵ��ӷֲ��� 3 ���ܼ�����ÿ���ܼ������ĵ�������ͬ�� C ��ԭ�Ӻ���������� 6 ���˶�״̬��ͬ�ĵ��ӣ� D �Ƕ�����Ԫ���е縺����С��Ԫ�أ� E ������������ˮ����������ǿ�� ��̬ F ԭ�Ӻ��������ֻ��һ�����ӣ� �����ܲ���������ӡ� G Ԫ���� D Ԫ��ͬ���壬����� 3 �����ڡ�
��1��Ԫ�� A�� B�� C �ĵ�һ��������С�������____________________����Ԫ�ط��ű�ʾ����
��2��E����ۺ������� E ԭ�ӵ��ӻ���ʽΪ_____________�� ��̬ E ԭ���У��������ռ������ܼ��ĵ�����������״Ϊ____________________________��
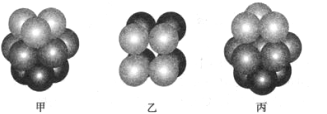
��3��Fԭ�ӵ���Χ�����Ų�ʽΪ_______________________�� F ���ʾ�����ԭ�ӵĶѻ���ʽ����ͼ�е�_______����д�������� ���������������� ���þ���Ŀռ�������Ϊ_____________����������λ��Ч���֣�
��4����֪Ԫ�� A��B�γɵ�(AB)2����������ԭ�Ӷ����� 8�����ȶ��ṹ����������� ������ ������Ŀ֮��Ϊ__________��
��5��ͨ������£� D ���ʵ��۷е�� G ���ʸߣ�ԭ����_________________________��
��6����֪ DE ����ľ�������ͼ��ʾ��
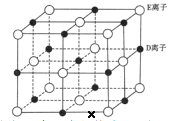
���� DE �����е����� E ����ȥ�������� D ����ȫ����Ϊ A ԭ�ӣ��������е� 4 ����С�����������ĸ�����һ��A ԭ�ӣ����� 4 ����С�������������ڡ�λ����С���������е� A ԭ��������� 4 �� A ԭ���Ե����������ɴ˱�ʾ A��һ�־���ľ�������֪ A��A ���ļ���Ϊa cm�� NA��ʾ�����ӵ�����������þ����к���_________�� A ԭ�ӣ��þ�����ܶ���______________g��cm-3����ʽ��ʾ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����A������KAl(SO4)2��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ������֮��ı仯��

�ݴ˻ش��������⣺
��1��I��II��III��IV�IJ�������ȡ�ķ��뷽����___________________��
��2������������ͼ��Ӧ��ϵ��д������B��C��E�������ʵĻ�ѧʽ
��������B________________��C______________________��E_______________
��3��д���١����ĸ���Ӧ����ʽ�������ӷ�Ӧ��д���ӷ���ʽ��
��____________________________ ��__________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C���ǽ�������A����C����������Һ�У�A�ı�����C������A��B������Һ���ԭ���ʱ��BΪ��صĸ�����A��B��C���ֽ����Ļ��˳��Ϊ
A.A>B>CB.A>C>BC.B>A>CD.B>C>A
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������SO2(g)��O2(g)�ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У��ڲ�ͬ�¶��½��з�Ӧ��2SO2(g)+ O2(g)![]() 2SO3 ��H<0���õ�����е���������������˵������ȷ����
2SO3 ��H<0���õ�����е���������������˵������ȷ����
ʵ���� | �¶�/�� | ƽ�ⳣ��/mol-1��L | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
A. T1��T2�Ĺ�ϵ��T1 �� T2
B. x= 1.6��y=0.2 ��t<6
C. K1��K2�Ĺ�ϵ��K2��K1
D. ʵ��1��ǰ6min�ķ�Ӧ������(SO2)=0.2 mol��L-1��min-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe3O4��һ�ֺ�ɫ��ĩ���ֳƴ�����������������ɿ�д��FeO��Fe2O3��ij��ѧʵ��С��ͨ��ʵ����̽��һ��ɫ��ĩ�Ƿ���Fe3O4��CuO���(������������ɫ����)��̽���������£�
��������裺 ����1����ɫ��ĩ��CuO������2����ɫ��ĩ��Fe3O4;
����3����ɫ��δ��CuO��Fe3O4�Ļ����
�����̽��ʵ�飺
����һ��ȡ������ĩ��������ϡ���ᣬ������2�����3������ʵ��������___________����ط�Ӧ�����ӷ���ʽΪ__________________________________��
�������� �������ϣ� Cu2+��������ˮ��Ӧ��������ɫ��Һ��Cu2++4NH3��H2O=Cu(NH3)42++4H2O��Ϊ̽���Ǽ���2���Ǽ���3��������ȡ������ĩ��ϡ�������ܽ���ټ���������ˮ��������___________���������2������������___________���������3������
��������
ѧ����������ͼ��ʾװ�ý���ʵ�飬������Ӧǰ��װ��C����Ʒ����������ȷ����Ʒ����ɡ��ش��������⣺
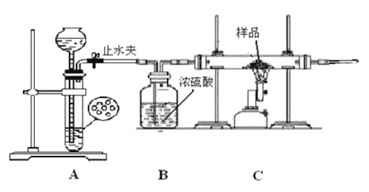
(1)����ʵ�鲽����Ⱥ�˳����___________(�����)��
�ٴ�ֹˮ�У��ڹر�ֹˮ�У��۵�ȼC���ľƾ���ƣ�
��Ϩ��C���ľƾ���� ���ռ��������鴿��
�ڵ�ȼC���ƾ����ǰҪ���еı�Ҫ������__________________________��
(2)������Ʒȫ���μӷ�Ӧ����ʵ��ǰ��Ʒ������Ϊ4.7�ˣ�ʵ���Ƶ�װ��C�й��������3.6�������___________(�1����2����3��) ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼW��X��Y��ZΪ�������ʣ�����ͷ����һ��ת���ij�����Ӧ�����г������ܽ��е��ǣ� ��
ѡ�� | W | X | Y | Z |
|
A | S | SO2 | SO3 | H2SO4 | |
B | Al | AlCl3 | NaAlO2 | Al2(SO4)3 | |
C | Fe | FeCl3 | Fe(OH)2 | FeCl2 | |
D | Na | Na2O2 | NaOH | NaCl |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com