
【题目】已知:25 C 时,Ksp[Zn(OH)2]= 1.0×10-18, Ka(HCOOH)= 1.0×10-4。该温度下,下列说法错误的是
A. HCOO-的水解平衡常数为 1.0×10-10
B. 向 Zn(OH)2 悬浊液中加少量 HCOOH,溶液中 c(Zn2+)增大
C. Zn(OH)2溶于水形成的饱和溶液中,c(Zn2+)>1.0×10-6 mol/L
D. Zn(OH)2(s) +2HCOOH(aq)![]() Zn2+(aq) +2HCOO-(aq) +2H2O(l)的平衡常数 K= 100
Zn2+(aq) +2HCOO-(aq) +2H2O(l)的平衡常数 K= 100
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. MnO2与浓盐酸混合加热:MnO2+4H++2Cl﹣![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B. 大理石与盐酸反应:CO32﹣+2H+ = H2O+CO2↑
C. 向醋酸溶液中滴加NaOH溶液:OH-+H+![]() H2O
H2O
D. 漂白粉溶液吸收二氧化碳:Ca2++ CO2+ H2O = CaCO3↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列说法正确的是( )
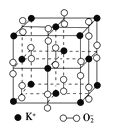
A. 超氧化钾的化学式为KO2,每个晶胞含14个K+和13个O
B. 晶体中每个K+周围有8个O,每个O周围有8个K+
C. 晶体中与每个K+距离最近的K+有8个
D. 晶体中0价氧原子与-2价氧原子的数目比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。
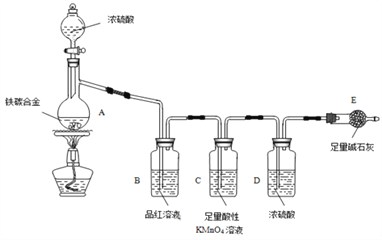
I、探究浓硫酸的某些性质
(1)按图示连接装置,检查装置___________,称量E的质量。
(2)将aɡ铁碳合金样品放入A中,再加入适量的浓硫酸,仪器A的名称为______,未点燃酒精灯前,A、B 均无明显现象,其原因是______________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象,如A中![]() ,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
(4)随着反应的进行,浓硫酸浓度逐渐减小变为稀硫酸,A中还可能发生某些离子反应,写出相应的离子方程式:_________________、____________________。
II、测定铁的质量分数
(5)待A中固体完全消失并不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为___________________(写表达式)。
(6)某同学认为上述方法较复杂,使用如图所示的装置和其他常用的实验仪器测定某些数据即可。为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。

①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量ag
【答案】气密性 蒸馏烧瓶 常温下,铁被浓硫酸钝化 C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 品红溶液逐渐褪色 强氧化 2Fe3++Fe=3Fe2+ Fe+2H+=Fe2++H2↑
CO2↑+2SO2↑+2H2O 品红溶液逐渐褪色 强氧化 2Fe3++Fe=3Fe2+ Fe+2H+=Fe2++H2↑ ![]()
③
【解析】
(1)按图示连接好装置以后,首先检查装置的气密性:(2)根据仪器构造可知仪器A的名称为蒸馏烧瓶;常温下Fe在浓硫酸中钝化,碳不与浓硫酸反应,故无明显现象;(3)浓硫酸具有强氧化性,在加热的条件下碳与浓硫酸反应的方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;二氧化硫具有漂白性,因此B中的现象是品红溶液逐渐褪色,根据以上分析可知浓硫酸具有强氧化性;(4)硫酸浓度减小后,稀硫酸与铁发生置换反应生成硫酸亚铁和氢气,另外铁还能与硫酸铁反应生成硫酸亚铁,离子方程式分别为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+;(5)称取ag铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则ag铁碳合金中含碳元素的质量为
CO2↑+2SO2↑+2H2O;二氧化硫具有漂白性,因此B中的现象是品红溶液逐渐褪色,根据以上分析可知浓硫酸具有强氧化性;(4)硫酸浓度减小后,稀硫酸与铁发生置换反应生成硫酸亚铁和氢气,另外铁还能与硫酸铁反应生成硫酸亚铁,离子方程式分别为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+;(5)称取ag铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则ag铁碳合金中含碳元素的质量为![]() ,则含铁的质量为
,则含铁的质量为![]() ,铁的质量分数为
,铁的质量分数为![]() ;(6)因为铁炭合金中的铁可以与稀硫酸反应生成氢气,瓶总质量的减少量即为氢气的生成量,而铁的质量可以通过氢气的质量求出,答案选③。
;(6)因为铁炭合金中的铁可以与稀硫酸反应生成氢气,瓶总质量的减少量即为氢气的生成量,而铁的质量可以通过氢气的质量求出,答案选③。
【题型】实验题
【结束】
29
【题目】现有一种铜粉和铝粉的混合物样品,为测定该样品中铝的含量,称取5.0g此样品置于锥形瓶中,将100mL稀盐酸加入其中恰好完全反应,剩余固体2.3g.
(1)求该混合物中铝的质量分数为多少?
(2)所用盐酸中溶质的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.9克的镁铝合金,投入到500mL 2mol/L的盐酸中,金属完全溶解,再加入4mol/L的氢氧化钠溶液,若要生成沉淀最多,加入这种氢氧化钠溶液的体积是()
A.125mL B.200mL C.250mL D.560mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是____。
A.陶瓷 B.玻璃 C.水泥 D.生石灰
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为____________________,工艺师常用______(填物质名称)来雕刻玻璃。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作______。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.瓷坩埚 D.铁坩埚
(4)工业上常利用反应2C+SiO2![]() Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___(填化学式,下同),氧化剂是____
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___(填化学式,下同),氧化剂是____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的( )
①常温常压下,11.2 L乙烷所含的分子数为0.5NA
②14.2g 硫酸钠固体中含有0.1NA个硫酸钠分子:
③常温下,21gC3H6和C4H8的混合物中含有的碳原子数为1.5NA
④2gD216O中含有的质子数、中子数、电子数均为NA
⑤标准状况下,由H2O2分解制得4.48LO2转移的电子数目为0.2NA
⑥10ml 18mol/L 的浓硫酸与足量的镁反应时转移的电子数为0.18NA
A. ③④ B. ①⑥ C. ④⑤⑥ D. ①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于镁合金具有硬度大、密度小、散热性好、抗震性好等优异性能它被用于制笔记本电脑外壳、竞赛自行车车架等。现称取一定质量的镁铝合金样品放入500 mL稀硫酸中,固体全部溶解并放出气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

(1)合金中Al的质量为__________________。
(2)NaOH溶液的物质的量浓度为__________________。
(3)稀硫酸的物质的量浓度为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com