
【题目】Fe3O4是一种黑色粉末,又称磁性氧化铁,它的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
Ⅰ.提出假设: 假设1.黑色粉末是CuO;假设2.黑色粉末是Fe3O4;
假设3.黑色粉未是CuO和Fe3O4的混合物
Ⅱ.设计探究实验:
方案一:取少量粉末加入足量稀硝酸,若假设2或假设3成立则实验现象是___________,相关反应的离子方程式为__________________________________。
方案二: 查阅资料: Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生___________现象,则假设2成立;若产生___________现象,则假设3成立。
方案三:
学生丙利用下图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:
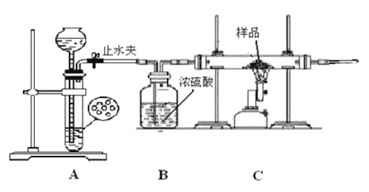
(1)下列实验步骤的先后顺序是___________(填序号)。
①打开止水夹;②关闭止水夹;③点燃C处的酒精喷灯;
④熄灭C处的酒精喷灯 ⑤收集氢气并验纯。
在点燃C处酒精喷灯前要进行的必要操作是__________________________。
(2)假设样品全部参加反应,若实验前样品的质量为4.7克,实验后称得装置C中固体的质量3.6克则假设___________(填“1”“2”或“3”) 正确。
【答案】 固体溶解,产生无色气体,并在试管上方变为红棕色 3Fe3O4+28H++NO3- = 9Fe3++NO+14H2O 只有红褐色沉淀 红褐色沉淀,同时溶液呈深蓝色 ①⑤③④② 检验装置中氢气的纯度 3
【解析】如果假设2成立,则加入硝酸后得到的溶液中含有三价铁离子,溶液为黄色,且在试管口处有红棕色气体产生。如果假设3成立,则加入硝酸后得到的溶液中含有三价铁离子和二价铜离子,溶液显蓝色,试管口处有红棕色气体产生。相关反应的离子方程式为3Fe3O4+28H++NO3- = 9Fe3++NO+14H2O。答案:固体溶解,产生无色气体,并在试管上方变为红棕色 . 3Fe3O4+28H++NO3- = 9Fe3++NO+14H2O
如果假设2成立,则加入稀硫酸后得到的溶液中含有三价铁离子,加入氨水后生成氢氧化铁红褐色沉淀;如果假设3成立则加入硫酸后溶液中既含有三价铁离子还含有铜离子,加入足量氨水反应生成氢氧化铁红褐色沉淀;铜离子与氨水发生反应Cu2++4NH3H2O═Cu(NH3)42++4H2O,溶液变为深蓝色。故答案为:红褐色沉淀;红褐色沉淀,同时溶液呈深蓝色
氢气混有空气加热发生爆炸,所以开始先通氢气,打开止水夹生成氢气,通过后续装置充满氢气,目的是排出装置中的空气,检验最后U型管出来的气体氢气纯度,气体纯净后再点燃C处的酒精喷灯,反应完成后先撤酒精灯,玻璃管冷却再停氢气,操作位熄灭C处的酒精喷灯,待C处冷却至室温后,关闭止水夹,防止生成的铜被空气中氧气氧化,所以其排列顺序是①⑤③④②;故答案为:①⑤③④②;检验装置中氢气的纯度
(2) CuO和Fe3O4都能被H2氧化生成相应的金属和水,所以减少的质量为氧元素的质量为1.1g。
如果全部是氧化铜,其质量应该为1.1g![]() 80/16=5.5g>4.7g; 如果全部是Fe3O4,其质量应该为1.1g
80/16=5.5g>4.7g; 如果全部是Fe3O4,其质量应该为1.1g![]() 232/64=4.0g<4.7g,所以假设3成立。答案:3
232/64=4.0g<4.7g,所以假设3成立。答案:3


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的( )
①常温常压下,11.2 L乙烷所含的分子数为0.5NA
②14.2g 硫酸钠固体中含有0.1NA个硫酸钠分子:
③常温下,21gC3H6和C4H8的混合物中含有的碳原子数为1.5NA
④2gD216O中含有的质子数、中子数、电子数均为NA
⑤标准状况下,由H2O2分解制得4.48LO2转移的电子数目为0.2NA
⑥10ml 18mol/L 的浓硫酸与足量的镁反应时转移的电子数为0.18NA
A. ③④ B. ①⑥ C. ④⑤⑥ D. ①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法
(1)用活性炭还原法可以处理氨氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)![]() N2(g)+CO2(g) △H=Q kJ· mol-1。
N2(g)+CO2(g) △H=Q kJ· mol-1。
在T℃时,反应进行到不同时间测得各物质的浓度如下表。
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min 内,NO 的平均反应速率v(NO)=___________。
T1 ℃时,该反应的平衡常数K=___________。
②30min 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母)。___________。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min 后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5∶3 ∶3,则Q________0(填“>”、“=”或“<”)。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图甲所示。
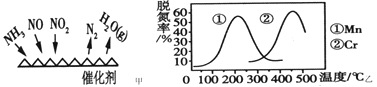
①由图甲可知,SCR技术中的氧化剂为___________。已知c(NO2)∶c(NO)=1∶1时脱氮效果最佳,若生成1mol N2时反应放出的热量为QkJ。此时对应的脱氮反应的热化学方程式为___________。
②图乙是不同催化剂Mn 和Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应的温度分别为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu3N 具有良好的电学和光学性能在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工程等领域中,发挥着广泛的、不可替代的巨大作用。
(1)C、N、O 三种元素的第一电离能由大到小的顺序为_________________。
(2)与N3-含有相同电子数的三原子分子的空间构型是____________。
(3)Cu+的电子排布式为___________,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu,但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO 为何会生成Cu2O:____________________。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙酸,乙醛分子中碳原子的杂化方式是___________,乙醛分子H-C-O的键角___________(填“大于”、“等于”或“小于”)乙醇分子中的H-C-O 的键角。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出Cu(H2O)2Cl2具有极性的分子的结构式:___________。
(6)Cu3N的晶胞结构如右图所示,N3-的配位数为___________,Cu+的半径为apm,N3-的半径为bpm,Cu3N的密度为___________g·cm-3(阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)Fe的基态原子共有________种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①已知:Cl元素在元素周期表中的位置可以描述为:第3行第17列,请用相同的形式描述Cr元素在元素周期表中的位置______________________。
②COCl2分子中所有原子均满足8电子构型,中心原子的杂化方式为________。COCl2分子中Cl—C—Cl之间的夹角______Cl—C—O之间的夹角(填“>”、“<”或“=”)。
(3)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
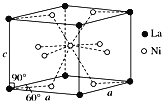
①该晶体的化学式为________________。
②已知该物质的摩尔质量为M g·mol-1,密度为d g·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是________nm3(用含M、d、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于镁合金具有硬度大、密度小、散热性好、抗震性好等优异性能它被用于制笔记本电脑外壳、竞赛自行车车架等。现称取一定质量的镁铝合金样品放入500 mL稀硫酸中,固体全部溶解并放出气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

(1)合金中Al的质量为__________________。
(2)NaOH溶液的物质的量浓度为__________________。
(3)稀硫酸的物质的量浓度为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,卤化银(AgX,X=Cl,Br)的2条溶解平衡曲线如图所示,已知AgCl,AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用pX-pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是
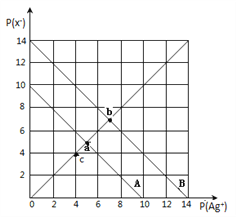
A. t℃时,c点可表示AgCl的不饱和溶液
B. B线表示的是AgBr
C. 取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定无白色沉淀生成
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈104
AgBr(s)+Cl-(aq)平衡常数K≈104
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com