
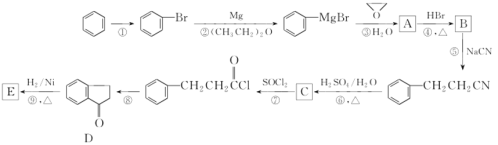
【题目】芳香族化合物 E 是合成某种香料的中间体 ,以苯为原料合成 E 流程如下 :
已知:CH3Br![]() CH3 MgBr
CH3 MgBr 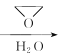 CH3CH 2CH2OH;
CH3CH 2CH2OH;
![]()
![]()
![]()
(1)写出反应①所需的试剂和条件______;
(2)化合物A中碳原子的杂化类型为_____, 分子中不同化学环境的氢原子共有___种;
(3)D中含氧官能团的名称为______;
(4)写出反应⑨的化学方程式_____,该反应的反应类型为_____;
(5)化合物C能与Na2CO3溶液反应生成CO2,符合以下 a 、b 、c、d条件的C的同分异构体与足量NaOH溶液反应的化学方程式___;
a.属于芳香族化合物 b.能发生银镜反应,也能发生水解反应 c. 结构中存在乙基 d苯环上的一氯代物只有 2 种
(6)以![]() 为主要原料,合成
为主要原料,合成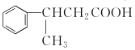 的流程为_________。
的流程为_________。
【答案】Br2/Fe(或Br2/FeBr3) sp2、sp3 6 羰基 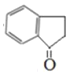 +H2
+H2![]()
 加成反应
加成反应 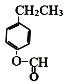 +2NaOH→
+2NaOH→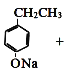 HCOONa+H2O
HCOONa+H2O ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
根据已知信息:CH3MgBr 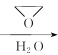 CH3CH2CH2OH;则
CH3CH2CH2OH;则![]() ,所以A是
,所以A是![]() ;
;![]() 与HBr发生取代反应生成B,B是
与HBr发生取代反应生成B,B是![]() ;
;![]() 在酸性条件下水解为羧酸C,C是
在酸性条件下水解为羧酸C,C是![]() ;
;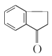 与氢气发生加成反应生成E,E是芳香族化合物,所以E的结构简式是
与氢气发生加成反应生成E,E是芳香族化合物,所以E的结构简式是 ,据此分析解答。
,据此分析解答。
(1)根据流程图示所示,反应①为苯与液溴用铁做催化剂,发生取代反应反应生成溴苯和溴化氢。所需的试剂和条件Br2/Fe(或Br2/FeBr3);
(2)A是![]() ,A中含有苯环为平面结构,苯环上的碳原子的杂化类型为sp2杂化,与苯环相连的碳原子都是饱和碳原子,类似于甲烷的结构,-CH2CH2OH上的碳原子的杂化类型为sp3;A分子结构对称,所以共有6种不同化学环境的氢原子;
,A中含有苯环为平面结构,苯环上的碳原子的杂化类型为sp2杂化,与苯环相连的碳原子都是饱和碳原子,类似于甲烷的结构,-CH2CH2OH上的碳原子的杂化类型为sp3;A分子结构对称,所以共有6种不同化学环境的氢原子;
(3)D的结构简式为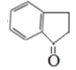 ,其中含氧官能团的名称是羰基;
,其中含氧官能团的名称是羰基;
(4)反应⑨为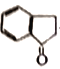 与氢气发生加成反应生成
与氢气发生加成反应生成 的化学方程式是
的化学方程式是 +H2
+H2![]()
 ;
;
(5)化合物C的同分异构体属于芳香族化合物,含有苯环;能发生银镜反应,也能发生水解反应,说明属于甲酸酯,存在乙基(-CH2CH3),且苯环上的一氯取代物只有两种,说明两个取代基位于苯环对位;符合条件的![]() 的同分异构体是
的同分异构体是 ,
, 与氢氧化钠反应的方程式是
与氢氧化钠反应的方程式是 +2NaOH→
+2NaOH→ HCOONa+H2O;
HCOONa+H2O;
(6)根据![]()
![]()
![]() ,
,![]() 可以先还原为
可以先还原为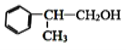 ,
,![]() 与溴化氢发生取代反应生成
与溴化氢发生取代反应生成![]() ,
,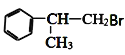 与NaCN反应生成
与NaCN反应生成 ,
, 在酸性条件下水解为
在酸性条件下水解为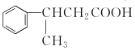 ,流程图为:
,流程图为:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】最新科技研究成果表明磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的循环寿命,该电池放电时的反应为![]() 。某磷酸铁锂电池的切面如下图所示。下列说法不正确的是( )。
。某磷酸铁锂电池的切面如下图所示。下列说法不正确的是( )。
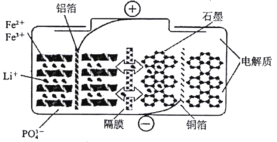
A.放电时,电池负极反应为:![]()
B.充电时,阳极上发生的反应为:![]()
C.放电时,Li+脱离石墨,经电解质嵌入负极
D.充电时,电子从电源负极流出经铜箔流入阴极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素中电负性最大的为_________(填元素符号)。
(2)下列关于CH4和CO2的说法不正确的是_________(填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是非极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp2
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的核外电子排布式为_______,Ni元素位于元素周期表的第_________族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有_________molσ键。
③某镍白铜合金的立方晶胞结构如图所示。
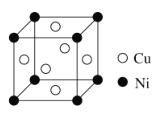
该晶体中距离Ni原子最近的Cu原子有_________个,若合金的密度为dg/cm3,阿伏加德罗常数的数值为NA,晶胞边长a=_________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组在某温度下测定溶液的pH时发现0.01mol/L 的NaOH溶液中,由水电离出的c(H+)c(OH-)=10-22,该探究小组将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1:10混合,混合后所得溶液恰好呈中性,若x=![]() y,则x为( )
y,则x为( )
A.2B.3C.4D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中将CO2与含少量CO的H2混合生成甲醇,反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),下图表示按![]() 分别为①1:4和②1:6两种投料比时,CO2的平衡经随温度变化的曲线。
分别为①1:4和②1:6两种投料比时,CO2的平衡经随温度变化的曲线。
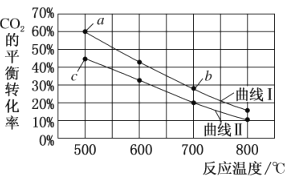
设①②两种投料比时CO2投料的物质的量浓度相等。下列有关说法正确的是
A.按投料比①时,CO2的平衡转化率随温度变化的曲线对应的是图中的曲线l
B.图中a点对应的H2的转化率为30%
C.图中b点对应的平衡常数K的值大于c点
D.![]() 的数值,a点比c点小
的数值,a点比c点小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. 氮原子的价电子排布图:![]()
B. 2p和3p轨道形状均为哑铃形,能量也相等
C. 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
D. 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫脲(![]() )是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
)是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
(1)硫脲中硫的化合价为_______;与硫脲互为同分异构且能与FeCl3溶液发生显色反应的化合物的化学式为_______
(2)可用H2NCN(氨基腈)与C2H5SH (乙硫醇)反应制备硫脲。氨基腈的电子式为_____
(3)制取氨基腈的传统工艺流程如下:
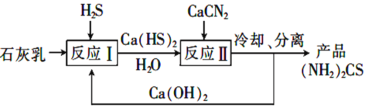
①反应Ⅱ的化学方程式为______
②测定硫脲含量的方法如下:
步骤1 :准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00 mL配制好的溶液注入碘量瓶中,加入V1 mL c1 mol/L I2的标
准溶液及适量的NaOH溶液,于暗处放置10 min(2NaOH+I2=NaIO+NaI+H2O,
4NaIO+(NH2)2CS+H2O =(NH2)2CO+4NaI+H2SO2)。
步骤3:加水及适量的盐酸,摇匀。
步骤4:用c2 mol/L标准Na2S2O2溶液滴定剩余的I2( I2+2Na2S2O2=2NaI+Na2S4O6) ,加入淀粉溶液,滴定至终点时消耗Na2S2O2溶液V2mL。
“步骤3”加入盐酸的目的_________(用离子方程式说明)。
“步骤4”滴定至终点时的颜色变化是________。
③产品中(NH2)2CS的质量分数为_______ (列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+![]() CO(g)═
CO(g)═![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g)△H2
CO2(g)△H2
Fe3O4(s)+CO(g)═3Fe(s)+CO2(g)H3
Fe2O3(s)+CO(g)═2Fe(s)+3CO2(g)H4
则△H4的表达式为__________(用含△H1、△H2、△H3的代数式表示).
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为__________,该温度下若测得固体混合物中m(Fe):m(O)=35:2,则FeO被CO还原为Fe的百分率为__________(设其它固体杂质中不含Fe、O元素).
(3)铁等金属可用作CO与氢气反应的催化剂.已知某种催化剂可用来催化反应CO(g)+3H2(g)CH4(g)+H2O(g)△H<0.在T℃,106Pa时将lmolCO和3molH2加入体积可变的密闭容器中.实验测得CO的体积分数x(CO)如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断CO(g)+3H2(g)![]() CH4(g)+H2O(g)达到平衡的是__________(填序号).
CH4(g)+H2O(g)达到平衡的是__________(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为__________;在T℃106Pa时该反应的压强平衡常数Kp(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为__________;
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是__________,理由是__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素,是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为:

请回答下列问题:
(1)对青蒿进行干燥、破碎的目的是_______。
(2)操作I需要的玻璃仪器主要有:烧杯、漏斗、______,操作Ⅱ的名称是_____。
(3)操作Ⅲ的主要过程可能是_______(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)某学生对青蒿素的性质进行探究:将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_____(填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com