
【题目】用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成原电池——燃料电池,该电池放电时发生的反应为CH4+2KOH+2O2===K2CO3+3H2O,下列说法错误的是( )
A. 通甲烷的一极为负极,通氧气的一极为正极
B. 放电时,通入O2一极附近溶液的pH升高
C. 放电一段时间后,KOH的物质的量不发生变化
D. 通甲烷极的电极反应式是:CH4+10OH--8e-===CO32-+7H2O
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol ![]() 的能量(kJ)相对大小如下图所示。下列有关说法错误的是
的能量(kJ)相对大小如下图所示。下列有关说法错误的是

A. 上述离子中结合![]() 能力最强的是E
能力最强的是E
B. 上述离子中最稳定的是A
C. 上述离子与![]() 结合有漂白性的是B
结合有漂白性的是B
D. ![]() 反应物的键能之和小于生成物的键能之和
反应物的键能之和小于生成物的键能之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
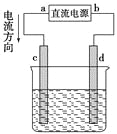
A. a为负极,b为正极
B. a为阳极,b为阴极
C. 电解过程中,d电极质量增加
D. 电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两份体积相同的某植物营养液,其配方分别如下:
KCl | K2SO4 | ZnSO4 | |
① | 0.3 mol·L-1 | 0.2 mol·L-1 | 0.1 mol·L-1 |
② | 0.1 mol·L-1 | 0.3 mol·L-1 | — |
下列对这两份营养液成分的分析中正确的是( )
A. K+的物质的量相同
B. Cl-的物质的量相同
C. 完全相同
D. SO![]() 的物质的量不同
的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2Fe(SO4)26H2O(M=392g/mol)又称摩尔盐,简称FAS,它是浅蓝色绿色晶体,可溶于水,难溶于水乙醇。某小组利用工业废铁屑进行下列实验。请按要求回答下列问题:
Ⅰ. FAS的制取。流程如下:

(1)步骤①加热的目的是_________________________。
(2)步骤②必须在剩余少量铁屑时进行过滤,其原因是(用离子方程式表示): ______________。
Ⅱ.NH4+含量的测定。装置如图所示:

实验步骤:①称取FAS样品a g,加水溶解后,将溶液注入Y中
②量取b mL c1 mol/LH2SO4溶液于Z中
③向Y加入足量NaOH浓溶液,充分反应后通入气体N2,加热(假设氨完全蒸出),蒸氨结束后取下Z。
④用c2mol/LNaOH标准溶液滴定Z中过量的硫酸,滴定终点时消耗d mLNaOH标准溶液。
(3)仪器X的名称______________;N2的电子式为______________。
(4)步骤③蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行处理的操作是__________________;NH4+质量百分含量为(用代数式表示)__________________。
Ⅲ. FAS纯度的测定。称取FAS m g样品配制成500 mL待测溶液。分别取20.00mL待测溶液,进行如下方案实验:
(5)方案一:用0.01000mol/L的酸性KMnO4溶液进行滴定。滴定过程中需用到的仪器中(填图中序号)_________。滴定中反应的离子方程式为____________________。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(6)方案二: 待测液 ![]() 固体n g ;则FAS的质量百分含量为(用代数式表示)_____________________________。
固体n g ;则FAS的质量百分含量为(用代数式表示)_____________________________。
(7)方案一、二实验操作均正确,却发现方案一测定结果总是小于方案二的,其可能的原因是_______________;为验证该猜测正确,设计后续实验操作为_________________,现象为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾可做净水剂的原因:_______________________________________________(请用相关的化学用语和文字描述),若向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是_________________________,有关的离子方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓盐酸和二氧化锰共热制取氯气,现要制取一瓶干燥纯净的氯气,并防止剩余氯气逸出污染空气。现有下列仪器和药品可使用:

(1)盛装浓盐酸的仪器名称_______
(2)连接上述仪器的正确顺序是(填各接口处的字母)A接______,______接______,______接______,______接______。
(3)气体尾气吸收装置中进行的化学反应方程式为________
(4)在装置中,①饱和食盐水的作用是______②浓硫酸的作用是______③氢氧化钠溶液的作用是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂制备净水剂硫酸铁铵晶体[NH4Fe(SO4)2·6H2O]的一种方案如下:

下列说法不正确的是
A. 滤渣A的主要成分是CaSO4
B. 相同条件下,NH4Fe(SO4)2·6H2O净水能力比FeCl3强
C. “合成”反应要控制温,温度过高,产率会降低
D. “系列操作”包括蒸发浓缩、降温结晶、过滤、干燥等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有 Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法正确的是

A. 若原溶液中不存在 Na+,则 c(Cl-)<0.1molL﹣1
B. 原溶液可能存在 Cl- 和 Na+
C. 原溶液中 c(CO32-)是 0.01molL﹣1
D. 原溶液一定存在 CO32-和SO42-,一定不存在 Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com