
����Ŀ����������(NaNO2)��һ�ֳ�����ʳƷ���Ӽ���ij��ȤС������ͼ��ʾװ���Ʊ�NaNO2����������������̽��(A�м���װ������ȥ)��

�������Ͽ�֪��
��2NO+Na2O2=2NaNO2��2NO2+Na2O2=2NaNO3��
��NO�ܱ�����KMnO4������NO3-��
�������������£�NaNO2�ܽ�I-����ΪI2��S2O32-�ܽ�I2��ԭΪI-����I2+2S2O32-=2I-+S4O62-���з�Ӧ�Ļ�ѧ����ʽ��
(1)װ��������a������Ϊ______________��A�з�Ӧ�Ļ�ѧ����ʽ��_______________��
(2)װ��B�й۲쵽����Ҫ������_____________________��
(3)װ��C��ʢ�ŵ��Լ���______________________��
(4)װ��E��������___________________��
(5)A�е���Ũ����֮ǰ��Ӧ��ͨ��N2һ��ʱ�䣬ԭ����__________________��
(6)Ϊ�ⶨ����NaNO2�Ĵ��ȣ�ȷ��ȡmgNaNO2��Ʒ������ƿ�в���������ˮ�ܽ⣬�ټ������KI��Һ�����뼸�ε�����Һ��Ȼ��μ�ϡ���ᣬ��cmol/LNa2S2O3��Һ�ζ����յ㣬�ظ�����2~3�Σ�ƽ������Na2S2O3V ml���ζ��յ��������___________________������Ʒ��NaNO2����������Ϊ__________��
���𰸡� ������ƿ C+4HNO3(Ũ) ![]() CO2��+4NO2��+2H2O ��Һ������ͭƬ�ܽ⣬����ɫ����ð�� ��ʯ��(������ʯ��) �����ж���NO���壬��ֹ��Ⱦ���� ����װ���еĿ�����������Ʒ�Ӧ���²�Ʒ���� ��Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ
CO2��+4NO2��+2H2O ��Һ������ͭƬ�ܽ⣬����ɫ����ð�� ��ʯ��(������ʯ��) �����ж���NO���壬��ֹ��Ⱦ���� ����װ���еĿ�����������Ʒ�Ӧ���²�Ʒ���� ��Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ ![]() %
%
�����������������(1)����װ��ͼ��������a����������װ��A��Ũ������̼�ڼ���ʱ����������ԭ��Ӧ�����ɶ���������������̼��ˮ��(2)��װ��B��NO2����ˮ�������ᣬ��������ͭ��Ӧ��������ͭ��һ��������ˮ��(3)NO��������̼��ˮ������������Ʒ�Ӧ������Cװ�õ������dz�ȥNO�еĶ�����̼��ˮ��(4)NO��Ⱦ������װ��E��������β��������(5) �����еĶ�����̼��������Ʒ�Ӧ�����ɵIJ�Ʒ������(6)NaNO2�ܽ�I-����ΪI2�����ӷ���ʽ��![]() ��S2O32-�ܽ�I2��ԭΪI-�����ӷ���ʽ��I2+2S2O32-=2I-+S4O62-���ﵽ�ζ��յ�ʱ���ⵥ�ʱ���ȫ���������ݹ�ϵʽNaNO2
��S2O32-�ܽ�I2��ԭΪI-�����ӷ���ʽ��I2+2S2O32-=2I-+S4O62-���ﵽ�ζ��յ�ʱ���ⵥ�ʱ���ȫ���������ݹ�ϵʽNaNO2![]() S2O32-����NaNO2������������
S2O32-����NaNO2������������
������(1)����װ��ͼ������a��������������ƿ����װ��A��Ũ������̼�ڼ���ʱ����������ԭ��Ӧ�����ɶ���������������̼��ˮ����Ӧ����ʽ��C+4HNO3(Ũ) ![]() CO2��+4NO2��+2H2O��(2)��װ��B��NO2����ˮ�������ᣬ��������ͭ��Ӧ��������ͭ��һ��������ˮ������װ��B�й۲쵽����Ҫ��������Һ������ͭƬ�ܽ⣬����ɫ����ð����(3)NO��������̼��ˮ������������Ʒ�Ӧ������Cװ�õ������dz�ȥNO�еĶ�����̼��ˮ��װ��C��ʢ�ŵ��Լ��Ǽ�ʯ����(4)NO��Ⱦ������NO�ܱ�����KMnO4������NO3-��װ��E��������β����������ֹ��Ⱦ������(5)�����еĶ�����̼��������Ʒ�Ӧ�����ɵIJ�Ʒ����������A�е���Ũ����֮ǰ��Ӧ��ͨ��N2һ��ʱ����(6)NaNO2�ܽ�I-����ΪI2�����ӷ���ʽ��
CO2��+4NO2��+2H2O��(2)��װ��B��NO2����ˮ�������ᣬ��������ͭ��Ӧ��������ͭ��һ��������ˮ������װ��B�й۲쵽����Ҫ��������Һ������ͭƬ�ܽ⣬����ɫ����ð����(3)NO��������̼��ˮ������������Ʒ�Ӧ������Cװ�õ������dz�ȥNO�еĶ�����̼��ˮ��װ��C��ʢ�ŵ��Լ��Ǽ�ʯ����(4)NO��Ⱦ������NO�ܱ�����KMnO4������NO3-��װ��E��������β����������ֹ��Ⱦ������(5)�����еĶ�����̼��������Ʒ�Ӧ�����ɵIJ�Ʒ����������A�е���Ũ����֮ǰ��Ӧ��ͨ��N2һ��ʱ����(6)NaNO2�ܽ�I-����ΪI2�����ӷ���ʽ��![]() ��S2O32-�ܽ�I2��ԭΪI-�����ӷ���ʽ��I2+2S2O32-=2I-+S4O62-���ﵽ�ζ��յ�ʱ���ⵥ�ʱ���ȫ���ģ��ﵽ�ζ��յ����������Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ��
��S2O32-�ܽ�I2��ԭΪI-�����ӷ���ʽ��I2+2S2O32-=2I-+S4O62-���ﵽ�ζ��յ�ʱ���ⵥ�ʱ���ȫ���ģ��ﵽ�ζ��յ����������Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ��
��NaNO2��������xg��
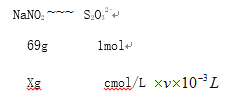
X= ![]()
NaNO2������������![]() =
=![]() %��
%��


 һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д� ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2 L���ܱ������н������·�Ӧ��A(g)��2B(g)![]() 3C(g)��2D(g)����ʼʱAΪ4 mol��BΪ6 mol��5 minĩʱ���C�����ʵ���Ϊ3 mol������㣺
3C(g)��2D(g)����ʼʱAΪ4 mol��BΪ6 mol��5 minĩʱ���C�����ʵ���Ϊ3 mol������㣺
��1��5minĩA�����ʵ���Ũ��___________________��
��2��5min��D��ƽ����ѧ��Ӧ����____________________��
��3��B��ת����_____________________________��
��4����Ӧ�������е���ѹǿ�뷴Ӧǰ��ѹǿ֮��Ϊ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ��С��ͬѧ��������װ���Ʊ���������̽������������(������������ȥ)����ش�

(1)ʵ�����Ʊ������Ļ�ѧ����ʽΪ__________��
(2)��װ��B�ռ�����ʱ��Ӧѡ�����Ľ�������_____(ѡ�a����b��)����˵��ѡ���������___________��
(3)��װ��B�е�ֹˮ��c�����۲쵽Բ����ƿ�ڲ����˺�ɫ��Ȫ����˵���������е�������_________��_________��
(4)Ϊ��ֹ��Ⱦ����������װ��(ʢ�ŵ�Һ���Ϊˮ)���������ն��ఱ������_____(�����)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ç��������ںϳ�ҩ���ƣ���ṹ��ʽ��ͼ�����й���ç�����˵����ȷ���ǣ� ��

A. ����ʽΪC7H6O5
B. �����к���2�ֹ�����
C. �ɷ����ӳɺ�ȡ����Ӧ
D. ��ˮ��Һ���Ȼ����ǻ����ܵ����H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪһ����Ȼ�������һ���ij��ݹ�Ч�������йظû������˵���������

A. �����к������ֺ���������
B. 1mol�û������������4molNaOH��Ӧ
C. �ȿ��Է���ȡ����Ӧ�����ܹ������ӳɷ�Ӧ
D. ������FeCl3������ɫ��Ӧ��Ҳ�ܺ�NaHCO3��Ӧ�ų�CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӹ����������仯�������������������е����÷����˾�仯��
��1���Ŵ��й��Ĵ���֮һ��ָ����������Ȼ��ʯ�Ƴɵģ�����Ҫ�ɷ���______������ĸ��ţ���
a��Fe b��FeO c��Fe3O4 d��Fe2O3
��2������������Ҫ��ѧ�ɷ�Ϊ��SiO2Լ45%��Fe2O3Լ40%��Al2O3Լ10%��MgOԼ5%���ø÷�����ȡҩ�ø��ϡ������������Ĺ����������£����ֲ����������ԣ���
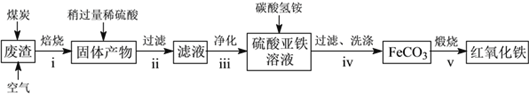
�ش��������⣺
���ڲ���i�в������ж����������__________________��
���ڲ���iii�����У�Ҫ��ȥ������֮һΪAl3����������ʱKsp[Al(OH)3]=1.0��10��32����ʱ�����Ͻ�Al3��������ȫ������Һ��pHΪ____________��
�۲���iv�У�����FeCO3�����ӷ���ʽ��_________________��
��3���Ȼ�����Һ��Ϊ��ѧ�Լ��еġ������֡������Ȼ�ͭ���Ȼ����Ļ����Һ�м�������ͭ��ĩ������µij�����д���ó����Ļ�ѧʽ_________________������ƽ���ƶ���ԭ������ϱ�Ҫ�����ӷ���ʽ���Դ������������ͣ�___________________��
��4���ٹ��϶��������ɫȾ����³ʿ���ĺϳɷ������£�

���ֽⷴӦii�����ӷ���ʽ��________________��
����������³ʿ���ϳ�ԭ���ɼ��ʳƷ��CN�����������£�
![]()
����ֽ������֤��ʳƷ�к���CN��������ͼ��ʱ��ֽ��FeSO4�����ã�
_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʳƷ������Ӧ������ζ���������Ѻá����п�����ʳƷ��װ���������������ǣ� ��
A.�轺B.����C.CaOD.KMnO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������̿����Ҫ�ɷ�MnO2������SiO2 ��Fe2O3��Al2O3��Cu2(OH)2CO3�ĵ����ʣ�����ϴ������Һ����1mol/LH2SO4��FeSO4��Һ���������������̺����죨Fe2O3��������������
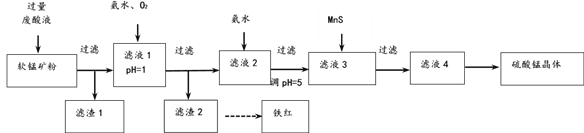
Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | |
��ʼ����ʱ | 8.3 | 6.3 | 4.7 | 3.4 | 2.7 |
��ȫ����ʱ | 9.8 | 8.3 | 6.7 | 4.4 | 3.2 |
��1�������ʵ����̿�ʹ��ǰ�轫����飬Ŀ����______��
��2������1�к��е���Ҫ������_______��
��3����Һ1�У��Ӱ�ˮ������ҺpH��3.2��ͨ��O2����Ӧ�����ӷ���ʽ��_______������H2O2����O2���Ƿ������������___________��
��4�����̿�������������������Һ��Ӧ�����ӷ���ʽ��_________��
��5����Һ3�м������ܵ����MnS��Ŀ���ǣ������ӷ���ʽ��ʾ��_________��
��6�����ؽᾧ������Һ4�л�ȡ�����̾���IJ����ǣ�__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�� ʱ,��0.10mol��L-1������ֱ�ζ������ͬ��Ũ�Ⱦ�Ϊ0.10mol��L-1������һԪ��XOH��YOH��ZOH,�ζ�������ͼ��ʾ��
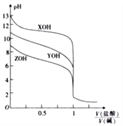
����˵����ȷ���ǣ� ��
A. YOH��ǿ�� B. 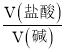 =0.5ʱ��c(Z+)>c(Y+)>c(X+)
=0.5ʱ��c(Z+)>c(Y+)>c(X+)
C. X++H2O![]() XOH+H+��ƽ�ⳣ��K=10-4 D. �ζ�XOHʱ���÷�̪��ָʾ��
XOH+H+��ƽ�ⳣ��K=10-4 D. �ζ�XOHʱ���÷�̪��ָʾ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com