
【题目】镍-铁碱性电池十分耐用,但其充电过程中正负极得到的产物对电解水有很好的催化作用,因此电池过充时会产生氢气和氧气,限制了其应用。科学家将电池和电解水结合在起,制成新型的集成式电池电解器,可将富余的能量转化为氢能储存。已知镍铁碱性电池总反应方程式为:Fe+2NiOOH+2H2O![]() Fe(OH)2+2Ni(OH)2。下列有关说法错误的是( )
Fe(OH)2+2Ni(OH)2。下列有关说法错误的是( )
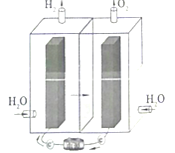
A.电能、氢能属于二次能源
B.该储能装置中的交换膜为阴离子交换膜
C.该装置储氢能发生的反应为:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.镍-铁碱性电池放电时正极的反应为:Ni(OH)2+OH--e-═NiOOH+H2O
科目:高中化学 来源: 题型:
【题目】有机物X是一种重要的有机化工原料,如图所示是以有机物X为原料设计的合成路线(部分产物、个别合成路线、反应条件等略去)。
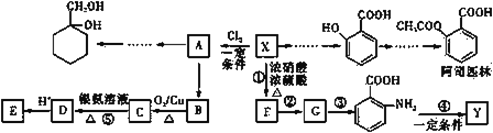
已知:i.X为芳香烃,其相对分子质量为92;Y是一种功能高分子材料。
ii.烷基苯在酸性高酸钾的作用下,侧链被氧化成羧基:
![]()
iii.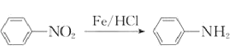 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X 结构简式为______。阿司匹林中官能团的名称为______。
(2)反应③的反应类型是______;反应②和③的顺序不能交换的原因是______。
(3)Y 的结构简式为______。
(4)已知 A 为一氯代物。反应⑤的离子方程式为______。
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有______种。
①芳香族化合物;
②不能发生水解反应,也不能发生银镜反应;
③1mol该有机物最多能与 2 mol NaHCO3完全反应。
(6)写出以 A 为原料制备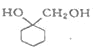 的合成路线流程图(其它试剂任选)_________________。
的合成路线流程图(其它试剂任选)_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】5﹣二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5﹣二甲氧基苯酚的部分物理性质见下表:
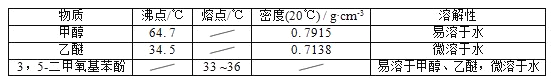
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取,①分离出甲醇的操作是的______;②萃取用到的分液漏斗使用前需__________________并洗净,分液时有机层在分液漏斗的________填(“上”或“下”)层;
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3溶液洗涤的目的是__,用饱和食盐水洗涤的目的是______;
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是__(填字母);
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤.为了防止倒吸,减压过滤完成后应先________________,再______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中![]() >1
>1
D.向0.1molL-1CH3COOH 溶液中加入少量水,溶液中 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是
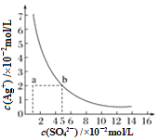
A. 含有大量SO42-的溶液中肯定不存在Ag+
B. Ag2SO4的溶度积常数(Ksp)为1×10-3
C. 0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
D. a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2+2S2O32-=S4O62-+2I-;CuI是不溶于水的白色沉淀。
相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入_________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是(用文字叙述):____________________________________________。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是______________________________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用_______________作滴定指示剂,滴定终点的现象是________________________。
②CuCl2溶液与KI反应的离子方程式为___________________________________________。
③该试样中CuCl2·2H2O的质量百分数为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,在CH3COONa稀溶液中分别加入少量下列物质:
①固体NaOH;②固体KOH;③固体NaHSO4;④固体CH3COONa;⑤冰醋酸
其中一定可使c(CH3COO-)/c(Na+)比值增大的是 ( )
A. ①② B. ②⑤ C. ①⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
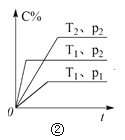
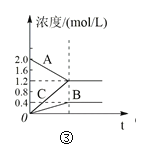
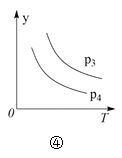
【题目】下列叙述与下图对应的是( )
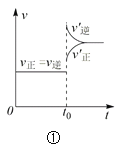
A.对于达到平衡状态的N2(g) + 3H2(g) 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动
B.由图②可知,p2 > p1,T1 > T2满足反应:2A(g) + B(g) 2C(g) ΔH < 0
C.图③表示的反应方程式为2A = B + 3C
D.对于反应2X(g) + 3Y(g) 2Z(g) ΔH < 0,图④y轴可以表示Y的百分含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物的下列说法正确的是
A.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
B.等质量的乙烯和甲烷燃烧时,乙烯消耗氧气多
C.苯分子中的碳碳键为单键与双键交替存在
D.乙烯和乙烷可用溴水来鉴别
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com