
【题目】关于NaHCO3性质的有关叙述正确的是( )
A. 只能与强酸反应,不能与强碱反应
B. 医疗上可用于治疗胃酸过多
C. 与足量的酸反应时放出的CO2比等质量的Na2CO3要少
D. 同温度时,NaHCO3的溶解度>Na2CO3的溶解度
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
【题目】与下图图像有关的叙述,正确的是

A. 表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量
B. 表示的热化学方程式为:H2(g)+ 1/2 O2(g) = H2O(g) △H= -241.8 kJ·mol-1
C. 表示2 mol H2(g)所具有的能量一定比2 mol气态水所具有的能量多483.6 kJ
D. H2O(g)的能量低于H2(g)和O2(g)的能量之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.氮氧化物、二氧化硫是造成大气污染的主要物质,某科研小组进行如下研究。
(1)写出SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热化学方程式_____________。
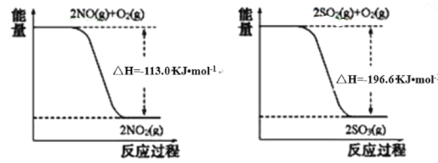
(2)常温下用NaOH溶液吸收SO2,当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,利用图所示装置(电极均为惰性电极)在pH为4~7之间电解,可使NaHSO3转化为Na2S2O4,并获得较浓的硫酸,这是电化学脱硫技术之一,
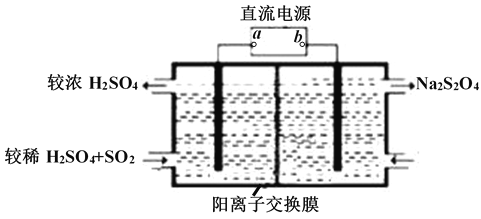
①a为电源的_______(填 “正极”或“负极”);
②阴极的电极反应式为______
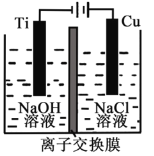
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,反应为2Cu + H2O ==Cu2O + H2↑。装置如图所示:该离子交换膜为__________离子交换膜(填“阴”或“阳”),该电池的阳极反应式为:____________________,钛极附近的pH_______ (增大、减小、不变)。
Ⅲ.氢氧燃料电池是符合绿色化学理念的新型发电装置。右图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。
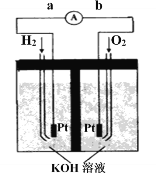
①氢氧燃料电池的能量转化主要形式是________,工作时电流方向为_______(用a→b或b→a表示)。
②负极的电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
(4)以下收集NO气体的装置,合理的是________(填序号)。
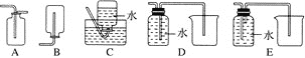
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH和Na2CO3混和物配制成100mL溶液,其中c(Na+) =0.5mol/L。在该溶液中加入过量盐酸反应完全后,将溶液蒸干后所得固体质量为( )
A.2.925 gB.5.85 gC.6.56 gD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容下.将l molX和2 molY置于密闭容器中发生反应:X(s)+2Y(g)![]() 2Z(g),10 min后达到平衡状态,下列说法正确的是
2Z(g),10 min后达到平衡状态,下列说法正确的是
A. 平衡前,容器中压强随反应进行而减小
B. 平衡后,容器中Y和Z的物质的量之比一定为1:1
C. 10 min后,升高温度,Y的反应速率不变
D. 生成Z的物质的量一定小于2 moI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 为短周期主族元素,其原子序数依次增大;B、C、D、E 位于同一周期; A 的简单气态氢化物可以用作制冷剂;1 mol B 单质与足量盐酸反应生成气体在标准状况下的体积为33.6 L;D 原子最外层电子数与核外电子总数之比为 3∶8;C 的原子子序数是 A 的两倍。
(1)A、B 简单离子半径由大到小的顺序为______________ (填离子符号) 。
(2)C 在元素周期表中的位置是_______________ 。
(3)A 的简单气态氢化物接触到 E 的简单气态氢化物时可观察到的现象是_____________。
(4) D 与 E 可形成原子个数比为 1∶2 的化合物,其电子式为________。
(5)C、D、E 最简单气态氢化物稳定性由高到低的顺序是___________ (用化学式表达 )。
(6)B 与 D 形成的化合物遇水迅速水解,写出该反应的化学方程式_______________________。
(7)若 E 单质与 NaOH 溶液反应生成 NaE、NaEO 和 NaEO3,则 30mL 2mol/LNaOH 与_____mol E 单质恰好完全反应(忽略 E 单质与水的反应及盐类的水解反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.水不能用来分离溴苯和苯的混合物
B.苯和甲苯都能发生取代反应
C.氯乙烯和乙二醇都能用来作为合成高分子化合物的原料
D.等物质的量的乙烯和乙醇分别完全燃烧,乙醇消耗氧气多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】膳食中的钠主要存在于食盐中,它是烹饪中重要的调味品,也是保证肌体水分平衡的最重要物质。钠缺乏症可造成生长缓慢、食欲减退。由于失水体重减轻、肌肉痉挛、恶心、腹泻和头痛。膳食中长期摄入过多的钠将导致高血压。这里涉及到的钠指的是( )
A.钠单质B.食盐C.钠离子D.碳酸氢钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com