
【题目】2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图所示)可用于ⅢB族元素对应的离子萃取,如La2+、Sc2+。写出基态二价钪离子(Sc2+)核外电子排布式:__________。其中电子占据的轨道数为__________个。
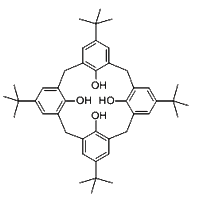
(2)对叔丁基杯[4]芳烃由4个烃基构成杯底,其中条件氧原子的杂化方式为___________。烃基间的相互作用力为_______________。
(3)不同大小的杯芳烃能识别某些离子,如:N3-、SCN-等。根据等电子体原料判断N3-空间构型为______;一定条件下,SCN-与MnO2反应可得到(SCN)2。试写出(SCN)2 的结构式:_______________。
(4)已知C60分子结构和C60晶胞示意图(如图Ⅱ,图Ⅲ所示):
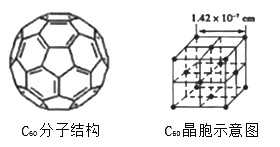
则一个C60分子中含有σ键个数为__________,与每个C60分子距离最近且相等的C60分子有_________个,C60晶体的密度为__________(计算结果保留两位小数)。
【答案】 1s22s22p63s23p63d1或[Ar]3d1 10 sp3 氢键 直线型 N≡C-S-S-C≡N 90 12 1.67g/cm3
【解析】本题考查选修三《物质结构与性质》,从基础知识入手,(1)Sc是21号元素,核外电子排布式为[Ar]3d14s2,则Sc2+的电子排布式为1s22s22p63s23p63d1或[Ar]3d1 ;s能级有1个轨道,p能级有3个轨道,d能级只有1个电子,占有1个轨道,因此电子占据的轨道有10个;(2)羟基中的氧原子,有2个σ键,2个孤电子对,因此杂化类型是sp3,羟基键通过氢键联系到一起;(3)N3-Y与CO2互为等电子体,因此N3-的空间构型为直线型;(SCN)2的结构式为N≡C-S-S-C≡N ;(4)根据C60分子结构,C60分子中1个碳原子有2个C-C键、1个"C=C",根据均摊法,一个碳原子真正含有的σ键的个数为3/2,即一个C60分子中含有σ键的个数为60×3/2=90;根据C60晶胞结构,离C60最近的C60上面有4个,中间有4个,下面有4个,即有12个;C60的个数为8×1/8+6×1/2=4,晶胞的质量为4×720/NAg,晶胞的体积为(1.42×10-7)3cm3,根据密度的定义,晶胞的密度等于为4×720/[NA×(1.42×10-7)3]g/cm3=1.67g/cm3。


科目:高中化学 来源: 题型:
【题目】某气态烃1 mol能和2 mol HCl加成得到饱和产物,其饱和产物又能和6 mol Cl2完全取代,则该烃是
A. C2H6 B. C2H2 C. C3H4 D. C4H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是( )
A.1:2 B.2:1 C.1:1 D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容容器中.可逆反应2NO(g)+O2(g)![]() 2NO2(g)△H<0,不能说明已达到平衡状态的是
2NO2(g)△H<0,不能说明已达到平衡状态的是
A. O2的消耗速率和NO2的生成速率之比为l:2
B. 反应容器中压强不随时间变化而变化
C. 混合气体颜色深浅保持不变
D. 混合气体平均分子量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某KNO3溶液中含杂质KCl和Ca(NO3)2,现欲除去杂质,得到纯净的KNO3溶液,则加入试剂的正确顺序是( )
A.AgNO3、K2CO3 B.AgNO3、K2CO3、HNO3
C.K2CO3、AgNO3 D.K2CO3、AgNO3、HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体应用与其性质的对应不正确的是( )
A.鉴别胶体与浊液(丁达尔效应) B.高压除尘(电泳现象)
C.河海交汇处可沉积沙洲(聚沉) D.喷雾剂的应用(布朗运动)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列图像的分析错误的是
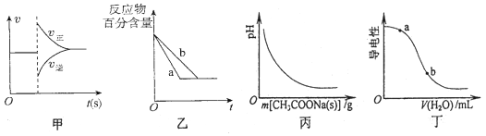
A.图甲可表示对平衡N2(g)+3H2(g)![]() 2NH3(g)加压、同时移除部分NH3时的速率变化
2NH3(g)加压、同时移除部分NH3时的速率变化
B.图乙中a、b曲线可表示反应H2(g)十I2(g)![]() 2HI(g)在有催化剂和无催化剂存在下建立平衡的过程
2HI(g)在有催化剂和无催化剂存在下建立平衡的过程
C.图丙表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化
D.图丁表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a<b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是

A. a点对应的无色溶液中能大量存在:Fe3+、Na+、Cl-、SO42-
B. b点对应的溶液中能大量存在:NH4+、Ca2+、AlO2-、I-
C. c点对应的溶液中能大量存在:Na+、Ba2+、Cl-、CO32-
D. d点对应的溶液中能大量存在:Na+、K+、SO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】定量分析是化学实验中重要的组成部分。
Ⅰ.中和热的测定:
(1)在实验室中,用50 mL 0.40 mol/L的盐酸与50 mL 0.50mol/L的NaOH溶液反应测定和热。假设此时溶液密度均为1 g/cm3,生成溶液的比容热c = 4.18 J/(g℃),实验起始温度为T1℃,终止温度为T2℃,请写出中和热的计算式(写出最后结果)△H=__________KJ/mol。
(2)1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6 kJ的热量。请写出表示该反应中和热的热化学方程式 。
Ⅱ.氧化还原滴定实验与中和滴定类似。为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。
(1)滴定原理为: (用离子方程式表示)。
(2)滴定时,KMnO4溶液应装在 (填“酸式”或“碱式”)滴定管中,达到滴定终点时的颜色变化为 。
(3)如图表示50mL滴定管中液面的位置,此时滴定管中液面的读数为 mL。
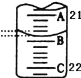
(4)为了减小实验误差,该同学一共进行了三次实验,假设每次所取H2C2O4溶液体积均为VmL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗KMnO4溶液体积/mL | 26.32 | 24.02 | 23.98 |
从上表可以看出,第一次实验中记录消耗KMnO4溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积
B.滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.第一次滴定盛装标准液的滴定管装液前用蒸馏水清洗过,未用标准液润洗,后两次均用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
(5)写出计算H2C2O4的物质的量浓度的最简表达式:C= mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com