
����Ŀ��һ�������£������Ϊ3 L���ܱ������з�ӦCO��g��+ 2H2��g��![]() CH3OH��g���ﵽ��ѧƽ��״̬��
CH3OH��g���ﵽ��ѧƽ��״̬��
��1����Ӧ��ƽ�ⳣ������ʽK=_____________��������ͼ�������¶ȣ�Kֵ��__________������������������С����������������
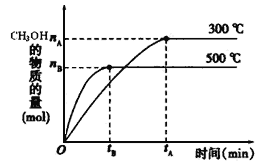
��2��500��ʱ���ӷ�Ӧ��ʼ���ﵽ��ѧƽ�⣬��H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ������__________����nB��tB��ʾ����
��3���жϸÿ��淴Ӧ�ﵽ��ѧƽ��״̬�ı�־��____________ ������ĸ����
a��v���ɣ�CH3OH��= v���ģ�CO��
b�����������ܶȲ��ٸı�
c����������ƽ����Է����������ٸı�
d��CO��H2��CH3OH��Ũ�Ⱦ����ٱ仯
��4��300��ʱ�����������ݻ�ѹ����ԭ����1/2���������������������£���ƽ����ϵ������Ӱ���ǣ�����ĸ��___________________��
a��c��H2������ b������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
c��CH3OH �����ʵ������� d������ƽ��ʱc��H2��/ c��CH3OH����С
���𰸡���1��![]() ��2�֣���С��2�֣�
��2�֣���С��2�֣�
��2��![]() mol��L-1��min-1��3�֣�
mol��L-1��min-1��3�֣�
��3��cd ��2�֣���4��cd��2�֣�
��������
���⣨1�����ݻ�ѧ��ӦCO��g��+ 2H2��g��![]() CH3OH��g������Ӧ��ƽ�ⳣ������ʽK=
CH3OH��g������Ӧ��ƽ�ⳣ������ʽK=![]() ������ͼʾ�������¶ȣ��״������ʵ������ͣ�˵��ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��
������ͼʾ�������¶ȣ��״������ʵ������ͣ�˵��ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��
��2��tBʱ���ڣ�����nBmolCH3OH��������2nBH2������c(H2)��2nB/3��v(H2)��![]() mol��L-1��min-1��
mol��L-1��min-1��
��3�����ɼ״�������CO��������Ӧ���ʣ����ܷ�Ӧ�ﵽƽ��״̬��a������������䣬������������䣬�κ�ʱ���ܶȲ��䣬b������![]() =m/n�������������䣬���ʵ������ŷ�Ӧ�Ľ��м�С����
=m/n�������������䣬���ʵ������ŷ�Ӧ�Ľ��м�С����![]() ����ʱ��Ӧ�ﵽƽ��״̬��c��ȷ���������ʵ�Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬��d��ȷ����ѡcd��
����ʱ��Ӧ�ﵽƽ��״̬��c��ȷ���������ʵ�Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬��d��ȷ����ѡcd��
��4������ѹǿƽ����������Ӧ�����ƶ��������淴Ӧ���ʶ�����H2���ʵ�����С��CH3OH���ʵ����������������С������ƽ��ʱc(H2)Ũ�ȱ�ԭƽ�������ƽ��ʱc��H2��/ c��CH3OH����С������ѡ��a��b����c��d��ȷ����ѡcd��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ���������������ԭ������ش��������⣺
(1)���淴ӦFeO(s)��CO(g)![]() Fe(s)��CO2(g)��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
Fe(s)��CO2(g)��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
T/K | 938 | 1 100 |
K | 0.68 | 0.40 |
��д���÷�Ӧƽ�ⳣ���ı���ʽ________��
�����÷�Ӧ������̶����ܱ������н��У���һ�������´ﵽƽ��״̬���������¶ȣ���������ƽ����Է�������________�����뺤�������������ܶ�________(�������С�����䡱)��
(2)�����£�Ũ�Ⱦ�Ϊ0.1 mol��L��1������������Һ��pH���±���
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
����������Һ�е������ӣ��������������ǿ����________��
�ڸ��ݱ��������жϣ�Ũ�Ⱦ�Ϊ0.01 mol��L��1�������������ʵ���Һ�У�������ǿ����________��������Һ�ֱ�ϡ��100����pH�仯��С����________(����)��
A��HCN B��HClO
C��H2CO3 D��CH3COOH
�۾��ϱ����ݣ������ж����з�Ӧ���ܳ�������________(����)��
A��CH3COOH��Na2CO3===NaHCO3��CH3COONa
B��CH3COOH��NaCN===CH3COONa��HCN
C��CO2��H2O��2NaClO===Na2CO3��2HClO
��Ҫ������ˮ��HClO��Ũ�ȣ�������ˮ�м���������̼������Һ����Ӧ�����ӷ���ʽΪ__________________________________��
(3)��֪������Cu(OH)2��Ksp��2��10��20����֪������ijCuSO4��Һ��[Cu2��]��0.02 mol��L��1�����Ҫ����Cu(OH)2��������Ӧ������ҺpH����________��Ҫʹ0.2 mol��L��1��CuSO4��Һ��Cu2��������Ϊ��ȫ( ʹCu2��Ũ�Ƚ� ��ԭ����ǧ��֮һ)��Ӧ����Һ���NaOH��Һ��ʹ��ҺpHΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��CO2�Ǻ�̼Ԫ�صij������壬Ҳ�Dz���̼ѭ������Ҫ���ʡ��о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����塣
��1��CO��������������֪��
Fe2O3(s) + 3C(s)��2Fe(s) + 3CO(g) ��H1��+489.0 kJ��mol��1��
C(s) +CO2(g)��2CO(g) ��H2��+172.5 kJ��mol��1
��CO��ԭFe2O3(s)���Ȼ�ѧ����ʽΪ______________________________��
��2���״�����Ҫ�Ļ���ԭ�ϣ�����ú������������CO��H2����ȡ�״��������ķ�ӦΪCO(g)+2H2(g) ![]() CH3OH(g)��ʵ�����У���1L���ݵ��ܱ������н���ģ��ϳ�ʵ�顣��1 mol CO��2 mol H2ͨ�������У��ֱ������300���500�淴Ӧ��ÿ��һ��ʱ����������CH3OH��Ũ�����±���ʾ��
CH3OH(g)��ʵ�����У���1L���ݵ��ܱ������н���ģ��ϳ�ʵ�顣��1 mol CO��2 mol H2ͨ�������У��ֱ������300���500�淴Ӧ��ÿ��һ��ʱ����������CH3OH��Ũ�����±���ʾ��
10min | 20min | 30min | 40min | 50min | 60min | |
300 �� | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500 �� | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
��300���500���Ӧ��ƽ�ⳣ����С��ϵΪK300��_________K500�����>������=����<������
�����й��ڸ÷�Ӧ��˵����ȷ����______________����ѡ����ĸ,��ͬ��
A���÷�Ӧ���κ��¶��¶����Է�����
B�������¶ȣ�����Ӧ���ʼ�С���淴Ӧ��������ƽ�����淴Ӧ�����ƶ�
C���¶�һ��ʱ��ѹǿ������ʱ��仯����˵����Ӧ�ﵽ��ƽ��״̬
D��ʹ�ø�Ч��������H������
��300 ��ʱ��ǰ10 min�ڣ��÷�Ӧ��ƽ����Ӧ����Ϊv(H2)��___mol/(L��min)��
�����д�ʩ�ܹ�����˷�Ӧ��CO��ת���ʵ���_________��
A. ����CO���� B. �����¶�
C. ʹ�����ʴ��� D. ���������ٳ���1 mol CO��2 mol H2
��500 ��ʱ�����ַ�Ӧ��ϵ���¶Ȳ��䣬60minʱ���������г���CH3OH�����H2��0.4mol����Ӧ����___�������Ӧ�������淴Ӧ�����������С��ٴδﵽƽ��ʱ��ƽ�ⳣ��Ϊ____________L2/mol2��
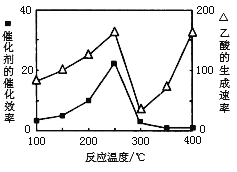
��3����TiO2��Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᡣ�ڲ�ͬ�¶��´����Ĵ�Ч����������������ʵĹ�ϵ����ͼ�������������������Ҫȡ�����¶�ʱ����Ӱ�췶Χ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ΰ����ĸ���Һ�䷴Ӧ��Ӧ�����ӷ���ʽ��д��ȷ����
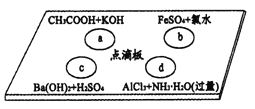
A. a��Ӧ��H����OH��![]() H2O
H2O
B. b��Ӧ��Fe2����Cl2![]() Fe3����2Cl��
Fe3����2Cl��
C. c��Ӧ��Ba2����![]() ��H����OH��
��H����OH��![]() BaSO4����H2O
BaSO4����H2O
D. d��Ӧ��Al3����3NH3��H2O��Al��OH��3����3![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ����Ʋ���ȷ����
A.��ʯ�ң�CaOB.��ʯ�ࣺ2CaSO4��H2O
C.���HCOOHD.Ӳ֬���ƣ�C17H35COONa
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס�����Ԫ�������ڱ��е����λ�����±�����������������Ӧˮ������ǿ��ˮ�ԣ��Ͷ���ͬһ���ڣ���ԭ������������ڲ������ͬ�������������ж���ȷ����(����)
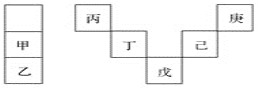
A. �������ԭ���������25
B. ��̬�⻯����ȶ��ԣ�����������
C. �����£����ҵĵ�������ˮ���ҷ�Ӧ
D. ������������������������ά
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���Na����Al3����Fe3����Cl����I����![]() ��
��![]() ��ij��ȤС���������ʵ�飺(1)ȡ��������Һ����������ᱵ��Һ����˵ð�ɫ��������Һ(2)��������ɫ�����м�������ϡHNO3�����ֳ�����ȫ�ܽ�(3)��(1)��������Һ�м����������ᣬ������Һ���ɫ,����������ȷ����
��ij��ȤС���������ʵ�飺(1)ȡ��������Һ����������ᱵ��Һ����˵ð�ɫ��������Һ(2)��������ɫ�����м�������ϡHNO3�����ֳ�����ȫ�ܽ�(3)��(1)��������Һ�м����������ᣬ������Һ���ɫ,����������ȷ����
A. ԭ��Һ�п��ܺ���Na����![]()
B. �ɣ�3���ƶ�ԭ��Һ�д���Fe3��
C. ԭ��Һ��һ����I��![]() ��Na��
��Na��
D. ͨ���ڻ�ɫ��Һ�м�����������Һ���Լ���ԭ��Һ���Ƿ����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�п�������Ƴ�ԭ��ص���(����)
A. CaO ��H2O===Ca(OH)2 B. NaOH��HCl===NaCl��H2O
C. 2KClO3![]() 2KCl��3O2�� D. Zn��2HCl===ZnCl2��H2��
2KCl��3O2�� D. Zn��2HCl===ZnCl2��H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���ķ���ʽΪC9H12�������ڷ�������ͬ���칹���У������������칹���� ��
A.6��B.7��C.8��D.9��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com