
����Ŀ��������I(C12H14O3)���Ʊ�Һ�����ϵ��м���֮һ��������к���ȩ����������I������E��H��һ�������ºϳɣ�
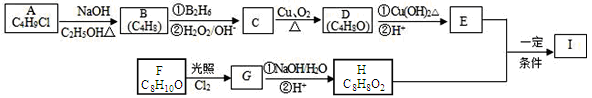
��֪������Ϣ���� A�ĺ˴Ź������ױ�����ֻ��һ�ֻ�ѧ�������⣻
��![]()
��������F�����ϵ�һ�ȴ���ֻ����������Fe3+����ɫ��
��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ���
��ش��������⣺
��1��A�Ľṹ��ʽΪ ��B���������ŵ�������
��2��C������Ϊ ��E�ķ���ʽΪ ��
��3��A��B��C��D�ķ�Ӧ���ͷֱ�Ϊ �� ��
��4��д��G��H�з�Ӧ���Ļ�ѧ����ʽ ��
��5��I�Ľṹ��ʽΪ ��
��6��I��ͬϵ��J��I����Է�������С28��J��ͬ���칹������ͬʱ����������������������ֻ������ȡ�����������ܷ���������Ӧ�������뱥��NaHCO3��Һ��Ӧ�ų�CO2������ ��(�����������칹)��J��һ��ͬ���칹�巢��������Ӧ���ữ��˴Ź�������Ϊ����壬�ҷ������Ϊ2��2��1��д��J������ͬ���칹��Ľṹ��ʽ____________________��
���𰸡�
��1����CH3��3CCl��̼̼˫����
��2��2-��-1-������C4H8O2��
��3����ȥ��Ӧ��������Ӧ��
��4��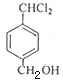 +2NaOH
+2NaOH![]()
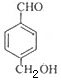 + 2NaCl + H2O��
+ 2NaCl + H2O��
��5��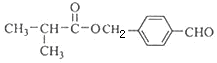 ��
��
��6��18��![]() ��
��
��������
���������A�ķ���ʽΪC4H9Cl���˴Ź������ױ�����ֻ��һ�ֻ�ѧ�������⣬��AΪ��CH3��3CCl�����������ƴ���Һ�����������·�����ȥ��Ӧ������BΪCH2=C��CH3��2��B������Ϣ2�еķ�Ӧ����CΪ��CH3��2CHCH2OH��C��������������DΪ��CH3��2CHCHO��D����������ͭ��Ӧ���ữ�õ�EΪ��CH3��2CHCOOH��F�ķ���ʽΪC8H10O�������ϵ�һ�ȴ���ֻ�����֣�Ӧ����2����ͬ�IJ������Ҵ��ڶ�λ����FΪ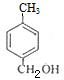 ���������ڹ��������·���ȡ����Ӧ������GΪ
���������ڹ��������·���ȡ����Ӧ������GΪ ��G����������ˮ��Һ����ˮ�ⷴӦ���ữ�õ�H������ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ�����HΪ
��G����������ˮ��Һ����ˮ�ⷴӦ���ữ�õ�H������ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ�����HΪ ��H��E����������Ӧ����I��������к���ȩ������������IΪ
��H��E����������Ӧ����I��������к���ȩ������������IΪ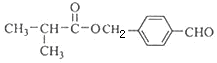 ��
��
��1��������������֪��AΪ��CH3��3CCl��BΪCH2=C��CH3��2������̼̼˫�����ʴ�Ϊ����CH3��3CCl��̼̼˫����
��2��������������֪��CΪ��CH3��2CHCH2OH������Ϊ2-��-1-������EΪ��CH3��2CHCOOH�������ʽΪC4H8O2���ʴ�Ϊ��2-��-1-������C4H8O2��
��3��A��B������ȥ��Ӧ��C��D����������Ӧ���ʴ�Ϊ����ȥ��Ӧ��������Ӧ��
��4��G����������ˮ��Һ����ˮ�ⷴӦ���ữ�õ�H����Ӧ���Ļ�ѧ����ʽΪ +2NaOH
+2NaOH![]()
 + 2NaCl + H2O��
+ 2NaCl + H2O��
��5��������������֪��I�Ľṹ��ʽΪ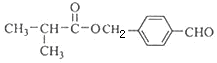 ���ʴ�Ϊ��
���ʴ�Ϊ��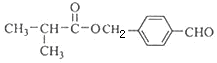 ��
��
��6��I��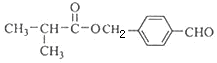 ����ͬϵ��J��I��Է�������С28��J��I��2��-CH2-ԭ���ţ�J��ͬ���칹������ͬʱ����������������������ֻ������ȡ�����������ܷ���������Ӧ�������뱥��NaHCO3��Һ��Ӧ�ų�CO2����J��ͬ���칹�庬��-CHO��-COOH������Ϊ-CHO��-CH2CH2COOH�����ڡ��䡢������λ�ã�����Ϊ-CHO��-CH��CH3��COOH�����ڡ��䡢������λ�ã�����Ϊ-CH2CHO��-CH2COOH�����ڡ��䡢������λ�ã�����Ϊ-CH2CH2CHO��-COOH�����ڡ��䡢������λ�ã�����Ϊ-CH��CH3��CHO��-COOH�����ڡ��䡢������λ�ã�����Ϊ-CH3��-CH��CHO��COOH�����ڡ��䡢������λ�ã��ʷ���������ͬ���칹����6��3=18�֣�J��һ��ͬ���칹�巢��������Ӧ���ữ��˴Ź�������Ϊ����壬�ҷ������Ϊ2��2��1����J��ͬ���칹�巢��������Ӧ���ữ��IJ��ﱽ������������2��Hԭ�ӣ��ʲ����б�����ֻ��1��Hԭ�ӣ�������2��-COOH��Ӧ������2��-CH2-��2��������ͬ�Ҵ��ڶ�λ�������в���Ϊ-CH2COOH���ʷ���������ͬ���칹��ṹ��ʽΪ��
����ͬϵ��J��I��Է�������С28��J��I��2��-CH2-ԭ���ţ�J��ͬ���칹������ͬʱ����������������������ֻ������ȡ�����������ܷ���������Ӧ�������뱥��NaHCO3��Һ��Ӧ�ų�CO2����J��ͬ���칹�庬��-CHO��-COOH������Ϊ-CHO��-CH2CH2COOH�����ڡ��䡢������λ�ã�����Ϊ-CHO��-CH��CH3��COOH�����ڡ��䡢������λ�ã�����Ϊ-CH2CHO��-CH2COOH�����ڡ��䡢������λ�ã�����Ϊ-CH2CH2CHO��-COOH�����ڡ��䡢������λ�ã�����Ϊ-CH��CH3��CHO��-COOH�����ڡ��䡢������λ�ã�����Ϊ-CH3��-CH��CHO��COOH�����ڡ��䡢������λ�ã��ʷ���������ͬ���칹����6��3=18�֣�J��һ��ͬ���칹�巢��������Ӧ���ữ��˴Ź�������Ϊ����壬�ҷ������Ϊ2��2��1����J��ͬ���칹�巢��������Ӧ���ữ��IJ��ﱽ������������2��Hԭ�ӣ��ʲ����б�����ֻ��1��Hԭ�ӣ�������2��-COOH��Ӧ������2��-CH2-��2��������ͬ�Ҵ��ڶ�λ�������в���Ϊ-CH2COOH���ʷ���������ͬ���칹��ṹ��ʽΪ��![]() ���ʴ�Ϊ��18��
���ʴ�Ϊ��18��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���������Ȼ�̼���Ҵ��������dz������л��ܼ�������ˮ���ܵ��� ��������ˮ�����ܶȱ�ˮС���� ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��ע����Ӧ����
�� �������Ʊ������飨C2H5Cl�� �� ��
�� ��ϩ��ˮ��Ӧ���Ҵ� �� ��
�� ����ȡ�屽 �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��K+��Cu2+��Ca2+��Al3+��AlO2-��CO32-��SO42-��Cl-�е�������������ɣ�ȡ��������Һ��������ʵ�飺
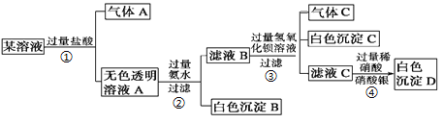
��������ʵ��ش��������⣺
(1)д������A�ĵ���ʽ ������C�Ľṹʽ ��
(2)д���������е����ӷ���ʽ �� ��
(3)��������ʵ�� (������������������)ȷ��ԭ��Һ�д���K+��˵������ ���������е����� (������������������)֤��ԭ��Һ�д���Cl-��˵������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵ�Ľ�����ȷ����
A��Al2O3���ͻ��������Ϊ�������۵��
B�����ά���к�ǿ�ĵ���������Ӧ��������ͨ�Ź���
C�������������ں������������Ϊ����������ǿ������������CO2��ˮ
D��FeCl3��Һ������ͭ��ӡˢ��·����������ΪFeCl3����ͭ���ʷ����û���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������;��˵����������ʵ����
A��SO2������ɱ�������� B��HF�����ڵ�̲���
C��NH3������������ D��SiO2��������̫���ܵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(10��)����14.4gCO��CO2�Ļ�����壬�ڱ�״������ռ�����ԼΪ8.96L���ش��������⣺

��1���û�������ƽ��Ħ������__________________________________��
��2�����������̼ԭ�ӵĸ���_____________________________��(��NA��ʾ����٤��������ֵ)
��3���������������ͨ����ͼװ�ã�����ռ�����������
���������ռ����������Ħ������_______________________��
��������������ռ�������������Ϊ__________________________��
���������ռ���������ĵ�������Ϊ__________________________��(��NA��ʾ����٤��������ֵ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʾ���ʱ仯�Ļ�ѧ����ʽ������ȷ����
A����ͭ����ʱ�����Դ�����������Ǵ�ͭ��������ӦʽΪCu��2e���TCu2+
B������ȼ�ϵ�صĸ�����Ӧʽ��O2+2H2O+4e���T4OH��
C���ö��Ե缫��ⱥ��ʳ��ˮʱ�������ĵ缫��ӦʽΪ2Cl����2e���TCl2��
D�����������绯ѧ��ʴ��������Ӧʽ��Fe��2e���TFe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ�������Ǵ�������(��Cr2O72-��CrO42-)��ҵ��ˮ�ij��÷������������£�
![]()
��֪ת�������еķ�ӦΪ2CrO42-(aq)+2H+(aq)![]() Cr2O72-(aq)+H2O(l)��ת����������Һ�и�Ԫ�صĺ���Ϊ28.6g��L��CrO42-��10/11ת��ΪCr2O72-������˵������ȷ����
Cr2O72-(aq)+H2O(l)��ת����������Һ�и�Ԫ�صĺ���Ϊ28.6g��L��CrO42-��10/11ת��ΪCr2O72-������˵������ȷ����
A. ��Һ��ɫ���ֲ��䣬˵���������淴Ӧ�ﵽƽ��״̬
B. �����̷�(FeSO4��7H2O)����ԭ��������1L��ˮ��������Ҫ458.7g
C. ������ת����Ӧ��ƽ�ⳣ��K��1��1014����ת����������Һ��pH��5
D. ������Ksp[Cr(OH)3]��1��10-32��Ҫʹ�������ˮ�е�c(Cr3+)����1��10-5mol��L��Ӧ����Һ��pH��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ����ڸ��¸�ѹ��CO���м��ߵĻ�ѧ���ԣ�������ֵ��ʻ��ﷴӦ��
��1����ҵ�ϳ�����ˮ�����絽���ȵ�̿����ʵ��ú���������Ƶ�CO��H2�����÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2������ú��������������̿�㽻�����������ˮ���������������Ŀ���� ����Ӧ���ɵ������ڼ��ȡ������������������ϳ�Һ��ȼ�ϼ״����÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3��һ�������£�CO��H2�ɺϳɼ��飬��Ӧ����ʽΪ��CO��g��+3H2��g��![]() CH4��g��+H2O ��g���������£��÷�Ӧ�ܹ��Է����е�ԭ���� ��
CH4��g��+H2O ��g���������£��÷�Ӧ�ܹ��Է����е�ԭ���� ��
��4��CO������ȼ�ϵ����ʹ�õĵ�����Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2�����õ�������ĵ缫��ӦʽΪ ��
��5����ҵ�Ͽ�ͨ���״��ʻ�������ȡ�����������Ӧ����ʽΪ��
CH3OH��g����CO��g��![]() HCOOCH3��g�� ��H =��29.1 kJ��mol��1
HCOOCH3��g�� ��H =��29.1 kJ��mol��1
������Ա������Ӧ�������о��������о�������£�
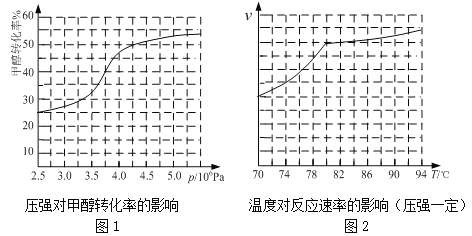
�����ݷ�Ӧ��ϵ��ѹǿ�Լ״�ת���ʵ�Ӱ�첢�ۺϿ��������ɱ����أ���ҵ��ȡ�������Ӧѡ���ѹǿΪ ��
a��3.5��106Pa b��4.0��106Pa c��5.0��106Pa
��ʵ�ʹ�ҵ�����в��õ��¶��� ���������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com