
【题目】(10分)现有14.4gCO和CO2的混合气体,在标准状况下所占的体积约为8.96L。回答下列问题:

(1)该混合气体的平均摩尔质量__________________________________;
(2)混合气体中碳原子的个数_____________________________;(用NA表示阿伏伽德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
①气球中收集到的气体的摩尔质量_______________________;
②标况下气球中收集到的气体的体积为__________________________;
③气球中收集到的气体的电子总数为__________________________;(用NA表示阿伏伽德罗常数的值)
【答案】(1)36g/mol (2) 0.4NA (3)① 28g/mol ②4.48L ③2.8NA
【解析】
试题分析:(1)混合气体的体积为8.96L,则物质的量为其物质的量为:n=![]() =
=![]() =0.4mol,
=0.4mol,
混合气体的平均摩尔质量为![]() =36g/mol;
=36g/mol;
(2)设混合气体中CO的物质的量为xmol,CO2的物质的量为ymol,则根据混合物的质量为14.4g可得:28x+44y=14.4 ①;根据气体的物质的量为0.4mol可得:x+y=0.4 ② 解①②得:x=0.2mol、y=0.2mol;由于CO和CO2中均含1个碳原子,故0.2molCO和0.2molCO2中共含0.4molC原子即0.4NA个;
(3)将混合气体依次通过如图装置,则CO2会被NaOH溶液吸收,剩余CO,被浓硫酸干燥后,则在气球中收集到的是干燥纯净的CO气体;
①气球中收集到的气体为CO,而一种物质的摩尔质量在数值上等于该物质的相对分子质量,故收集到气体的摩尔质量为28g/mol;
②气球中的气体为CO,其体积V=nVm=0.2mol×22.4L/mol=4.48L;
③一个CO含有14个电子,由(2)求出的CO的物质的量为0.2mol,则电子的物质的量为0.2mol×14=2.8mol,电子总数为2.8NA个。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机物A是一种重要化工生产的中间体,已知其结构简式如下图:
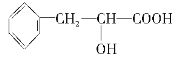
(1)A中含有的含氧官能团的名称
(2)A可能具有的化学性质有 (填写序号)。
①能与H2发生加成反应
②一定条件下可发生缩聚反应
③能与甲酸发生酯化反应
④能在浓硫酸和加热的条件下发生消去反应
⑤能与Ag(NH3)2OH溶液发生氧化反应
(3)A的一种同分异构体B,与Ag(NH3)2OH溶液混合于试管中水浴加热有银镜产生;B与浓溴水发生苯环上的取代反应时,1mol B能与3mol Br2恰好反应。请写出B发生银镜反应的化学方程式:
(只要求写出一个化学方程式,有机物写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的M层上的电子数比K层多5。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第 周期 族; ]
(2) C的离子结构示意图是 ,F中的化学键为 ;
(3) AB2的电子式为 ; F和AB2反应的化学方程式为 ;
(4) C、D、E三种元素的原子半径从小到大的顺序为 ; (用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法不正确的是( )
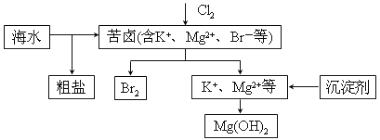
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C12H14O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:
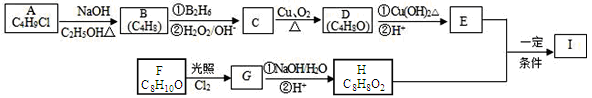
已知以下信息:① A的核磁共振氢谱表明其只有一种化学环境的氢;
②![]()
③化合物F苯环上的一氯代物只有两种且遇Fe3+不变色;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A的结构简式为 ,B所含官能团的名称是
(2)C的名称为 ,E的分子式为 。
(3)A→B、C→D的反应类型分别为 、 。
(4)写出G→H中反应①的化学方程式 :
(5)I的结构简式为 。
(6)I的同系物J比I的相对分子质量小28,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有 种(不考虑立体异构)。J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________方法区分晶体、准晶体和非晶体。
(2) 铁元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。基态Fe原子有________个未成对电子。
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“否”)平面型分子。
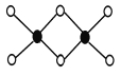
(4) Fe(CO)5 是一种配位化合物,该物质常温下呈液态,熔点为一20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断:该化合物的晶体中存在的作用力有( )
A.离子键 B.极性键 C.非极性键 D.范德华力 E.氢键 F.配位键
(5)很多金属盐都可以发生焰色反应,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会密切相关,下列说法正确的是
A.SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等
B.通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2
C.高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性
D.氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
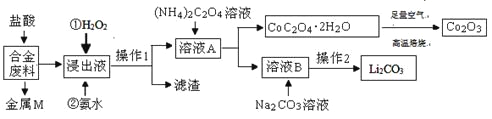
(1)金属M为__________。
(2)加入H2O2的作用是(用离子方程式表示)____________,加入氨水的作用是________。
(3)CoC2O4﹒2H2O高温焙烧的化学方程式为__________________________。
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其目的是___________,90℃时Ksp(Li2CO3)的值为___________。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/molL-1 | 0.21 | 0.17 | 0.14 | 0.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com