
����Ŀ���Ե�ʯ��[��Ҫ�ɷ�Ca(0H)2����Fe203��MgO��Si02������]Ϊԭ���Ʊ�����̼��Ƶġ��ֹ����������£�
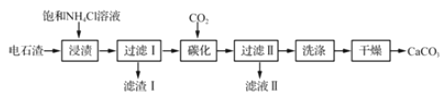
��1����ʯ������ˮ�γɵ�ʯ����ʱ�ᷢ����Ӧ�����ɵ������г�ˮ���______��
��2�������ա�ʱ��NH4Cl��Ca(0H)2��Ӧ�Ļ�ѧ����ʽΪ______��
��3�������ա�ʱ��һ��ʱ����Ca2+��ȡ�����¶ȱ仯��ͼ��ʾ��Ca2+��ȡ�����¶����߶�������ԭ�������______��
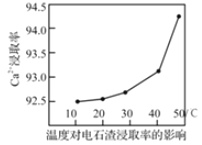
A.�¶����ߣ������ȡ��Ӧ���ʣ��Ӷ����Ca2+��ȡ��
B.�¶����ߣ���Һ���ȼ�С���Ӷ����Ca2+��ȡ��
C.�¶����ߣ�NH4Cl��Һˮ��̶ȼ�С���Ӷ����Ca2+��ȡ��
��4����̼����ʱ��-����õ��¹��գ���Ӧ�����ӷ���ʽΪ___��
��5����Һ���У���ѭ�����õ����ʵĻ�ѧʽΪ___��
��6����ϴ�ӡ�ʱ�������Ƿ�ϴ���ķ�����:__________��
���𰸡�CaSiO3 2NH4Cl��Ca(OH)2===CaCl2��2NH3��H2O AB Ca2���� 2NH3��H2O��CO2===CaCO3����2NH4+ ��H2O��Ca2����2NH3��H2O ��CO2===CaCO3����2NH4+ NH4Cl ȡ�������һ��ˮϴ��Һ���Թ��У���HNO3�ữ������AgNO3��Һ�����ް�ɫ������������ϴ��(�����а�ɫ����������δϴ��)
��������
��ʯ��[��Ҫ�ɷ�Ca(OH)2����Fe2O3��MgO��SiO2������]�����뱥���Ȼ�什��գ����ܽ�Ca(OH)2����Fe2O3��MgO������1ΪSiO2��ͨ�������̼��������̼��Ƴ�����������ϴ�Ӹ���ɵõ�̼��Ƴ̶ȣ���Һ��Ϊ��Σ��Դ˽����⡣
(1)��ʯ��[��Ҫ�ɷ�Ca(OH)2����Fe2O3��MgO��SiO2������]����ˮ������Ca(OH)2������ˮ����SiO2Ϊ������������ڼӦ�����κ�ˮ����SiO2�ܺ�Ca(OH)2��Ӧ����CaSiO3��ˮ��
(2)��������ʱ��NH4Cl��Ca(OH)2��Ӧ�����Ȼ��ƺͰ�������ѧ����ʽΪ2NH4Cl+Ca(OH)2�TCaCl2+2NH3H2O��
(3)A.�¶����ߣ�������Ӧ���ʣ��������¶ȣ��ɵ��°����ӷ���ʹƽ�������ƶ�����߸����ӵĽ�ȡ�ʣ���A��ȷ��
B. �¶������ܱ���Һ���ȼ�С���Ӷ����Ca2+��ȡ�ʣ���B��ȷ��
C.�����¶ȣ��ɴٽ�笠�����ˮ�⣬��Һ������ǿ�����Ca2+��ȡ�ʣ���C����
�ʴ�ΪAB��
(4)��̼����ʱ��һ����õ��¹��գ����ٰ����Ļӷ�����ַ�Ӧ������ʽΪCa2++2NH3H2O+CO2�TCaCO3��+2NH4++H2O��Ca2++2NH3+H2O+CO2�TCaCO3��+2NH4+��
(5)��Һ��Ϊ��Σ���Ҫ�ɷ�ΪNH4Cl����ѭ��ʹ�ã�
(6)����������Һ�е������ӣ���ͨ�����������ӵķ������飬������ȡ�������һ��ˮϴ��Һ���Թ��У���HNO3�ữ������AgNO3��Һ�����ް�ɫ������������ϴ��(�����а�ɫ����������δϴ��)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Al��Fe��Cu ����Ҫ�IJ���Ԫ�أ����������������Ź㷺��Ӧ�á��ش���������:
(1)��̬ Fe2+�ļ۵����Ų�ʽΪ _________���� __________��δ�ɶԵ��ӡ�
(2)�Ȼ����۵�Ϊ 194��,���������۵�Ϊ 2050�棬�����۵����ܴ��ԭ���� _________��
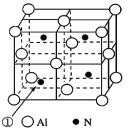
(3)���͵����γ�һ�־���������ṹ��Ԫ�ĸ��½ṹ�մɣ��侧������ͼ��ʾ�� ������ Al ����λ���� _________�����þ����ı߳�Ϊ a pm����þ�����ܶ�Ϊ_________g��cm3��(�� N ��ʾ�����ӵ�������ֵ)
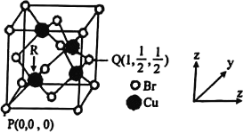
(4)һ��ͭ���廯�ᄃ���ṹ����ͼ��ʾ��Cu ����� Br ���������϶����ռ�ݴ����϶�İٷֱ�Ϊ__________���þ�����ͭ����λ����_________ ,������ڵ���ԭ����Ŀ��_________����ͼ�� P ��� Q ���ԭ�����������ȷ�� R ���ԭ���������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�������˵����ȷ����
A.���ͼױ�����ʹ���Ը��������Һ��ɫ
B.CH2=C(CH3)-CH=CH2������ʵ������巴Ӧ�������2��
C.����ʽΪC8H10�����ڷ�������ͬ���칹����3��
D.�����������顢��ϩ��ȫȼ��������������ǰ�߶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ǹ�ҵ���Ʊ�����������Ҫԭ�ϣ�����Ҫ�ɷ���Al2O3��ͬʱ������SiO2 ��Fe2O3����ҵ�Ͽ�ʹ�ü������ȡ�������е� Al2O3���乤ҵ������ͼ��ʾ������ͼʾ��Ϣ���ش��������⡣
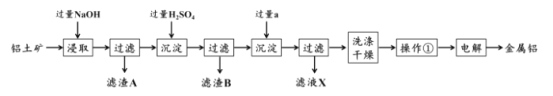
(1)Ϊ�����������Ľ�ȡЧ�ʣ��ɲ��õķ����ǣ�______��
(2)��һ�γ���ʱ������һϵ�����ӷ�Ӧ���������ɹ��� B �ķ�Ӧ�⣬��������������Ӧ����ֱ�д�����ǵ����ӷ���ʽ��_______��______��
(3)Һ���Լ� a �Ļ�ѧʽΪ_________��
(4)�ù��յĸ���Ʒ��������Һ X �У��� Na2SO4 �⣬����Ҫ�ɷ���________ (�ѧʽ)�����о�һ��ø���Ʒ�ڹ�ҵ�������ճ������е���;��________��
(5)�����ٵ�����Ϊ____������ʵ�����н��иò�������ƷӦ������_______�С�
(6)���һ�����ʱ������Ҫ������������ʯ���������� __________��
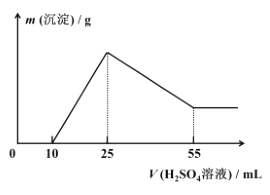
(7)ȡ 10.0 g ���������������ս��д��������ڹ�����ʹ�� 5.0 mol/L ��ϡ���ᡣ��һ�γ���ʱ���ó�����������������������仯��ϵ��ͼ��ʾ�������������Ʒ�� Al2O3 ����������Ϊ ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H3BO3)��һ��Ƭ��״�ṹ��ɫ���壬���ڵ�H3BO3����ͨ���������(����ͼ)�������й�˵����ȷ���ǣ� ��
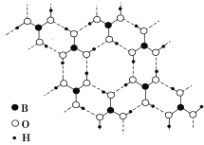
A. �����ᾧ������ԭ�Ӿ���
B. H3BO3���ӵ��ȶ���������й�
C. ��������ԭ�������Ϊ8�����ȶ��ṹ
D. ��1 mol H3BO3�ľ�������3 mol���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����
A. ��ˮ��ͨ��������������NH3H2O+SO2�TNH4++HSO3-
B. ���Ȼ�����Һ�м��������ˮ��Al3++3NH3��H2O��Al��OH��3��+3NH4+
C. ����Ȼ�þ��Һ��2Cl-+2H2O ![]() 2OH-+Cl2��+H2��
2OH-+Cl2��+H2��
D. ����������Һ�е�������������Һ��Ba2+ǡ����ȫ������Ba2++2OH-+2H++SO42-=BaSO4��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ��У�C6H5CH2Cl����һ����Ҫ���л���ѧԭ�ϡ���ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��С�
��1��д��ʵ������ȡ�����Ļ�ѧ����ʽ___��
��2�������з��������Ȼ��дֲ�Ʒ�Ĵ��ȡ�
����1����ȡ5.11g��Ʒ����ƿ�У�����200.00mL4mol/L����������Һ���ȣ���ȴ�����¡����� 200.00mL4mol/L���ᣬһ��ʱ�����ƿ�е���Һȫ��ת����250.00 mL ������ƿ��,��ˮ���ݡ�
�������ƿ�и���25.00 mL��Һ����ֻ��ƿ�У�������25.00 mL0.2000mol/L��������Һ��
�i���:�����������ָʾ������0.2000 mol/LNH4SCN��Һ�ֱ�ζ�ʣ��������������õζ��������±���
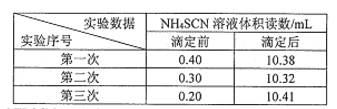
�ټ��������Ŀ����_________��
���ڲ��������У��жϴﵽ�ζ��յ��������_______��
�۸���Ʒ���Ȼ��е�����������д��������̣�__________��
�������ⶨ���ӭ�������Ȼ�������Ԫ�ص����ۺ�����ԭ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ķϽ���м����Ҫ�ɷ�ΪCu��Fe��Al�������������Al2O3��Fe2O3��Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС���������ʵ�����̣��øù����ĺϽ������ȡ�Ȼ������̷�����(FeSO4��7H2O)�͵������塣
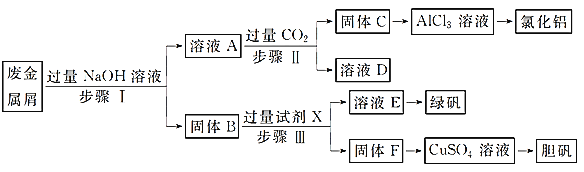
��ش�
��д����������Ӧ�����ӷ���ʽ��_______________________��
���Լ�X��______________��D��______________��
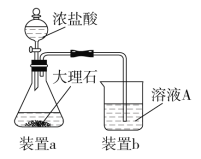
���ڲ�����ʱ������ͼװ����ȡCO2��ͨ����ҺA�С�һ��ʱ��۲쵽�ձ��в����İ�ɫ���������١�Ϊ�������C���٣��ɲ�ȡ�ĸĽ���ʩ��_____________________��
���ɹ���F��ȡ����ͭ��Һ��ͨ�������ַ�����
����һ��������F�ڼ�����������Ũ���ᷴӦ��
��������������FͶ���ȵ�ϡ�����У�Ȼ��ͨ��������
����һ��ȱ��Ϊ��_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ������
A.CH4![]() H2
H2![]() H2OB.N2
H2OB.N2![]() NH3
NH3![]() NH4Cl
NH4Cl
C.Cu![]() NO2
NO2![]() HNO3D.CH2=CH2
HNO3D.CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com