
����Ŀ����֪����Ԫ�ص�ԭ��������С˳��ΪC>A>B>D>E��A��Cͬ���ڣ�B��Cͬ���塣A��B�γɵ����ӻ�����A2B���������ӵĵ�������ͬ�����������Ϊ30��D��E���γ�4��10�����ӵķ��ӡ��Իش��������⣺
��1��д������Ԫ�ص����ƣ�A________B_______C__________D_________
��2���õ���ʽ��ʾ������A2B���γɹ��̣�______________________��
��3��д��DԪ���γɵĵ��ʵĽṹʽ��__________________________��
��4��A��B����Ԫ����ɵĻ�����A2B2���ڵĻ�ѧ����________________��
��5��д���������ʵĵ���ʽ��E��B�γɵĻ�����__________________��A��B��E�γɵĻ�����_____________��
���𰸡� �� �� �� �� ![]() N��N ���Ӽ����ۼ�
N��N ���Ӽ����ۼ� ![]() ��
��![]()
![]()
��������A��B�γ����ӻ�����A2B���������ӵĵ�������ͬ���ҵ�������Ϊ30������ÿ�����Ӷ���10�����ӣ��ɻ�ѧʽ�Ľṹ��֪��B��2����λ����ɣ�A��1����λ����ɣ�����A��NaԪ�أ�B��OԪ�أ���ΪA��Cͬ���ڣ�B��Cͬ���壬����CΪSԪ�أ�D��E���γ�4��10���ӵķ��ӣ�ԭ������B��D��E����֪�÷�����NH3������D��NԪ�أ�E��HԪ�أ���
��1���������Ϸ�����֪AΪ�ƣ�BΪ����CΪ��DΪ������2��A2B��Na2S������Ϊ���ӻ�����õ���ʽ��ʾNa2S���γɹ���Ϊ![]() ����3�������ĽṹʽΪN��N����4��A��B����Ԫ����ɵĻ�����A2B2�ǹ������ƣ����ڵĻ�ѧ�������Ӽ����ۼ�����5��E��B�γɵĻ�������ˮ��˫��ˮ������ʽΪ
����3�������ĽṹʽΪN��N����4��A��B����Ԫ����ɵĻ�����A2B2�ǹ������ƣ����ڵĻ�ѧ�������Ӽ����ۼ�����5��E��B�γɵĻ�������ˮ��˫��ˮ������ʽΪ![]() ��
��![]() ��A��B��E�γɵĻ�����Ϊ�������ƣ�NaOH�к��������������������ӹ��ɵ����Ӽ���O��H�γɹ��ۼ�������ʽΪ
��A��B��E�γɵĻ�����Ϊ�������ƣ�NaOH�к��������������������ӹ��ɵ����Ӽ���O��H�γɹ��ۼ�������ʽΪ![]() ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D���ֶ�����Ԫ��, ���ǵ�ԭ��������A��D��������, ��֪A��Bԭ������ͬ�ĵ��Ӳ���, ��A��L���������K�������������, C�ڿ�����ȼ��ʱ���ֻ�ɫ����, C�ĵ����ڼ�������B�ĵ��ʳ�ַ�Ӧ, ���Եõ���D������ɫ��ͬ�ĵ���ɫ��̬������, �Ը������������ش�:
��1��Ԫ������: A ______ B _____ C _____ D ______
��2��DԪ��λ�����ڱ���___________����____________��
��3��д��AB2��C2B2��Ӧ�Ļ�ѧ����ʽ��________________________________________��
��4������ʽ��ʾ������ C2D ���γɹ��̣�________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1g������ȫȼ������ˮ����ʱ�ų�����121kJ����������1mol O=O����ȫ����ʱ��������496kJ��ˮ������1mol H��O���γ�ʱ�ų�����463kJ����������1mol H��H������ʱ��������Ϊ�� ��
A.920kJ
B.557kJ
C.436kJ
D.181kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�������������ᷢչ�Ļ������о���ѧ��Ӧ�е������仯�������ڸ��õ����û�ѧ��ӦΪ�������������
��1����Ȼ���Ϳ�ȼ��(mCH4nH2O)���Ǹ�Ч�ྻ����Դ��Ҳ����Ҫ�Ļ���ԭ�ϡ�
����ȼ��(mCH4nH2O)����_____���壬д��CH4�Ľṹʽ______��
����֪25�桢101kPaʱ��1g������ȫȼ������Һ̬ˮ�ų�55.65kJ��������������·�ӦCH4(g)+2O2(g)=CO2(g)+2H2O(l)�� ��H=___kJ/mol��
��2���ü���--��������(KOH��Һ)ȼ�ϵ������Դ�����CuCl2��Һ����Ӧװ������ͼ��ʾ��

��b�缫����Ϊ______��d�缫�ĵ缫��ӦʽΪ__________��
������CuCl2��Һ��������ij�缫������3.2g����Cuʱ��������ȼ�ϵ�����ĵ������ڱ�״���µ������_______mL��
��3��25�棬101kPa�����£�14gN2��3gH2��Ӧ����NH3�������仯����ͼ��ʾ��
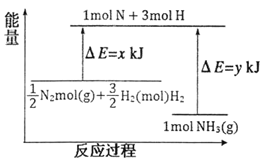
��֪:��x=1127��
��25�棬101kPa�£�N2(g)+3H2(g)![]() 2NH3(g) ��H=-92kJmol-1����y=______��
2NH3(g) ��H=-92kJmol-1����y=______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�����������������Һһ�������Ե��ǣ�������
A.�������Al��Ӧ�ų�H2����Һ
B.�ӷ�̪������ɫ����Һ
C.pH=6��ij��Һ
D.c��H+����c��OH����������ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɡ�
��ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼ1װ����һ�������ͬ����Ԫ��C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о���
��ͬѧ�������ͼ2װ������֤±��Ԫ�����ʵĵݱ���ɣ�ͼ2��A��B��C�����ֱ���մ��NaBr��Һ������ʪ��ĵ���KI��ֽ��ʪ��ĺ�ֽ��
��֪������Ũ�������������ܷ�Ӧ����������

��1������������������ѡ����ͬѧ��Ƶ�ʵ�����õ����ʣ�ͼ1���Լ�A��BΪ������ţ�____��
��ϡ������Һ�� ��Ũ��� ��̼���Ʒ�ĩ����Na2SO3��Һ
д��ͼ1��ƿ�з�����Ӧ�����ӷ���ʽΪ__________________________________________��
��2����ͬѧ����ʵ��ͼ1�ձ�������Ϊ____________________________________��
��3����ͬѧ����ʵ��ͼ2��B��������Ϊ__________________________________��
��4��д��ͼ2��A��������Ӧ�����ӷ���ʽΪ__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X��Y��Z��Ԫ�ص�ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С��Y��Zԭ������������֮��Ϊ10��C��D����X��Y��Z������Ԫ����ɵĻ����Cͨ��״����Ϊ��ɫҺ�壬 DΪ��ɫ�ǿ�ȼ�����壬GΪ����ɫ�������壬J��MΪ������I��Ư�����ã���Ӧ�ٳ���������ӡˢ��·�塣������֮���ת����ϵ����ͼ������������ʡ�ԡ���ش��������⣺
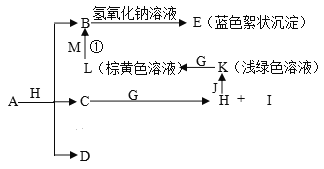
��1��д��A�Ļ�ѧʽ__________________��C�ĵ���ʽ______________________��
D�Ľṹʽ______________________________��
��2����22.4L����״����D����ͨ��1L 1mol/L NaOH��Һ�У���ȫ���պ���Һ�г���Na���⣬���������ڵ�������______________________________��
��3����֪M����ϡ���ᣬ��Һ�����ɫ�����ų���ɫ���塣��д���÷�Ӧ�����ӷ���ʽ___________________________________________________________��
��4�����黯����K�������ӵ�ʵ�鷽����______________________________________
��5��д����ӦK+G��L�Ļ�ѧ����ʽ��________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ��ȷ�ӦZn��H2SO4===ZnSO4��H2��������������ȷ����(����)
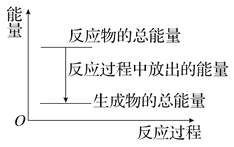
A. ��Ӧ�����е�������ϵ������ͼ��ʾ
B. 1 mol Zn����������1 mol H2������
C. ���������Ϊԭ��أ���п������
D. ���������Ϊԭ��أ�����32��5 g Zn�ܽ�ʱ�������ų�������һ��Ϊ11��2 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵͼ����ĸ����Ԫ�أ�������ȷ����
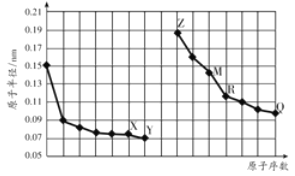
A. R�����ڱ��ĵ�15��
B. Y��Q����Ԫ�ص���̬�⻯�P������������ˮ�����Ϊǿ��
C. �����ӵİ뾶:X>Z>M
D. Z�ĵ����ܴ�M��QԪ�ع��ɵ�����Һ���û�������M
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com