
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是_____,该错误操作会导致测定结果___________
(2)判断滴定终点的现象是:________________________________________
(3)如图是某次滴定时的滴定管中的液面,其读数为_______ mL。
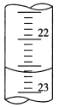
【答案】① 偏大 锥形瓶中溶液从无色变为粉红色,且半分钟不变色 22.60
【解析】
(1)碱式滴定管在装液前没有用所装液体进行润洗并据此分析误差;
(2)根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)滴定管的最小读数为0.01mL,滴定管0刻度在上方,结合图示液面判断溶液体积。
(1)碱式滴定管在装液前应用所装液体进行润洗,用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上,碱式滴定管未用标准氢氧化钠溶液润洗,就直接注入标准NaOH溶液,会造成标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=![]() 可知,c(待测)偏大,故答案为:①;偏大;
可知,c(待测)偏大,故答案为:①;偏大;
(2)滴定时,当溶液颜色变化且半分钟内不变色,可说明达到滴定终点,所以当滴入最后一滴氢氧化钠溶液,溶液由无色变为粉红色,且半分钟内不褪色,故答案为:当滴入最后一滴氢氧化钠溶液,溶液由无色变为粉红色,且半分钟内不褪色;
(3)根据图示可知,滴定管中的液面读数为22.60mL,故答案为:22.60。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在容积固定的密闭容器中存在反应:A(g)+3B(g)![]() 2C(g) △H<0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g) △H<0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:

下列判断正确的是
A. 图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B. 图Ⅱ研究的是温度对反应的影响,且甲的温度较高
C. 图Ⅱ研究的是压强对反应的影响,且甲的压强较大
D. 图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院理化技术研究所张铁锐等人成功制备了超薄LDH纳米片光催化剂,实现了在常温常压和可见光或直接太阳辐射下N2和H2O合成氨,其原理示意图如下。下列说法正确的是( )
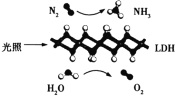
A.在该合成氨反应条件下,每转移2NA个电子需要22.4L的H2O
B.反应前后极性键的数目不变
C.LDH是反应的催化剂,并不参与反应
D.反应中氧化产物与还原产物的物质的量之比为4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图X是直流电源。Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒。接通电路后,发现d附近显红色。

(1)①电源上b为___极
②Z槽中e为___极。
③连接Y、Z槽线路中,电子流动的方向是d___e(用“→”或“←”填空)。
(2)①写出Y槽中总反应的化学方程式:____。
②写出Z槽中e极上反应的电极反应式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
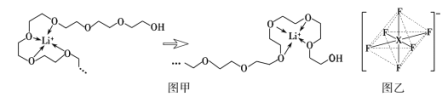
①聚乙二醇分子中,碳、氧的杂化类型分别是___、___。
②从化学键角度看,Li+迁移过程发生___(填“物理变化”或“化学变化”)。
③PF6中P的配位数为___。
④相同条件,Li+在___(填“LiPF6”或“LiAsF6”)中迁移较快,原因是___。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的品胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为___g·cm-3(列出计算表达式)。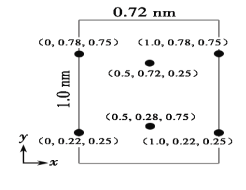
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是( )
A. 沸点:戊烷>2,2-二甲基戊烷>2,3-二甲基丁烷>丙烷
B. 密度:CCl4>CHCl3>H2O>苯
C. 含氢质量分数:甲烷>乙烷>乙烯>乙炔>苯
D. 等质量的物质燃烧耗O2量:苯>乙烷>乙烯>甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
A.CH3CH2CH2CH2CH2OH B.(CH3)2COHCH2CH3
C.(CH3)2CHCH2CH2OH D.(CH3)3CCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分离与提纯是化学实验的重点。根据下列实验目的,分别选择相应的实验装置,将其实验编号填在对应的横线上。
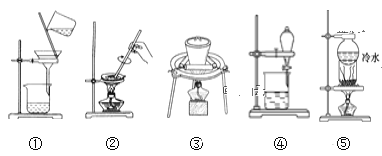
(1)从溴水中提取溴__。
(2)除去氧化钙中的碳酸钙__。
(3)分离食盐和碘的混合物__。
(4)除去硫酸钡固体中少量的硝酸钾__。
(5)从氯化钠溶液中得到氯化钠晶体__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应。钠及其氧化物的物质的量 均为0.1 mol,水的质量为100 g。下列说法正确的是

A.甲、乙、丙都属于氧化还原反应
B.甲反应的离子方程式为Na+2H2O![]() Na++2OH-+H2↑
Na++2OH-+H2↑
C.丙充分反应,能产生0.05 mol O2,转移电子0.1 mol
D.甲、乙、丙充分反应后所得溶液的质量分数分别为w1、w2、w3,则2w1=w2=w3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com