
【题目】下列选项中原因或结论与现象对应的是
选项 | 现象 | 原因或结论 |
A | 将NO2球浸泡在热水中,球中气体颜色加深 | 2NO2(g) △H=-56.9kJ·mol-1,升温平衡向生成NO2方向移动 |
B | 在密闭容器中有反应:A(g)+B(g) | x=l,增大压强平衡正向移动 |
C | 向装有2mL5%H2O2溶液的两只试管中分别滴0.lmol·L-1 FeCl3和CuSO4溶液各lmL,摇匀。滴入 FeCl3溶液产生的气泡更快些 | Fe3+的催化效果比Cu2+的好 |
D | 常温下将铝片放入浓硝酸中无明显现象 | 常温下铝和浓硝酸不反应 |
A. A B. B C. C D. D
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】下列电离方程式中,正确的是
A. K2SO4=2K++SO4-2 B. Ba(OH)2=Ba2++OH2-
C. Mg(NO3)2=Mg2++2(NO3)2- D. Fe2(SO4)3=2Fe3++3SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝“确定为食品污染之一”而加以控制。铝在下列场合须加以控制的是( )
①糖果内包装 ②电线电缆 ③牙膏皮 ④氢氧化铝胶囊(作内服药) ⑤用明矾和小苏打作出食物膨化剂.
A.①③④⑤B.②③④⑤C.②③⑤D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示,根据以上微观示意图得出的结论中,正确的是( ) 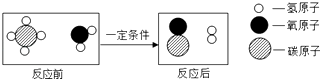
A.反应前后各元素的化合价均不变
B.水煤气的成分是一氧化碳和氧气
C.该反应中含氢元素的化合物有3种
D.该反应的化学方程式中甲烷和水的计量数之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象能正确反映对应的实验操作的是( )
A.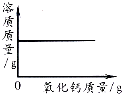 向一定量的饱和石灰水中加入氧化钙
向一定量的饱和石灰水中加入氧化钙
B.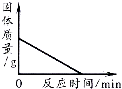 加热一定量高锰酸钾固体产生氧气
加热一定量高锰酸钾固体产生氧气
C.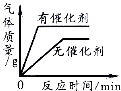 用一定量的双氧水制取氧气
用一定量的双氧水制取氧气
D.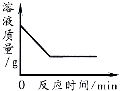 向一定量的硝酸银溶液中插入铜丝
向一定量的硝酸银溶液中插入铜丝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 在托盘天平上放两片大小、质量一样的纸,然后将氢氧化钠放在纸片上称量
B. 把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液移入容量瓶
C. 用蒸馏水洗涤烧杯、玻璃棒2—3次,洗涤液也移入容量瓶
D. 沿玻璃棒往容量瓶中加入蒸馏水,到刻度线1—2cm时改用胶头滴管滴加,直到溶液凹液面恰好与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A和B是前三周期的元素,它们的离子A2﹣、B3+具有相同的电子层结构。下列说法中正确的是( )
A.原子序数:A>BB.原子半径:A>B
C.离子半径:A2﹣>B3+D.质子数:A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的化学方程式或离子方程式正确的是
A. 氯气用于自来水的杀菌消毒:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 将“NO2球”浸泡在热水中,颜色变深:2NO2(g)![]() N2O4(g) △H<0
N2O4(g) △H<0
C. 向Ba(OH)2溶液中滴加NaHSO4溶液,至溶液呈中性:OH-+ Ba2++ H++SO42-== BaSO4↓+ H2O
D. 除去铁粉中的杂质Al:Al+2OH-== AlO2-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不能证明H2(g)+I2(g)2HI(g)已达平衡状态的是
A. 一个H﹣H 键断裂的同时有两个H﹣I键断裂
B. 恒温恒容时,某一生成物浓度不再变化
C. 恒温恒容时,混合气体颜色不再变化
D. 恒温、压强一定,体积可变的容器,混合气体的密度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com